
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Інструкція до навчальної практики №9
Дата__________________ Тема: Метод комплексонометрії. Мета: Закріпити теоретичні знання, набути практичних умінь та навичок проведення хімічного аналізу методом комплексонометрії.
В.В. Болотов Аналітична хімія X.: Оригінал, 2004, с Д.Д. Луцевич Аналітична хімія К.: Здоров'я, 2003, с План. 1. Приготування вихідного розчину – MgSO4 ·7H2O 2.Приготування робочого розчину Трилону Б. 3.Стандартизація робочого розчину
Характеристику методу за алгоритмом. Методику проведення кількісного визначення
Провести кількісне визначення досліджуваної речовини у розчині даним методом. Приготування вихідного розчину – MgSO4 ·7H2O
Приготування робочого розчину – Трилону Б
Стандартизація робочого розчину –Трилону Б (за вихідним розчином MgSO4 · 7H2O)
Підпис викладача:___________________________ Інструкція до навчальної практики №10
Дата__________________ Тема: Аналіз вмісту МgSO4, ZnS04. Аналіз води.
Мета: Провести аналіз вмісту лікарських препаратів МgS04 і ZnS04 води методом комплексонометрії Література: В.В. Болотов Аналітична хімія X. Оригінал, 2004, с.268-276 Д.Д. Луцевич Аналітична хімія К.: Здоров'я, 2003, с.241-244 План: Аналіз вмісту МgS04 і ZnS04 в лікарських препаратах. Аналіз води. Знати: 1. Теоретичні основи методу комплексонометрії. Методику визначення вмісту МgS04 і ZnS04 в лікар ських препаратах Методику аналізу води Уміти: 1. Аналізувати вміст МgSO4, ZnS04 в в лікарських препаратах Проводити аналіз води. Обчислювати і оформляти результати лабораторних досліджень Лабораторна робота Обладнання та реактиви: вимірювальні колби V=50; 100;1000 см3, лійка, бюретка V= 25,00 см3, піпетка градуйована V= 10,0 (5,0) см3, колба Ерленмейера, трилон Б, МgSO4, ZnS04, амонійна буферна суміш, хромоген темно-синій, вода з різних джерел. Хід роботи
Аналіз досліджуваної речовини:(Спосіб титрування прямий)
Аналіз досліджуваної речовини:(Спосіб титрування прямий)
Аналіз води
У колбу відміряти 50 см3 водопровідної води, (джерельної) прилити 15 см3 амонійної буферної суміші та 5 краплин хромогену темно-синього, титрувати розчин до появи синього забарвлення. Обчислити Т(твердість води ммоль екв/дм3) за формулою Т = С(екв)(тр) *V(тр) * 1000 / V(Н2О)
1. Що лежить в основі методу трилонометрії? 2. Як виконується умова титрування при певному рН? 3. Який колір індикатору еріохрому чорного Т при рН 8,0-10,0? 4. Якого кольору комплекси індикатору еріохрому чорного Т з металами? 5. ________________________________________________________________________________________________________________________ 6. Який спосіб титрування застосовують для визначення катіонів кальцію, магнію, барію, цинку тощо? 7. Який спосіб титрування застосовують для визначення аніонів? 8. Для визначення твердості 50 см3 води витратилось 2,3 см3 0,1 моль/дм3розчину трилону Б з К=0,98. Розрахувати твердість води.
9. 25,00 см3 розчину, що містить 0,7200 г солі алюмінію в 100 см3, обробили 20,00 см3 розчину 0,1024 моль/дм3 трилону Б. Надлишок реагенту відтитрували 22,08 см3 розчину 0,0503 моль/дм3 цинку (II) сульфату. Визначити масову відсоткову частку алюміній (III) - іонів у зразку.
10. Розрахувати вміст СаС12 (%) в розчині, на титрування 20,00 см3 якого витратилось 22,8 см3 0,1 М розчину Трилону Б (К= 1,021)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 137; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.58.60.192 (0.017 с.) |
 Література
Література Знати:
Знати: Уміти:
Уміти:


 0,1
0,1 




 1. 2. 3.
Зважити (q) у бюксі на: техно-хімічних терезах(1),
Зважити(q) у бюксі на аналітичних терезах(2) (mаналіт) =
Висипати (q) у вимірювальну колбу(3),
Зважити порожній бюкс на аналітичних терезах(mб.)=
q(практ) = m(аналіт) – m(б.); q(практ)=
1. 2. 3.
Зважити (q) у бюксі на: техно-хімічних терезах(1),
Зважити(q) у бюксі на аналітичних терезах(2) (mаналіт) =
Висипати (q) у вимірювальну колбу(3),
Зважити порожній бюкс на аналітичних терезах(mб.)=
q(практ) = m(аналіт) – m(б.); q(практ)=
 ;
; 
 ;
;
 ; К=
; К=  Т=
Т=






 1. 2. 3.
Зважити (q) у бюксі на: техно-хімічних терезах(1),
Зважити(q) у бюксі на аналітичних терезах(2) (mаналіт) =
Висипати (q) у вимірювальну колбу(3),
Зважити порожній бюкс на аналітичних терезах(mб.)=
q(практ) = m(аналіт) – m(б.); q(практ)=
1. 2. 3.
Зважити (q) у бюксі на: техно-хімічних терезах(1),
Зважити(q) у бюксі на аналітичних терезах(2) (mаналіт) =
Висипати (q) у вимірювальну колбу(3),
Зважити порожній бюкс на аналітичних терезах(mб.)=
q(практ) = m(аналіт) – m(б.); q(практ)=
 ;
; 
 ;
;


 1 2
Зважити (q) у бюксі на: техно-хімічних терезах(1),
Висипати (q) у вимірювальну колбу(2),
1 2
Зважити (q) у бюксі на: техно-хімічних терезах(1),
Висипати (q) у вимірювальну колбу(2),
 Трилон Б
MgSO4
+NH4OH
+NH4Cl
+хромоген
Трилон Б
MgSO4
+NH4OH
+NH4Cl
+хромоген
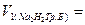


 ; Vс. =
; Vс. =
 ;
;
 =
=
 – об’єм, який взято для титрування
– об’єм, який взято для титрування
 – середній об’єм, який затрачено на титрування
– середній об’єм, який затрачено на титрування
 ;
;

 ; К=
; К=
 q ().=
q ().=




 1 2 3
2.Зважити (q) у бюксі на: техно-хімічних терезах(1),
3.Зважити(q) у бюксі на аналітичних терезах (2) mаналіт =
4.Висипати (q) у колбу(3) Ерленмейєра,
5.Зважити порожній бюкс на аналітичних терезах(mб.)=
6.q(практ) = m(аналіт) – m(б.); q(практ)=
7.Протитрувати трилоном Б у присутності розчинів амонійної буферної суміші та хромогену до зміни забарвлення_____________
Обчислення:
1.
1 2 3
2.Зважити (q) у бюксі на: техно-хімічних терезах(1),
3.Зважити(q) у бюксі на аналітичних терезах (2) mаналіт =
4.Висипати (q) у колбу(3) Ерленмейєра,
5.Зважити порожній бюкс на аналітичних терезах(mб.)=
6.q(практ) = m(аналіт) – m(б.); q(практ)=
7.Протитрувати трилоном Б у присутності розчинів амонійної буферної суміші та хромогену до зміни забарвлення_____________
Обчислення:
1.  q ()=
2.
q ()=
2.  w =
w =

 4.Наважку у (см3) х 10
4.Наважку у (см3) х 10



 5.Протитрувати
Обчислення:
5.Протитрувати
Обчислення:
 ;
C(
;
C( )=
)=
 q (
q ( )=
)=
 w=
w=

 q =
2.У 100г. р-ну 10,0% міститься – 10,0 г. (досл.)
х(m)– q г.
х(m)=
3.
q =
2.У 100г. р-ну 10,0% міститься – 10,0 г. (досл.)
х(m)– q г.
х(m)=
3.  ; V піп.к. =
4. Навжку у (см3)
; V піп.к. =
4. Навжку у (см3) 
 ,
, 
 протитрувати трилоном Б у присутності розчинів амонійної буферної суміші та хромогену до зміни забарвлення_____________
Обчислення:
протитрувати трилоном Б у присутності розчинів амонійної буферної суміші та хромогену до зміни забарвлення_____________
Обчислення:




