
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Стандартизація робочого розчину NaOH (за титрованим розчином HCl)
NaOH+ HCl→NaCl + H2O
T(NaOH) =
К 2.Аналіз досліджуваної речовини:
а)сильної кислоти сильним гідроксидом; __________________б) слабкої кислоти сильним гідроксидом _____________ в) слабкого гідроксиду сильною кислотою?________________________________________________
________________________________________________________________________________________________________________________________________________________________________________________________________________
моль екв /дм3. Луг чи кислота в надлишку і скільки? ________________________________________________________________________________________________________________________________________________________________________________________________________________
Підпис викладача:_____________________ Інструкція до навчальної практики №6 Дата__________________ Тема: Метод Мора. Мета: Закріпити теоретичні знання, набути практичних умінь та навичок проведення хімічного аналізу методом аргентометрії
В.В. Болотов Аналітична хімія X.: Оригінал, 2004, с Д.Д. Луцевич Аналітична хімія К.: Здоров'я, 2003, с План. 1.Приготування вихідного розчину натрій хлориду з СN = 0,05 моль екв/дм3. 2.Стандартизація робочого розчину аргентум нітрату.
Характеристику методу за алгоритмом. Методику проведення кількісного визначення
Провести кількісне визначення досліджуваної речовини у розчині даним методом. Лабораторна робота
|
||||||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 290; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.102.225 (0.006 с.) |
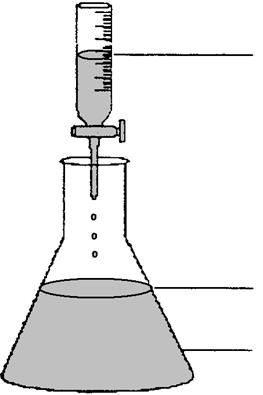 HCl
ф/фталеїн
HCl
ф/фталеїн
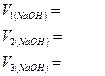
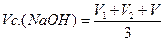 ;
; 
 ;
; 
 – точнийоб’єм, який взято для титрування
– точнийоб’єм, який взято для титрування – середнійоб’єм, який затрачено на титрування
– середнійоб’єм, який затрачено на титрування ;
; ;
; =
=
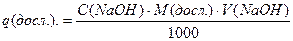 ;
q досл.=
2.
;
q досл.=
2. 





 1 2 3 4
3.Зважити (q) у бюксі на: техно-хімічних терезах(1),m=______
4.Зважити(q) у бюксі на аналітичних терезах (2) mаналіт =___
5.Висипати (q) у вимірювальну колбу(3),
6.Зважити порожній бюкс на аналітичних терезах(mб.)=_____
7.q(практ) = m(аналіт) – m(б.); q(практ)=________________
8. Точний об’єм (10см3 )досліджуваного розчину помістити у колбу для титрування.
9.Протитрувати (тричі) хлоридною кислотою у присутності індикатора _________ до зміни забарвлення_____________
1 2 3 4
3.Зважити (q) у бюксі на: техно-хімічних терезах(1),m=______
4.Зважити(q) у бюксі на аналітичних терезах (2) mаналіт =___
5.Висипати (q) у вимірювальну колбу(3),
6.Зважити порожній бюкс на аналітичних терезах(mб.)=_____
7.q(практ) = m(аналіт) – m(б.); q(практ)=________________
8. Точний об’єм (10см3 )досліджуваного розчину помістити у колбу для титрування.
9.Протитрувати (тричі) хлоридною кислотою у присутності індикатора _________ до зміни забарвлення_____________
 ; V(досл) (10,00 см3)
C( ) =
; V(досл) (10,00 см3)
C( ) =
 q ( ) =
q ( ) =
 ; w()=
; w()=
 .
q HСІ=
2.У 100г. р-ну 36,5% міститься –36,5. (HСІ)
х(m)– q г.
х (m)=
3.
.
q HСІ=
2.У 100г. р-ну 36,5% міститься –36,5. (HСІ)
х(m)– q г.
х (m)=
3.  ;V піп.к. =
4.
;V піп.к. =
4.

 HСІ →
HСІ → 
 ← H2O
← H2O  5.Протитрувати лугом у присутності індикатора _________ до зміни забарвлення_____________
6.Обчислення:
1.
5.Протитрувати лугом у присутності індикатора _________ до зміни забарвлення_____________
6.Обчислення:
1.  ; V (HСІ)(10,00см3)
C(HСІ)=
2.
; V (HСІ)(10,00см3)
C(HСІ)=
2.  q(HCІ)=
3.
q(HCІ)=
3. 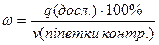 ;
w=
;
w=

 Контрольні завдання
Контрольні завдання 
 Література
Література Уміти:
Уміти:


