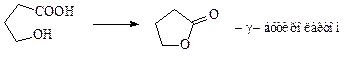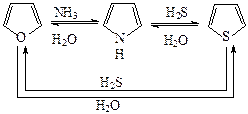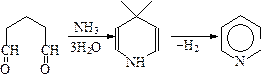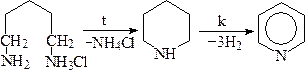Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Сложноэфирная конденсация Кляйзена.
Сложноэфирная конденсация Кляйзена идет между эфирами карбоновых кислот, имеющими a-водородные атомы в среде спирта в присутствии алкоголятов:
Реакция идет аналогично альдольной конденсации, но после присоединения нуклеофила к атому углерода С=О группы ацильная группа отщепляет уходящую группу. При конструировании гетероциклов необходимо также помнить, что 5- и 6-членные циклы очень устойчивы, и молекулы, стремясь перейти в более устойчивое соединение, часто самопроизвольно образуют циклическую форму. При этом протекают такие реакции, которые обычно возможны только в очень жестких условиях. Например, образование циклического имида из амида дикарбоновой кислоты (сукцинимид, фталимид, сахарин и др.)
В синтезе гетероциклических соединений по схеме «А» могут использоваться самые различные субстраты от алканов до карбоновых кислот, но чаще всего применяют дикарбонильные соединения. 1. Циклизация 1,4-дикарбонильных соединений ( Синтезы Пааля-Кнорра ) является общим методом синтеза фурана, пиррола (в присутствии аммиака) и тиофена (в присутствии соединений серы):
Выходы целевых продуктов высокие (80-90%), за исключением тиофена. Считают, что P2S5 и P2S3 восстанавливают карбонильные соединения, поэтому выход составляет 40-50%. - 1.1. Синтезы производных фурана из слизевой кислоты, пентоз и пентозанов являются разновидностью циклизации 1,4-дикарбонильных соединений, которые образуются по ходу реакции.
Фурфурол используется в промышленности как растворитель и как сырье для синтеза различных веществ, в том числе и лекарственных, например, фурацилин. Пентозаны (полисахариды, состоящие из пентоз) составляют существенную часть соломы.
Фурацилин (семикарбазон 5-нитро-2-фуранкарбальдегида или a-нитрофурфурола) - представитель группы бактерицидных препаратов, производных a-нитрофурана. - 1.2. Синтезы пиррола и его производных из 1,4-бутиндиола и бутандиовых кислот так же разновидность циклизации 1,4-дикарбонильных соединений, которые образуются по ходу реакции:
- 1.3. В синтезах производных тиофена вместо 1,4-дикарбонильных соединений, которые восстанавливаются сульфидами, лучше использовать алканы, алкены, производные 1,3-бутадиина. Нуклеофильное присоединение по активированным p-связям приводит к образованию 1,4-тиокарбонильного соединения:
2. Взаимное превращение пятичленных гетероциклов с одним гетероатомом (реакция Юрьева) также можно отнести к схеме А, т.к. при этом образуются две новые связи С - Х:
3. Пирролидиновый цикл, который широко применяется в синтезах лекарств (например, пиромекаина, гигрония и др.), можно получить алкилированиемпервичного амина соответствующим дигалогенидом:
4. Синтез индола внутримолекулярной конденсацией о-аминофенилуксусного альдегида включает образование С-Х связи.
5. Циклизация a-ациламинокарбонильных соединений – разновидность общего способа получения пятичленных циклов из 1,4-дикарбонильных соединений – применяется для синтеза производных оксазола, тиазола и имидазола. Таким образом синтезируют оксазол в производстве витамина В6:
6. Синтез производных пиридина из 1,5-дикарбонильных соединений:
Образующийся дигидропиридин легко дегидрируется (окисляется) до пиридина. Если взять непредельное 1,5-дикарбонильное соединение, то сразу образуется пиридин. 1,5-Дикарбонильных соединений доступны (легко синтезируются), поэтому данный метод получения производных пиридина широко используется. Чтобы аммиак не инициировал альдольную конденсацию, его лучше заменить гидроксиламином. При этом отпадает необходимость в окислении продуктов реакции. 7. Синтез пиридина из пентаметилендиамина (кадаверина) можно отнести к схеме А:
Реакция использовалась для доказательства структуры пиридина. 8. Синтез производных фентиазина, которые относятся к нейролептикам и используются для лечения различных психических заболеваний, осуществляют циклизацией 3-замещенных дифениламинов сплавлением их с серой. В результате образуются две С – Х связи:
Циклизацию ведут при 170-180оС в присутствии каталитических количеств иода до прекращения выделения сероводорода. Считают, что механизм реакции SE, что при температурах выше 160оС циклическая молекула (ромбической или моноклинной) серы S8 раскрывается и образует двухвалентные радикалы общего строения . S(х) . (х = 1…8), которые с иодом - кислотой Льюиса - образуют устойчивые комплексы с высокой электрофильностью:
Целевой продукт извлекают экстракцией кипящим хлорбензолом с последующей очисткой углем и кристаллизацией. Выделяющийся сероводород улавливают в специальных ловушках растворами едкого натра или окислителей (гипохлориты кальция, натрия). Выход с оборотом маточников достигает 80%.
|
|||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 551; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.135.224 (0.006 с.) |