
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кислородсодержащие соединения серы
Оксид серы (IV) SO2. В молекуле SO2 центральный атом серы находится в состоянии sp 2-гибридизации, форма расположения гибридных орбиталей атома серы – правильный треугольник, форма молекулы – угловая. Валентный угол составляет около 119,5°. На атоме серы имеется неподеленная электронная пара (рис. 2.7).
Физические свойства. При обычных условиях оксид серы (IV) или сернистый газ – бесцветный газ с резким удушливым запахом, температура плавления равна ‒75°С, температура кипения равна ‒10°С. SO2 хорошо растворим в воде: при 20°С в 1 объеме воды растворяется 40 объемов сернистого газа. Получение SO2. В промышленности: S + O2 = SO2; 4FeS2 + 11O2 = 2Fe2O3 + 8SO2. В лаборатории: BaSO3 + H2SO4(конц) = BaSO4↓ + SO2↑ + H2O; 2H2SO4(конц) + Cu = SO2↑ + CuSO4 + 2H2O. Химические свойства SO2
Наличие неподеленной электронной пары у атома серы придает молекуле SO2 способность к реакциям присоединения. На прямом солнечном свету SO2 соединяется с хлором, образуя S(Cl2)O2 – диоксид-дихлорид серы (сульфурилхлорид): SO2 + С12 = S(Cl2)O2. S(Cl2)O2 – бесцветная жидкость с резким запахом, является хлорангидридом серной кислоты, легко гидролизуется: S(Cl2)O2 + 2H2O = H2SO4 + 2НС1. Оксиду SO2 соответствует кислота H2SO3. Сернистая кислота H 2 SO 3 не получена в свободном состоянии. Сернистой кислотой называют раствор SO2 в воде. При растворении устанавливаются равновесия: SO2 + H2O ⇄ H2SO3 H2SO3 ⇄ H+ + HSO HSO H2SO3 – двухосновная слабая кислота, разлагающаяся в момент получения: Na2SO3 + 2HCl = 2NaCl + SO2↑ + H2O. При записи уравнений с участием сернистой кислоты ее формулу (H2SO3) представляют в виде SO2 + H2O. H2SO3 образует средние соли (сульфиты) и кислые соли (гидросульфиты): SO2 + 2KOH = K2SO3 + H2O; SO2 + KOH(нед) = KНSO3. При нагревании сульфиты диспропорционируют: 4Na2SO3 = 3Na2SO4 + Na2S. Сернистая кислота и ее соли обладают окислительно-восстановительной двойственностью. Восстановительные свойства для производных серы в степени окисления +4 (диоксид, сернистая кислота и ее соли) более характерны, чем окислительные свойства. Практически мгновенно протекает окисление сульфитов и гидросульфитов многими окислителями (KМnО4, С12, Вr2 и др.):
5Na2SО3 + 2KМnО4 + 3Н2SО4 = 5Na2SО4 + 2МnSО4 + K2SО4 + 3H2O; Na2SО3 + С12 + H2O = Na2SО4 + 2НС1; H2SO3 + 4Н+ + 4 e – = S + 2H2O, Е SO Сульфиты настолько сильные восстановители, что даже в твердом виде они постепенно окисляются кислородом воздуха: 2Na2SО3 + О2 = 2Na2SО4. Сульфиты легко присоединяют не только кислород, но и серу: K2SO3 + S = K2S2O3 (тиосульфат калия)
Растворимые сульфиты подвергаются гидролизу: SO K2SO3 + HOH ⇄ KHSO3 + KOH. SO 2 является одним из основных источников загрязнения атмосферы. При сжигании угля, содержащего небольшие количества соединений серы, в атмосферу выбрасывается диоксид серы. Растворяясь во влаге, находящейся на листьях или в воздухе, SO2 образует раствор сернистой кислоты, который затем окисляется до серной кислоты. Атмосферная влага с растворенными SO2 и H2SO4 выпадает в виде кислотных дождей, приводящих к гибели растительности. В пищевой промышленности SO2 используют для обеззараживания и снижения щелочности. В процессах консервирования пюре, соков, плодов он играет роль антисептика, консерванта и антиокислителя. После удаления SO2 (десульфитизация) остаточное содержание диоксида серы в продуктах не должно превышать 0,01%. Оксид серы (VI) SO3 является ангидридом H2SO4. При стандартных условиях SO3 – бесцветная жидкость, затвердевающая при t < 16ºС, при t > 42ºС переходит в газовую фазу. Молекула SO3 имеет sp 2 гибридизацию атомных орбиталей серы, форму плоского треугольника, угол между связями равен 120º:
В зависимости от температуры SO3 имеет различную структуру. В виде молекул SO3 существует только в газовой фазе, в жидком состоянии полимеризуется в циклический тример (SO3)3. В кристаллическом состоянии образуются зигзагообразные полимерные цепи (SO3) n. Атомные орбитали серы в полимерных соединениях находятся в состоянии sp 3 – гибридизации, связи направлены к вершинам тетраэдра:
Способность молекул SО3 объединяться в кольца или полимеры связана с координационной ненасыщенностью в ней атома серы, который может за счет sp 3- и sp 3 d 2-гибридизации орбиталей образовывать по четыре и по шесть σ-связей. Поэтому молекулы SО3 склонны к реакциям присоединения:
SО3 + НС1 = Н[SО3С1] (сильная хлорсульфоновая кислота). SO3 – типичный кислотный оксид, бурно реагирует с водой. На воздухе SО3 дымит, взаимодействуя с парами воды с образованием мельчайших капелек серной кислоты: SO3 + H2O → H2SO4. Проявляя кислотные свойства, SО3 реагирует с основными оксидами, со щелочами: SO3 + CaO = CaSO4; SO3 + Ba(OH)2 = BaSO4↓ + H2O; SO3 + NaOH(разб) = NaHSO4 SO3 + 2NaOH(конц) = Na2SO4 + H2O. SO3 термически нестоек, при t > 700ºС разлагается: 2SO3 Степень окисления серы S+6 – высшая, поэтому SO3 является сильнейшим окислителем: 5SO3 + 2P = P2O5 + 5SO2↑; 3SO3 + H2S = 4SO2↑ + H2O. В промышленности SO3 получают окислением SO2 в присутствии катализатора (Pt или V2O5): 2SO2 + O2 Серная кислота H2SO4. Физические свойства. Бесцветная маслообразная жидкость, очень гигроскопичная, неограниченно смешивается c водой, процесс растворения сильно экзотермичен, при нагревании выше 296ºС начинает разлагаться на SO3 и Н2О. Синтез в промышленности 1. Получение SO2: S + O2 = SO2; 4FeS2 + 11O2 = 2Fe2O3 + 8SO2. 2. В промышленности применяют два метода получения серной кислоты, различающиеся стадией окисления SO2. В контактном методе окисление SO2 в SO3 проводят при температуре 400 – 450ºС на катализаторе V2O5: 2SO2 + O2 Необходимость использования катализатора в этой обратимой реакции обусловлена тем, что сместить равновесие в сторону образования SO3 можно, в соответствии с принципом Ле Шателье, только при понижении температуры (реакция экзотермическая). Однако при низких температурах сильно падает скорость протекания реакции. Поскольку для оптимального сдвига равновесия вправо требуется низкая температура, а для достижения удовлетворительной скорости – высокая температура, на практике процесс проводят при температуре 400 – 450ºС. В нитрозном методе получения серной кислоты SO2 окисляют оксидом азота (IV): SO2 + NO2 = SO3 + NO↑; 2NO + O2 = 2NO2. 3. Поглощение SO3 концентрированной серной кислотой: n SO3 + H2SO4 = H2SO4 · n SO3 (олеум) (n = 1‒3). Поглощение SO3 водой на практике сильно затруднено, так как SО3 начинает энергично поглощать воду, образуя воздушно-капельную взвесь («туман»). Безводная серная кислота хорошо растворяет SO3 и реагирует с ним, образуя тяжелую маслообразную жидкость – олеум (H2SO4 · · n SO3), представляющую собой смесь полисерных кислот. Для получения концентрированной серной кислоты олеум смешивают с серной кислотой, содержащей некоторое количество воды: H2SO4 · n SO3 + n H2O = (n + 1)H2SO4. Разбавленная H2SO4 является сильной кислотой, проявляет характерные для кислот химические свойства: H2SO4(разб) = 2H+ + SО Fe + H2SO4 = FeSO4 + Н2; CuO + H2SO4 = CuSO4 + Н2O; Ca(OH)2 + H2SO4 = CaSO4 + 2Н2O; CaCO3 + H2SO4 = CaSO4 + Н2O + CO2; NH3 + H2SO4 = NH4HSO4. Серная концентрированная кислота H2SO4(конц) является кислотой-окислителем. H2SO4(конц) реагирует с металлами, расположенными в электрохимическом ряду напряжений после водорода (Сu, Ag, Hg), с неметаллами. H2SO4(конц) не взаимодействует с Au, Pt, Os, Ir. Некоторые металлы (Al, Cr, Fe) в H2SO4(конц) пассивируются на холоду. Продуктами восстановления H2SO4(конц) могут быть S+4O2, S0, H2S–2. При увеличении активности восстановителя образуется продукт с более низкой степенью окисления серы:
2H2SO4(конц) + 2Ag = SO2↑ + Ag2SO4↓ + 2H2O; 5H2SO4(конц) + 4Mg = H2S↑ +4MgSO4↓ + 4H2O; 2H2SO4(конц) + C(графит) = 2SO2↑ +СO2↑ + 2H2O; H2SO4(конц) + H2S = SO2↑ + S↓ +2H2O; H2SO4(конц) + KCl = KHSO4 + HCl. При приготовлении водных растворов серной кислоты происходит сильное разогревание смеси, которое может сопровождаться ее разбрызгиванием. Выделение большого количества теплоты является следствием образования водородных связей между H2SO4 и H2O. Правило разбавления концентрированной серной кислоты: при непрерывном перемешивании раствора кислоту вливают в воду. Способность серной кислоты образовывать гидраты H2SO4 · n H2O позволяет использовать ее как сильный водоотнимающий агент. Серная кислота применяется также в производстве сульфатов и других соединений серы, минеральных удобрений, красителей и лекарственных препаратов. Соли серной кислоты. Серная кислота образует большое число как средних, так и кислых солей. Большинство солей хорошо растворимы в воде. Малоратворимыми являются сульфаты щелочноземельных металлов, серебра, свинца, многие сульфаты кристаллизуются из растворов в виде кристаллогидратов: CuSО4 · 5H2O – медный купорос, FeSО4 · 7H2O – железный купорос, Na2SО4 · 10H2O – глауберова соль, MgSО4 · 7H2O – горькая (английская) соль, CaSО4 · 2H2O – гипс. Для серной кислоты характерно образование двойных солей, называемых квасцами, например, хромовокалиевые квасцы KСr(SО4)2 · 12Н2О; алюмокалиевые квасцы KА1(SО4)2 · 12Н2О. Из всех сульфатов наименьшей растворимостью обладает сульфат бария. Поэтому образование Ва S О4 в виде белого осадка используют как качественную реакцию на сульфат-ион: Ва2+ + SO H2SO4 + BaCl2 = BaSO4↓ + 2HCl. Выпадает белый осадок, не реагирующий с HCl и HNO3. При прокаливании твердые сульфаты ведут себя по-разному. Сульфаты щелочных металлов плавятся без разложения. Сульфаты металлов средней активности образуют соответствующие оксиды: ZnSО4 Сульфат железа (II) разлагается по механизму внутримолекулярного окисления-восстановления: 4FeSО4 Сульфаты наиболее тяжелых металлов разлагаются до металла: Ag2SО4 Большинство оксокислот серы(VI) генетически удобно рассматривать как результат замещения кислорода или гидроксидной группы в молекуле серной кислоты на изоэлектронные частицы. При замещении в H2SO4 концевого атома кислорода на атом серы образуется тиосерная кислота H2S2O3. В свою очередь, замещение мостикового атома кислорода в дисерной кислоте на один или цепочку атомов серы возникает ряд политионовых кислот, а на пероксидную группу –О–О– – пероксодисерная кислота. Гидроксидная группа –ОН в H2SO4 может заместиться на гидропероксогруппу
Тиосоединения. Как отмечено выше, при замене в сульфат-ионе одного атома кислорода на атом серы образуются тиосульфат-ионы S2
В лаборатории тиосульфаты получают при кипячении раствора сульфита с порошком серы: Na2S+4O3 + S0 Тиосерная кислота неустойчива из-за протекания внутримолекулярного окислительно-восстановительного процесса. Поэтому при подкислении тиосульфатов они начинают выделять свободную серу и SO2.: Na2S2O3 + 2HCl = 2NaCl + SO2↑ + S↓ +H2O. Наличие в тиосульфатах S-2 придаёт им восстановительные свойства. Тиосульфат натрия используется для связывания хлора: Na2S2O3+ С12(нед) + Н2О = Na2SО4 + S + 2НС1; Na2S2O3 + 4С12(изб) + 5Н2О = Na2SО4 + Н2SО4 + 8НС1. Na2S2O3 используется в медицине как противотоксическое средство при отравлениях соединениями ртути, свинца, синильной кислотой и ее солями, при этом образуются плохо растворимые нетоксичные сульфиты или менее ядовитые тиоцианаты: S2 Pb2+ + S S + СN– = NСS–. Na2S2O3∙5H2O (тривиальное название – гипосульфит) используют для растворения малорастворимых солей, например бромида серебра: 2Na2S2O3 + AgBr = NaBr + Na3[Ag(S2O3)2]. Важным свойством тиосульфата натрия является его способность образовывать с иодом бесцветный тетратионат нария: I2 + 2Na2S2O3 = 2NaI + Na2S4O6 (тетратионат натрия);
Эта реакция широко используется в аналитической химии. Na2S4O6 – соль тетратионовой кислоты. Политионовые кислоты – это кислоты состава: Н2S n О6 или Н2(О3S–S n ‒ 2–SО3), где n = 2–22. В состав политионовых кислот входят зигзагообразные цепи атомов серы. Название кислоты и ее солей определяется числом атомов серы, входящих в состав кислоты или соли: Na2S6O6 – гексатионат; Na2S5O6 – пентатионат; Na2S4O6 – тетратионат; Na2S2O6 – дитионат. Политионовые кислоты существуют только в водных растворах и медленно разлагаются при хранении: Н2S n О6 = Н2SО4 + SО2 + (n ‒ 2)S. Соли политионовых кислот щелочных металлов хорошо растворимы в воде. В сухом состоянии довольно устойчивы, при нагревании они разлагаются: Na2S6O6 Полисерные кислоты Н2SО4 · n SО3 (n = 1 ÷ 3) существуют в свободном виде. Тяжелые маслянистые жидкости, носят название «олеум»:
H 2 S Пероксосерные кислоты характеризуются наличием в структуре пероксидной группы (–О–О–). H2SO5 – пероксомоносерная (мононадсерная кислота, кислота Каро), H2S2O8 – пероксодисерная кислота (двунадсерная кислота):

Обе кислоты – бесцветные кристаллические вещества, плавящиеся при нагревании с разложением при температуре 47°С (H2SO5) и 65°С (H2S2O8):
2H2SO5 = 2H2SO4 + О2. Водород, связанный с пероксогруппой в H2SO5, на металл не замещается, кислота является одноосновной. Для H2SO5 известны соли, например КНSО5 (пероксомоносульфат или кароат калия). Пероксосерные кислоты подвергаются необратимому гидролизу с выделением пероксида водорода. Гидролиз пероксодисерной кислоты протекает в две стадии: H2S2O8 + H2O = H2SO5 + Н2SО4; H2SO5 + Н2О ⇄ Н2SО4 + Н2О2. Наличие пероксидной группировки у этих двух кислот обусловливает их окислительные свойства. Пероксодисульфат аммония (NH4)2S2O8 способен окислить Mn2+ до MnO 5(NH4)2S2O8 + 2MnSO4 + 8Н2О = 5(NH4)2SO4 + 2HMnO4 + 7H2SO4; 3(NH4)2S2O8 + Сr2(SO4)3 + 7Н2О = 3(NH4)2SO4 + H2Сr2О7 + 6H2SO4. Стандартный электродный потенциал системы: S2O имеет очень высокое значение, поэтому окислительную функцию по отношению к сульфат-ионам может выполнять только электрический ток. H 2 S 2 O 8 получают электролизом холодной концентрированнойсерной кислоты: 2Н2SО4(конц) H2S2O8 можно получить действием H2SO4(конц) на пероксодисульфаты: K2S2O8 + H2SO4(конц) = H2S2O8 + K2SO4. H 2 SO 5 получают действием 100-процентного H2O2 на H2S2O8 или H2SO4: H2SO4 + H2O2 = H2SO5 + H2O; H2S2O8 + H2O2 = 2H2SO5. При замещении гидроксидной группы серной кислоты на изоэлектронные группы (F–, Cl–) образуются соответственно фтор- (F(OH)SO2)и хлорсульфоновая (Cl(OH)SO2) кислоты. Практически их синтезируют взаимодействием галогеноводородных кислот HF (HCl) с жидким SO3: HF + SO3 = HSO3F. Введение фтора из-за усиления поляризации связи О–Н приводит к повышению силы фторсульфоновой кислоты. Элементы подгруппы селена В структуре твердого и жидкого селена содержатся цепи и циклы Se8. В отличие от серы селен не имеет температурной области, в которой его расплав состоял бы только из циклических молекул. При нагревании до 620ºС степень полимеризации и вязкость возрастают, а в интервале 620–920ºС ‒ уменьшаются. В теллуре, в соответствии с увеличением доли металлической связи по сравнению с серой и селеном, циклические структуры не присутствуют. В пару над селеном и теллуром присутствуют молекулы Se n (2 ≤ n ≥ 9) и Те n (2 ≤ n ≥ 7). В ряду элементов VI группы главной подгруппы O – S – Se – Te – Po радиус атомов увеличивается, энергия ионизации уменьшается, неметаллические свойства элементов убывают, а их металлические свойства растут. В реакциях с азотной кислотой сера и селен ведут себя как неметаллы, а полоний – как металл: S + 2HNO3 = H2SO4 + 2NO; Se + 2HNO3 = H2SeO4 + 2NO; Po + 8HNO3 = Po(NO3)4 + 4NO2 + 4Н2О. По химическим свойствам Se и Te очень сходны с серой. Горят на воздухе с образованием диоксидов: Se + О2 = SeО2; Тe + О2 = ТeО2. SeО2 и ТeО2 – твердые вещества в отличие от SО2. С водородом при повышенных температурах частично взаимодействует лишь селен, теллур непосредственно с водородом не соединяется: Н2 + Se = Н2Se. Сера и селен с водой и разбавленными кислотами не взаимодействуют. Теллур взаимодействует с водой даже при обычных условиях, а полоний взаимодействует с соляной кислотой: Те + 2Н2О = ТеО2 + 2Н2↑; Ро + 2НС1 = РоС12 + Н2↑. В кипящих водных растворах щелочей селен и теллур, подобно сере, медленно растворяются (диспропорционируют): 3Se + 6KОН = 2K2Se + K2SeО3 + 3Н2О. С усилением металлических признаков склонность элементов данной подгруппы к проявлению отрицательных степеней окисления уменьшается. Поэтому Н2Se и Н2Тe менее устойчивы, чем Н2S, и проявляют более сильные восстановительные свойства. Селеноводород и теллуроводород прямым взаимодействием не получают. Они могут быть получены действием разбавленных кислот на селениды и теллуриды металлов: 2Na + Se = Na2Se (селенид натрия); Na2Se + 2HCl = H2Se + 2NaCl. H2Se и H2Тe при нормальных условиях – бесцветные газы с неприятным запахом. Селеноводород более ядовит, а теллуроводород менее ядовит, чем сероводород. Растворимость в воде H2Se и H2Тe примерно такая же, как и H2S. Водные растворы этих соединений проявляют кислотные свойства.
|
|||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 673; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.59.187 (0.1 с.) |



 2SO3;
SO2 + Br2 + 2H2O = H2SO4 + 2HBr;
SO2 + 2HNO3(конц) = H2SO4 + 2NO2↑
2SO3;
SO2 + Br2 + 2H2O = H2SO4 + 2HBr;
SO2 + 2HNO3(конц) = H2SO4 + 2NO2↑
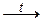 CaSO3
CaSO3
 ,
, 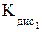 = 2 ∙ 10-2;
= 2 ∙ 10-2; ,
, 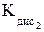 = 6 ∙ 10-8.
= 6 ∙ 10-8. = 0,45 В;
= 0,45 В;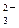 + 2ОН– – 2 e – = SО42‑ + H2O, Е
+ 2ОН– – 2 e – = SО42‑ + H2O, Е 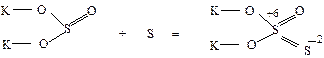
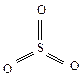


 2SO2 + O2.
2SO2 + O2. 2SO3.
2SO3. ;
;
 H2SO4( конц )
H2SO4( конц )
 = ВаSО4↓;
= ВаSО4↓; ZnО + SО3↑.
ZnО + SО3↑. :
:


 O 7 – дисерная (Н2SО4 · SО3); H 2 S
O 7 – дисерная (Н2SО4 · SО3); H 2 S 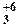 O 10 – трисерная
O 10 – трисерная , а Сr3+ до Сr2О
, а Сr3+ до Сr2О 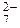 :
: + 2 e – = 2SO
+ 2 e – = 2SO 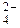 , Е
, Е  H2S2O8 + H2.
H2S2O8 + H2.


