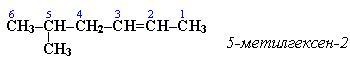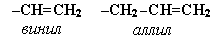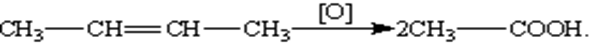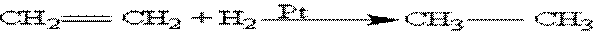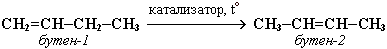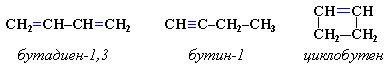Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: Алкены (этиленовые углеводороды, непредельные, олефины)
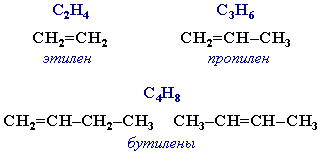
Общая формула гомологического ряда алкенов CnH2n. В отличие от предельных углеводородов, алкены содержат двойную связь С=С. В образовании такой связи участвуют атомы углерода в sp2-гибридизованном состоянии С=С: σ-связь и π-связь. Простейшие представители:
σ-Связи, образуемые sp2-гибридными орбиталями, находятся в одной плоскости под углом 120°. Поэтому молекула этилена имеет плоское строение:
По своей природе π-связь резко отличается от σ-связи: π-связь менее прочная вследствие меньшей эффективности перекрывания р-орбиталей. Номенклатура алкенов По международной номенклатуре ИЮПАК названия алкенов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ен: 2 атома С → эт ан → эт ен;
Главная цепь углеродных атомов выбирается таким образом, чтобы она обязательно включала в себя двойную связь (т.е. она может быть не самой длинной). Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение двойной связи, ставится обычно после суффикса –ен. Например:
Для простейших алкенов применяются также исторически сложившиеся названия: этилен (этен), пропилен (пропен), бутилен (бутен-1), изобутилен (2-метилпропен) и т.п. В номенклатуре различных классов органических соединений наиболее часто используются следующие одновалентные радикалы алкенов:
Изомерия алкенов Структурная изомерия алкенов 1. Изомерия углеродного скелета (начиная с С4Н8):
2. Изомерия положения двойной связи (начиная с С4Н8):
3. Межклассовая изомерия с циклоалканами, начиная с С3Н6:
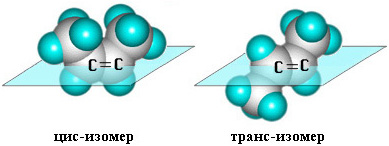
Пространственная изомерия алкенов Цис -транс-изомерия обусловлена наличием в молекуле двойной связи, когда у каждого из двух атомов углерода при двойной связи различные заместители, могут существовать в виде двух пространственных изомеров, отличающихся расположением заместителей относительно плоскости π-связи Вращение атомов вокруг двойной связи невозможно без ее разрыва. Это обусловлено особенностями строения π-связи (π-электронное облако сосредоточено над и под плоскостью молекулы). Вследствие жесткой закрепленности атомов поворотная изомерия относительно двойной связи не проявляется.
Так, в молекуле бутена-2 СН3–СН=СН–СН3 группы -СН3 могут находиться либо по одну сторону от двойной связи – это цис-изомер; либо по разные стороны – это транс -изомер:
Цис-транс -изомерия не проявляется, если хотя бы один из атомов С при двойной связи имеет 2 одинаковых заместителя. Физические свойства алкенов По физическим свойствам алкены мало отличаются от алканов с тем же числом атомов углерода в молекуле. Низшие гомологиС2—С4 при нормальных условиях — газы,С5—С17 — жидкости, высшие гомологи — твердые вещества. Алкены нерастворимы в воде, хорошо растворимы в органических растворителях.
Способы получения алкенов
1) Крекинг алканов. Крекинг алканов является важнейшим промышленным способом получения алкенов из высококипящих фракций нефти. Под действием сильного нагревания (до 700 °С) в молекулах алканов гомолитически расщепляются s-связи С—С, при этом образуется смесь низкомолекулярных алканов и алкенов:
2) Реакции элиминирования. Эта группа реакций лежит в основе большинства способов получения алкенов. 3) Дегидрогалогенирование происходит при действии спиртовых растворов щелочей на моногалогениды, согласно правила Зайцева.
4) Дегидратация спиртов (происходит при нагревании спиртов с серной кислотой) 5) Дегалогенирование (происходит при нагревании дигалогенидов, имеющих атомы галогена у соседних атомов углерода, с двухвалентными металлами) 6) Дегидрирование алканов ( проводят при 500 °С в присутствии катализатора)
Химические свойства алкенов Определяются наличием в их молекулах двойной связи. Электронное облако π -связи подвергается атаке электрофильными агентами. Поэтому многие реакции алкенов протекают по механизму электрофильного присоединения. 1) Гидрогалогенирование. При взаимодействии алкенов с галогеноводородами (НСl, НВr) образуются галогеналканы, причем если исходный алкен несимметричен, то реакция протекает по правилу Марковникова.
2) Гидратация.
При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Присоединение воды идет по правилу Марковникова. 3) Галогенирование. При добавлении к алкену брома (в виде бромной воды) бурая окраска брома быстро исчезает. Эта реакция является качественной на двойную связь: 4) Окисление. · При окислении алкенов перманганатом калия КMnO4 в нейтральной или щелочной среде окрашенный раствор перманганата калия быстро обесцвечивается (буреет). Эта реакция также является качественной на двойную связь (р. Вагнера).
· При окислении перманганатом калия в кислой среде или хромовой смесью происходит полный разрыв двойной связи с образованием карбоновых кислот. 5) Восстановление (гидрирование). Эта реакция протекает в присутствии катализатора — мелко раздробленного никеля, платины или палладия — при комнатной температуре:
6) Реакции полимеризации. 7) Изомеризация алкенов Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al2O3). Изомеризация алкенов приводит или к перемещению π–связи:
или к перестройке углеродного скелета:
Применение алкенов Этилен применяется для получения этилового спирта, полиэтилена, политетрафторэтилена (тефлона), уксусного альдегида, галогенопроизводных и многих других органических соединений. Он ускоряет созревание плодов (помидоров, цитрусовых и др.) при введении небольших количеств его в воздух теплиц. Этилен и его гомологи используются как химическое сырье для синтеза полимерных материалов (пластмасс, каучуков, пленок) и других органических веществ. Тема 2.4 Алкадиены (диены) Алкадиены – класс непредельных алифатических углеводородов, содержащих две двойные связи в молекуле. Общая формула гомологического ряда алкадиенов СnН2n-2.
Номенклатура алкадиенов По правилам международной номенклатуры ИЮПАК главная цепь молекулы алкадиена должна включать обе двойные связи. Нумерация атомов углерода в цепи проводится так, чтобы двойные связи получили наименьшие номера. Названия алкадиенов производят от названий соответствующих алканов (с тем же числом атомов углерода), в которых последняя буква «н» заменяется на суффикс –диен. Заместители в цепи указывают в начале названия, а местоположение двойных связей – в конце. Классификация алкадиенов: 1. Диены с кумулированными двойными связями - две двойные связи расположены у одного атома углерода; (неустойчивы). СН2 = С = СН2 (аллен)
2. Диены с изолированными двойными связями – двойные связи разделены двумя и более одинарными связями; (свойства как у алкенов).
СН2=СН–СН2–СН=СН2
3. Диены с сопряженными двойными связями - две двойные связи разделены одной одинарной; (особые свойства).
СН2= СН—СН = СН2.
Эти соединения широко используются в производстве для получения синтетических каучуков и других органических веществ. Изомерия сопряженных диенов
Структурная изомерия 1. Изомерия положения сопряженных двойных связей:
2. Изомерия углеродного скелета:
3. Межклассовая изомерия с алкинами и циклоалкенами. Например, формуле С4Н6 соответствуют следующие соединения:
Пространственная изомерия Диены, имеющие различные заместители при углеродных атомах у двойных связей, подобно алкенам, проявляют цис - транс -изомерию.
|
|||||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 71; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.0.25 (0.02 с.) |