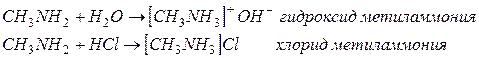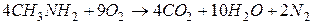Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: азотсодержащие органические соединения. ⇐ ПредыдущаяСтр 6 из 6
АМИНЫ• Аминами называет органические производные аммиака, в котором один, два или все три атома водорода замещены на углеводородный радикал. Классификация и номенклатура аминов.
Физические свойства аминов. Метиламин, диметиламин, триметиламин и этиламин - газообразные вещества. Следующие представители гомологического ряда - жидкости, а высшие амины - твердые вещества. Газообразные и жидкие амины обладают запахом, напоминающим запах аммиака. Химические свойства аминов. 1. Основные свойства аминов.
2. Горение.
Получение аминов. 1. Восстановление нитросоединений. C2H5NO2 + 3H2 → C2H5NH2 + 2H2O 2. Взаимодействие галогенпроизводных с аммиаком. Применение аминов. Амины широко применяются в органическом синтезе. Они служат промежуточными продуктами синтеза лекарственных средств, синтетических волокон, пластмасс, стимуляторов роста растений. АНИЛИН. Строение молекулы.
Физические свойства. Маслянистая жидкость, бесцветная, но быстро темнеющая на воздухе, в воде малорастворим, ядовит. Химические свойства. 1. Основные свойства. C6H5NH2 + H2O → [C6H5NH3]OH гидроксид фениламмония
C6H5NH2 + HCl → [C6H5NH3]Cl хлорид фениламмония 2. Реакция замещения.
3. Горение. 4C6H5NH2 + 31О2 → 24СО2 + 14H2O + 2N2 Получение анилина. 1. Реакция Зинина.
2. Реакция Зайцева.
Анилин используется для получения лекарств, красителей, взрывчатых веществ.
ТЕМА: АМИНОКИСЛОТЫ. Аминокислотами называют органические соединения, а молекулах которых содержатся карбоксильная группа (– СООH) и аминогруппа (– NH2) Строение и номенклатура аминокислот.
Физические свойства. Аминокислоты представляет собой белые, кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом. Химические свойства. 1. Амфотерные свойства аминокислот. NH2 – CH2 – COOH + NaOH → NH2 – CH2 – COONa + H2O NH2 – CH2 – COOH + HCl → [NH2 – CH2 – COOH]+Cl- 1. Образование сложных эфиров. NH2 – CH2 – COOH + C2H5OH → NH2 – CH2 – CO – O – C2H5 + H2O 2. Реакция конденсации
Получение аминокислот. 1. Взаимодействие галогенпроизводных карбоновых кислот с аммиаком. Cl – CH2 – COOH + NH3 → NH2 – CH2 – COOH + HCl 2. Гидролиз белков. Применение аминокислот.
Аминокислоты и их производные используют в качестве лекарств. Синтетические аминокислоты - сырье для производства полиамидных синтетических волокон и изделий из этих полимеров. БЕЛКИ. Белками называют природные полимеры, состоящие из большого числа остатков α-аминокислот, связанных между собой пептидными связями. Строение белка. Первичная структура - это последовательность аминокислот в полипептидной цепи. Вторичная структура - образование опирали. Третичная структура - конфигурация, которую приобретает в пространстве свернутая в спираль молекула белка. Физические свойства белков. Молекулы фибриллярных белков вытянуты в длину, это основной строительный материал сухожилий, мускульных и покровных тканей. Такие белки в воде не растворимы. Глобулярные белки свернуты в клубочки. Глобулярные белки растворимы в воде либо в растворах кислот или оснований. Химические свойства белков. 1. Денатурация. При нагревании, под действием сильных кислот или оснований, солей тяжелых металлов происходит необратимое осаждение (свертывание) белков.
2. Гидролиз. Под действием ферментов, а также водных растворов кислот или щелочей происходит разрушение первичной структуры белка в результате гидролиза пептидных связей. Гидролиз приводит к образованию пептидов и аминокислот.
3. Качественные реакции белков. а) биуретовая реакция - при действии на белки раствора солей меди (2) в щелочной среде возникает фиолетовое окрашивание. б) ксантопротеиновая реакция - при действии на белки концентрированной азотной кислоты образуется желтая окраска.
|
|||||
|
Последнее изменение этой страницы: 2021-07-19; просмотров: 50; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.8.110 (0.006 с.) |