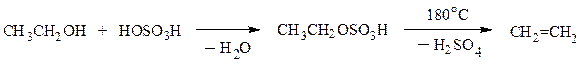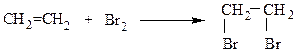Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 3.1.3 Получение и свойства этилена
Реактивы, материалы, приборы: этанол, серная кислота, концентрированная, натронная известь, раствор перманганата калия, бромная вода, пористая глина, хлоркальциевая трубка, изогнутая стеклянная трубка, спиртовка, пробирки, мерные пробирки.
В пробирку наливают 5 см3 смеси этанола и концентрированной серной кислоты, взятых в соотношении 1:2, для равномерного кипения бросают несколько кусочков пористой глины и через хлоркальциевую трубку, наполненную кусочками натронной извести (для связывания образующихся также CO2 и SO2), подсоединяют к стеклянной изогнутой трубке. Пробирку со смесью нагревают. Образующийся этилен пропускают в отдельные пробирки с раствором перманганата калия и бромной водой. Обесцвечивание растворов указывает на протекание следующих реакций:
По окончании опыта отставляют горелку и тотчас же разбирают прибор во избежание засасывания раствора щелочи в смесь этилового спирта с серной кислотой. Рассмотрите механизм электрофильного присоединения бромирования и окисления этилена при различных условиях:
Наблюдение:
Выводы:
Опыт 3.1.4 Свойства жидких ненасыщенных
Реактивы, материалы, приборы: бензин или керосин как источники непредельных углеводородов или скипидар, 5%-й раствор брома в CCl4, 2%-й раствор перманганата калия, серная кислота концентрированная, 10%-й раствор соды, индикаторная бумага, пробирки, капельницы.
Бромирование алкенов. В сухие пробирки наливают по 1 см3 алкенов и добавляют по каплям при встряхивании 5%-й раствор брома в CCl4. Если желтая окраска брома исчезает медленно, смесь осторожно подогревают. Цвет влажной индикаторной бумажки, поднесенной к пробирке, не изменяется. Напишите уравнение реакции бромирования 2-метилпентена-2 и рассмотрите ее механизм (АЕ).
Окисление алкенов водным раствором перманганата калия (реакция Вагнера). В пробирки наливают по 1 см3 алкенов, добавляют 1 см3 10%-го раствора соды, затем по каплям при встряхивании – 2%-й раствор перманганата калия. Фиолетовая окраска исчезает, появляется бурый осадок Напишите уравнение реакции окисления 2-метилпентена-2:
Реакции алкенов с концентрированной серной кислотой. В сухие пробирки наливают по 1 см3 алкенов, добавляют 1 см3 концентрированной серной кислоты и осторожно взбалтывают смесь в течение нескольких минут. Если смесь сильно разогревается, пробирку охлаждают водой. Слой алкена исчезает, смесь буреет. Напишите уравнение реакции образования алкилсульфата и рассмотрите ее механизм (АЕ) на примере бутена-1:
Наблюдение:
Выводы:
|
||||
|
Последнее изменение этой страницы: 2021-04-12; просмотров: 130; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.140.186.201 (0.004 с.) |