
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 2.2.2 Определение серы в органическом веществе
Реактивы, материалы, приборы: оксид свинца, 5 н раствор гидроксида натрия, шерстяное волокно, лопаточка, капельницы.
В пробирку добавляют одну четвертую часть лопаточки оксида свинца, кусочек шерстяного волокна, 5 капель 5 н раствора гидроксида натрия и смесь нагревают на пламени спиртовки. Наблюдают выпадение осадка сульфида свинца черного цвета, который свидетельствует о присутствии серы в исследуемом волокне.
Наблюдение:
Выводы:
Опыт 2.2.3 Определение азота и серы в тиомочевине
Реактивы, материалы, приборы: тиомочевина, натронная известь, вода, 0,5 н раствор уксуснокислого свинца, красная лакмусоваябумага, лопаточка, пробирки, спиртовки, капельницы.
В пробирку помещают четвертую часть лопаточки тиомочевины и половину лопаточки натронной извести, смесь перемешивают, встряхивая пробирку. Пробирку осторожно прокаливают в пламени горелки. Присутствие азота определяют по изменению цвета влажной лакмусовой бумаги. Затем пробирку охлаждают. В нее приливают 1 см3 воды, содержимое взбалтывают и раствор декантируют в другую пробирку. В жидкость добавляют 2 капли 0,5 н раствора ацетата свинца. Выпадает черный осадок сульфида свинца.
Na2S + (CH3COO)2 Pb ¾ ® 2 CH3COONa + PbS↓
Наблюдение:
Выводы:
Опыт 2.2.4 Открытие азота и серы в шерстяном волокне
Реактивы, материалы, приборы: шерсть, металлический натрий, вода, кристаллический сульфат железа (II), 1-й раствор хлорида железа (III), 10%-й раствор соляной кислоты, 1%-й раствор ацетата свинца, уксусная кислота, 2%-й раствор нитропруссида натрия, тиомочевина, натронная известь, лакмусовая бумага, пробирки, спиртовки, капельницы, фарфоровая чашка, воронка, бумажный фильтр, пипетки.
В сухую пробирку вносят небольшое количество исследуемого вещества (шерсть) и кусочек металлического натрия величиной с горошину (РАБОТАТЬ В ВЫТЯЖНОМ ШКАФУ С ЗАЩИТНЫМ ЭКРАНОМ!). Пробирку в пламени горелки нагревают до температуры красного каления и опускают в фарфоровую чашку с 4-5 см3 воды. Образующийся раствор отфильтровывают от угля и стекла и делят на четыре части. Обнаружение азота методом Лассеня. При сплавлении с натрием органическое вещество (кератин – белок шерсти) разлагается и содержащийся азот образует с углеродом и натрием цианид натрия, который обнаруживают переводом его в берлинскую лазурь.
Для этого к одной части фильтрата добавляют 2-3 кристаллика сульфата железа (II), нагревают до кипения, приливают 2-3 капли 1%-го раствора хлорида железа (III) и подкисляют соляной кислотой. При наличии в исследуемом веществе азота появляется синяя окраска берлинской лазури:
Na + [ С ] + [N] ® NaCN FeSO4 + NaOH ® Fe(OH)2 ¯ + Na2SO4 6 NaCN + Fe(OH)2 ¾ ® Na4[Fe(CN)6] + 2 NaOH Na4 [Fe(CN)6] + FeCl3 ¾ ® NaFe [Fe(CN)6] ¯ + 3 NaCl берлинская лазурь
Открытие серы. Врезультате восстановительной деструкции шерсти при сплавлении с металлическим натрием образуется сульфид натрия. Сульфид-анион открывают обычными качественными реакциями: 1. Ко второй пробирке фильтрата (см. выше) добавляют 0,5 см3 1%-го раствора ацетата свинца и подкисляют уксусной кислотой. Присутствие серы обнаруживается по образованию коричнево-черного осадка сульфида свинца:
Na2S + (CH3COO)2 Pb ¾ ® 2 CH3COONa + PbS ↓
2. К третьей пробирке (см. выше) приливают 0,5 см3 2%-го раствора нитропруссида натрия. Появляется интенсивное красно-фиолетовое окрашивание, переходящее постепенно в бурый цвет:
Na2S + Na2 [Fe(CN)5 (N О)] ¾ ® Na4[Fe(CN)5 (N О S)]
3. К четвертой пробирке по каплям прибавляют 10%-й раствор соляной кислоты; при этом появляется характерный запах сероводорода:
Na 2 S + 2 HCl ¾ ® H 2 S + 2 NaCl
Наблюдение:
Выводы:
Опыт 2.2.5 Открытие галогенов
В большинстве органических соединений галоген прочно связан с углеродом ковалентной связью, поэтому его нельзя обнаружить реакцией с нитратом серебра. Для обнаружения галогена органическое вещество либо восстанавливают водородом в момент выделения (натрий в спирте), тогда галоген превращается в анион, либо проводят опыт с получением зеленой окраски пламени.
Реактивы, материалы, приборы: хлороформ, тетрахлорид углерода, нитрат серебра, медная проволока, дистиллированная вода, лакмусовая бумага.
Реакция с нитратом серебра. Полоску фильтровальной бумаги смачивают исследуемым раствором вещества (хлороформом) и сжигают под мокрой химической воронкой. Продукты горения смывают дистиллированной водой в пробирку, добавляют раствор нитрата серебра. Образование осадка галогенида серебра указывает на присутствие галогена в исследуемом веществе.
2 CHCl3 + O2 + 2 H2O ¾ ® 2 CO2 + 6 HCl HCl + AgNO3 ¾ ® AgCl ↓+ HNO3
Проба Ф. Ф. Бейльштейна. Медную проволоку с петлей на конце прокаливают на горелке до исчезновения посторонней окраски пламени. Остывшую петлю, покрывшуюся черным налетом оксида меди (II), опускают в пробирку с каплей тетрахлорметана и вновь вносят в пламя горелки. Пламя окрашивается в зеленый цвет, что указывает на присутствие в органическом соединении галогена.
CCl 4 + 2 CuO ¾ ® 2 CuCl 2 + CO 2
Медь с галогеном образует соединение, пары которого и окрашивают пламя горелки в зеленый цвет.
Наблюдение:
Выводы:
УГЛЕВОДОРОДЫ
В составе органического вещества углерод находится в одном из трех валентных состояний – Sp3, Sp2 и Sp-гибридизация. В образовании простой, одинарной σ-связи со стороны атома углерода всегда участвует гибридная Sp3, Sp2 и Sp-орбиталь. Для нее характерно перекрывание электронных орбиталей вдоль линии связи, соединяющей центры взаимодействующих атомов. Такая связь прочная, дипольный момент ее незначительный. Кратные π-связи образованы не гибридными, а р-орбиталями за счет их перекрывания по обе стороны линии, соединяющей центры атомов. Электронная плотность π-связи удалена от ядер, перекрывание р-орбиталей меньше, поэтому они менее прочные, полярные и легкоразрывающиеся под внешним воздействием. Отсюда и различие в свойствах насыщенных углеводородов (алканы, циклоалканы) и ненасыщенных (алкены, алкины). Алканы устойчивы к различным реагентам, для них типичны гомолитические, радикальные реакции замещения – SR, идущие в присутствии таких активаторов, как свет, температура, пероксиды. Ненасыщенные углеводороды значительно более реакционноспособные, для них характерен гетеролиз π-связи, следствием чего являются реакции электрофильного присоединения АЕ, реакции окисления и полимеризации, а для алкинов – еще и реакции замещения «кислого» водорода у тройной связи на металл. В данном случае проявляются кислотные свойства ацетилена и моноалкилацетиленов, обусловленные большей электроноотрицательностью атома углерода в состоянии Sp-гибридизации, т.е. большей долей π-электронов, по сравнению с Sp2- и Sp3-гибридизацией, что вызывает сдвиг электронной плотности в молекуле:
Нδ+ →Сδ– ≡ Сδ– ← Нδ+ Электронная конфигурация ароматических углеводородов (арены) характеризуется копланарностью атомов цикла и наличием (4n + 2) π-электронов. π-Электронная плотность распределена по всей π-орбитальной системе над и под плоскостью цикла в виде двух тор, образуя как бы единую π-связь. Такая делокализация π-электронов обуславливает необычно низкую энергию невозбужденного состояния аренов, их повышенную термодинамическую стабильность. Несмотря на наличие π-связи, т.е. на ненасыщенный характер ядра аренов, реакции, идущие с разрывом π-связи (реакции присоединения, окисления), не являются для них типичными, хотя и могут происходить в определенных условиях. Характерными реакциями аренов являются реакции электрофильного замещения (SЕ) – галогенирования, нитрования, сульфирования, алкилирования, ацилирования и др. В этих реакциях бензольное ядро служит источником π-электронов, которые удерживаются ядрами углерода слабее и доступны для электрофильных реагентов. В производных бензола группа, связанная с кольцом, влияет на реакционную способность и определяет ориентацию заместителя. Электронодонорные заместители, проявляющие +Мэфф. или +Iэфф. (группы OH, OR, NH, NR2), активируют ядро, облегчая Iэфф, и направляют новый заместитель в орто- и пара-положения. Галогены, хотя и ориентируют благодаря своему +Мэфф. новый заместитель в орто- и пара-положения, но из-за –Iэфф. затрудняют процесс замещения. Электроноакцепторные заместители (NO2 SO3H COOH CN CCl3 и др.) дезактивируют бензольное ядро, затрудняют SЕ и направляют новый заместитель в мета-положение. Различие в действии ориентантов I и II рода является следствием их влияния на стабильность образующихся σ-комплексов.
АЦИКЛИЧЕСКИЕ УГЛЕВОДОРОДЫ
|
|||||||
|
Последнее изменение этой страницы: 2021-04-12; просмотров: 444; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.217.203.172 (0.017 с.) |
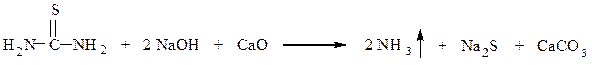
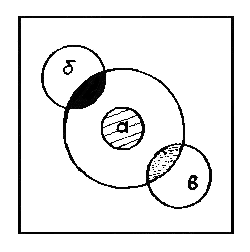 Микроколичества азота и серы в органических соединениях можно обнаружить по методу Рево. Для этого отфильтрованный раствор набирают в пипетку и наносят на фильтровальную бумагу размером 3 х 3 см в виде пятна диаметром в центре 2 см. В центре пятна наносят 1 каплю 0,1 н раствора сульфата железа (II). Когда жидкость впитается, туда же наносят 1 каплю 2 н раствора соляной кислоты. При наличии азота сразу же появляется синее пятно берлинской лазури (а). По периферии пятна исследуемого вещества наносят 1 каплю 0,1 н раствора ацетата свинца, а в противоположную сторону пятна – 1 каплю 0,5 н раствора нитропруссида натрия. При наличии серы в исследуемом веществе в первом случае (б) появится темно-коричневое пятно сульфида свинца, а в противоположной стороне (случай в) – красно-фиолетовое пятно комплексной соли Na4 [Fe(CN)5 (NОS)].
Микроколичества азота и серы в органических соединениях можно обнаружить по методу Рево. Для этого отфильтрованный раствор набирают в пипетку и наносят на фильтровальную бумагу размером 3 х 3 см в виде пятна диаметром в центре 2 см. В центре пятна наносят 1 каплю 0,1 н раствора сульфата железа (II). Когда жидкость впитается, туда же наносят 1 каплю 2 н раствора соляной кислоты. При наличии азота сразу же появляется синее пятно берлинской лазури (а). По периферии пятна исследуемого вещества наносят 1 каплю 0,1 н раствора ацетата свинца, а в противоположную сторону пятна – 1 каплю 0,5 н раствора нитропруссида натрия. При наличии серы в исследуемом веществе в первом случае (б) появится темно-коричневое пятно сульфида свинца, а в противоположной стороне (случай в) – красно-фиолетовое пятно комплексной соли Na4 [Fe(CN)5 (NОS)].


