Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Классификация почечно-клеточного рака
по системе TNM ( 7-я редакция, 2010 г.) Т первичная опухоль Тх первичная опухоль не может быть оценена Т0 нет данных о первичной опухоли Т1опухоль не более 7см в наибольшем измерении, ограниченная почкой Т1аопухоль не более 4см в наибольшем измерении, ограниченная почкой Т1bопухоль более 4 см, но не более 7см в наибольшем измерении, ограниченная почкой Т2опухоль более 7см в наибольшем измерении, ограниченная почкой Т2аопухоль более 7 см, но не более 10см в наибольшем измерении, ограниченная почкой Т2bопухоль более 10 см в наибольшем измерении, ограниченная почкой Т3 опухоль распространяется в крупные вены или инвазирует надпочечник или окружающие ткани, но не выходит за пределы фасции Герота Т3а опухолевая инвазия надпочечника или паранефральной клетчатки в пределах фасции Герота Т3Ь опухоль распространяется в нижнюю полую вену ниже диафрагмы Т3с опухоль распространяется в нижнюю полую вену выше диафрагмы или инвазирует ее стенку Т4 опухоль распространяется за пределы фасцииГерот (включая смежное распространение на ипсилатеральный надпочечник) Nрегионарные лимфатические узлы Nxрегионарные лимфатические узлы не могут быть оценены N0нет метастазов в регионарных лимфатических узлах N1метастаз в одном регионарном лимфатическом узле N2метастазы более, чем в одном регионарном лимфатическом узле М отдаленные метастазы Мх отдаленные метастазы не могут быть оценены М0 нет отдаленных метастазов М1 отдаленные метастазы Критерии р TNM (патологоанатомическая классификация рТ, pN, pM-критерии соответствуют T, N и М-критериям Критерий G (гистопатологическая градация) Gxстепень дифференцировки не может быть оценена G1высокодифференцированная опухоль G2умереннодифференцированная опухоль G34 низкодифференцированная /недифференцированная опухоль
Классификация РП по стадиям
КЛИНИКА РП Клинические факторы Прогностически неблагоприятным являются: общее тяжелое состояние больного, наличие симптомов заболевания на момент установления диагноза, снижение массы тела более чем на 10%, анемия, гиперкалиемия, гипоальбуминемия, повышение уровня щелочной фосфатазы сыворотки крови.
Патоморфологические факторы Стадия опухолевого процесса (Т), является наиболее значимым фактором прогноза при РП. Пациенты с опухолью, ограниченной почкой, имеют лучший прогноз, инвазия за пределы капсулы Герота (Т) уменьшает выживаемость на 27%, наличие опухолевого тромбоза почечной и нижней полой вен на 40%. Опухолевая инвазия в коллатеральные вены и капилляры также неблагоприятна. Метастазы в лимфоузлы свидетельствуют о плохом прогнозе (5-летняя выживаемость 5-30%). При наличии отдаленных метастазов стадия Т прогностического значения не имеет. Одним из наиболее важных прогностических факторов является возможность радикального удаления всех определяемых метастазов.
Гистопатоморфологические факторы Дифференцировка опухоли независимый фактор прогноза после стадии заболевания: 5-летняя выживаемость пациентов с опухолями G1составляет 75%, G270%, G350%, G435%. Плоидность ДНК коррелирует с благоприятным прогнозом. Митотический индекс опухоли связан с выживаемостью больных РП, установлено, что при наличии менее 1 митоза на 10 полей зрения, 10-летняя выживаемость достигает 65%, при большем количестве снижается до 1-15%. Генетические факторы Непапиллярный РП отличается худшей выживаемостью по сравнению с папиллярной и хромофобной формами. Рак собирательных протоков, составляющий 1-2% всех случаев почечно-клеточного рака, является агрессивной опухолью с высоким метастатическим потенциалом.
Клинические проявления рака почки Классическая триада симптомов рака почки: боль, гематурия, пальпируемая опухоль в настоящее время встречается редко. В большинстве случаев в начальных стадиях заболевание протекает бессимптомно. Появление микрои макрогематурии следует расценивать как наиболее ранний симптом РП, указывающий на необходимость обследования больных на предмет выявления опухоли почек, тем более, что современные методы диагностики позволяют выявлять опухоли до 0,5 см в диаметре. К сожалению, выраженные клинические проявления заболевания возникают, главным образом, на поздних стадиях. Среди местных симптомов наиболее часто отмечаются боль и гематурия.
Боли в пояснице и животе возникают при инвазии или сдавлении растущей опухолью окружающих структур, а также при почечной колике, обусловленной закупоркой мочеточников сгустками крови. Острая боль может быть также следствием кровоизлияния в опухоль или ее разрыва с последующим формированием заброшенной гематомы. Пальпируемая опухоль третий местный симптом рака почки, который бывает положительным у 12-15% пациентов на момент установления диагноза. Пальпация более эффективна при бимануальном исследовании, когда одной рукой надавливают сзади, а другой выполняют глубокую пальпацию спереди. Варикоцеле отмечается у 2-3% больных, как довольно редкий симптом, главным образом, при сдавлении нижней полой вены. Артериальная гипертензия непостоянный симптом (вызывается сдавлением сегментарных артерий, окклюзией мочеточника, метастазами в головной мозг, формированием артериовенозных шунтов или повышенной секрецией опухолью ренина) наблюдается у 15% больных раком почки. Синдром сдавления нижней полой вены (отеки ног, варикоцеле, расширения подкожных вен брюшной стенки, тромбоз глубоких вен нижних конечностей, протеинурия) развивается у 50% больных при опухолевом тромбозе НПВ или при ее сдавлении опухолью или увеличенными лимфатическими узлами. РП часто сопровождается развитием, так азываемых, паранеопластических синдромов, наблюдаемых более чем у половины больных. Нормальная почечная паренхима продуцирует разнообразные биологически активные вещества, в результате у пациентов могут возникать артериальная гипертензия, эритроцитоз, гиперкальциемия, гипертермия и др. Появление этих симптомов может быть единственным проявлением заболевания. После радикального удаления опухоли паранеопластические проявления, как правило, исчезают, но могут возникнуть вновь при рецидивировании или продолжении болезни. Таким образом, клинические проявления паранеопластического синдрома могут быть использованы также и для мониторинга заболевания. Редкой формой паранеопластического синдрома (1,7%) является амилоидоз. Сохраняющийся после нефрэктомии амилоидоз является крайне неблагоприятным фактором прогноза. В некоторых случаях при РП развиваются признаки печеночной недостаточности при отсутствии метастатического поражения печени: у больных отмечается гипоальбуминемия, повышение щелочной фосфатазы, лейкопения, лихорадка, возможно появление очагов некроза печеночной паренхимы (синдром Штафера). Восстановление функции печени после нефректомии является благоприятным прогностическим признаком. Более 25% больных на момент установления диагноза уже имеют отдаленные метастазы. При метастатическом поражении легких появляются кашель и кровохарканье. Костные метастазы могут манифестировать болевым синдромом, развитием патологических переломов, компрессией спинного мозга, появлением пальпируемой опухоли. Поражение головного мозга сопровождается быстрым появлением и нарастанием неврологической симптоматики. Множественные метастазы в печень могут проявляться желтухой. Как правило, появление общих симптомов: анемия, высокая СОЭ, потеря аппетита, похудание, слабость является признаком распространенного опухолевого процесса.
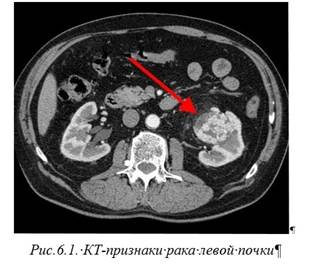
Диагностика и лечение рака почки. ДИАГНОСТИКА РАКА ПОЧКИ В результате появления современных неинвазивных диагностических методов, таких как УЗКТ, РКТ, МРТ, алгоритм обследования больных РП изменился. Зачастую опухоли почки обнаруживают случайно при УЗКТ, выполняемой по поводу другого заболевания. Несмотря на высокую диагностическую ценность УЗКТ, последняя всегда должна быть дополнена рентгеновской КТ, которая в настоящее время является основным методом диагностики объемных образований почки. Для диагностики и стадирования РП широко применяются УЗИ, компьютерная томография (в том числе, спиральная КТ), рентгенография легких. На рис.6.1 представлена компьютерная томограмма в артериально-паренхиматозную фазу, аксиальная плоскость, где отмечено образование верхнего сегмента левой почки в виде узла, размером 66×42×53мм, с неоднородной структурой, за счет гиподенсной зоны в периферических отделах образования.
Радиоизотопное сканирование скелета показано при наличии болей в костях и повышении уровня щелочной фосфатазы. МРТ выполняется больным с аллергией на йодсодержащие контрастные вещества, с хронической почечной недостаточностью, опухолевым тромбозом НПВ, а также для подтверждения наличия костных метастазов. Радионуклидная ренография выполняется для оценки функционального состояния пораженной и здоровой почек, что может иметь большое значение для решения вопроса о тактике лечения. Экскреторная урография в настоящее время реже применяется для диагностики РП, чаще для оценки функции контралатеральной почки. Если диагноз опухоли почки был установлен при ультразвуковой или рентгеновской компьютерной томографии, экскреторная урография не дает дополнительной информации для стадирования. Однако это исследование показано больным с макрогематурией для дифференциальной диагностики с папиллярными образованиями верхних мочевыводящих путей. Ультразвуковая компьютерная томография почек, в настоящее время является основным методом первичной диагностики рака почки. Метод позволяет не только диагностировать объемное образование почки, но и провести дифференциальный диагноз между простой или комплексной кистой и солидной опухолью. Несомненными достоинствами метода являются также его низкая стоимость, отсутствие побочных эффектов и возможность использования с целью скрининга РП. Использование допплеровского датчика позволяет определить гиперваскуляризацию опухоли, что более характерно для злокачественного процесса, однако этот критерий не является бесспорным, так как до 20% опухолей почки отличаются низкой васкуляризацией. Бесспорными достоинствами метода являются возможность интраоперационной оценки распространенности опухоли при выполнении резекции почки, определения протяженности опухолевого тромбоза НПВ и оценки распространенности поражения печени.
В качестве методов уточняющей диагностики используются РКТ, МРТ, ангиография (АГ), изотопные исследования, биопсия опухоли. Тонкоигольная биопсия опухоли применятся в случаях, когда дополнительные методы исследования не позволяют на дооперационном этапе установить диагноз, при этом точность диагностики достигает 98%. В тех случаях, когда в пунктате получены элементы крови, даже при отсутствии опухолевых клеток пункцию следует повторять, т. к. может иметь место распад опухоли с образованием гематомы.
ЛЕЧЕНИЕ РАКА ПОЧКИ
В лечении РП применяются все существующие на сегодняшний день методы противоопухолевой терапии: хирургический, химиотерапия (таргетная терапия), лучевая терапия, иммунотерапия.
Хирургическое лечение локализованного рака почки Хирургический метод и по сей день остается наиболее эффективным в лечении РП. Адьювантные методы лечения: химиотерапия, лучевая терапия, иммунотерапия – практически не повышают выживаемости больных РП. Радикальная нефрэктомия основное вмешательство при хирургическом лечении РП получила всеобщее признание после того, как в 1963 году Robson были опубликованы вполне приемлемые результаты хирургического лечения РП. Принципы выполнения радикальной нефрэктомии мало изменились с тех пор и включают в настоящее время: раннюю перевязку почечной артерии и вены; удаление почки вне фасции Герота вместе с окружающей паранефральной клетчаткой; удаление одноименного надпочечника; выполнение регионарной лимфаденэктомии. Наиболее важным моментом является удаление почки вне фасции Герота, так как ее инвазия отмечается в 25% случаев. Удаление надпочечника не всегда целесообразно, за исключением тех случаев, когда опухоль находится в верхнем полюсе или имеется субтотальное поражение почки. Влияние лимфаденэктомии на отдаленную выживаемость остается предметом дискуссии. 1) Радикальная нефрэктомия остается методом выбора в лечении локальных форм РП. Большинство исследователей считают, что резекция возможна при размерах опухоли не более 3-5см. 2) Радикальная нефрэктомия показана в случаях РП с опухолевой инвазией почечной и нижней полой вены. 3) Радикальная нефрэктомия может выполняться пациентам с единичными отдаленными метастазами в сочетании с их одномоментным или последовательным удалением. Паллиативная нефрэктомия применяется при РП для уменьшения интоксикации, снижения интенсивности болевого синдрома и купирования профузного кровотечения.
Преимуществами лапаротомного доступа при нефрэктомии являются возможность ревизии брюшной полости, удаления метастатических опухолей, выполнения операции при наличии сопутствующей патологии, например холецистэктомии при холецистите или экстирпации матки при фибромиоме. Из применяемых лапаротомных доступов наибольшее распространение получили срединный и трансректальный. В настоящее время с успехом применяются и лапароскопические операции, при которых доступ рассматривается просто как вид хирургического доступа. Торакоабдоминальные доступы применяются в случаях, когда тромб в нижней полой вене поднимается выше диафрагмы. Лимфаденэктомия при РП подразумевает удаление всей жировой клетчатки с лимфатическими узлами, окружающей магистральные сосуды, от уровня ножек диафрагмы, непосредственно ниже уровня отхождения верхней брыжеечной артерии, до бифуркации аорты и нижней полой вены. Обоснованием лимфаденэктомии является то, что наличие метастазов РП в лимфатические узлы является одним из наиболее значимых неблагоприятных факторов прогноза. Появление регионарных метастазов снижает выживаемость больных до 5-30%. Удаление пораженных лимфатических узлов может улучшить результаты хирургического лечения и, кроме того, обеспечить корректное стадирование, а, следовательно, и прогноз результатов лечения.
Хирургическое лечение рака почки, сопровождающегося опухолевым тромбозом РП имеет тенденцию к формированию опухолевых тромбов с их распространением по почечной и нижней полой венам вплоть до правого предсердия. Венозная инвазия встречается у 4-10% больных, из которых у 60% тромб распространяется выше устьев печеночных вен. Основным отличием нефрэктомии с тромбэктомией является необходимость мобилизации и резекции НПВ. Особенно опасно удаление тромба при его распространении на правое предсердие, при некоторых видах тромбоза требуется кардиопульмональное шунтирование и гипотермия с остановкой кровообращения. У больных без отдаленных метастазов радикальная нефрэктомия с тромбэктомией обеспечивает 5-летнюю выживаемость от 50 до 65%. Активный хирургический подход к больным с опухолевым тромбозом НПВ является эффективным методом лечения, а радикальное удаление тромба любой протяженности дает шанс на выздоровление большинству больных. Резекция почки является методом выбора в тех случаях, когда опухоль располагается в одном из полюсов почки, не деформирует почечную лоханку и не превышает 3 см в наибольшем измерении. Наряду с традиционными методиками, в последнее время эта операция выполняется с помощью так называемого «биоэлектросварочного аппарата», разработанного под руководством академика Б. Е. Патона. Методика позволяет выполнять операцию с минимальной кровопотерей. Энуклеацию опухоли допустимо выполнять у больных с единственной функционирующей почкой при условии, что размеры опухоли не превышают 3см, и она локализована в одном из полюсов.
|
|||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 42; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.147.124 (0.028 с.) |