Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Инструментальные исследования в диагностике РЛ
Наиболее простым и доступным методом исследования при РЛ является рентгенография легких, обязательно в двух проекциях, для того чтобы выявить патологические образования, скрытые за тенью сердца или куполами диафрагмы. Наиболее эффективным рентгеновское исследование является при периферических и перибронхиальных опухолях и позволяет выявить новообразования диаметром от 5-10 мм. Менее информативно рентгеновское исследование - при центральном раке, когда опухоль располагается в просвете бронха и не видна на его фоне. В подобных случаях обтурация бронха выявляется по косвенным признакам: гиповентиляция, ателектаз, смещение тени средостения в больную сторону, высокое стояние купола диафрагмы с пораженной стороны, симптом Гольцхнехт-Якобсона - смещение тени средостения на глубоком вдохе в больную сторону. В начальных стадиях центрального РЛ рентгенологические симптомы отсутствуют, и ориентироваться на них в диагностике заболевания нельзя. Компьютерная томография органов грудной клетки, брюшной полости и забрюшинного пространства позволяет точно определить локализацию процесса (рис.2.1 и рис.2.2), вовлечение соседних структур, распространение процесса на грудную стенку и средостение, выявить наличие увеличенных лимфоузлов в средостении, метастазов в головном мозге и других органах. Внутривенное контрастирование позволяет визуализировать лимфоузлы и сосудистые структуры средостения, уточнить особенности васкуляризации опухоли. Но на основании только рентгеновского исследования нельзя судить о характере процесса (доброкачественный или злокачественный) и принимать решение о невозможности хирургического лечения.
Магнитно-резонансная томография дает возможность выявить отдаленные метастазы в головной мозг, оценить распространение опухоли на окружающие структуры, особенно инвазию крупных сосудов, мягких тканей, тел позвонков. МРТ может рассматриваться как альтернатива КТ при непереносимости йодсодержащих контрастных препаратов. Позитронно-эмиссионная томография (ПЭТ) превосходит КТ в оценке характера поражения медиастинальных лимфоузлов. ПЭТ позволяет диагностировать опухолевую инвазию грудной стенки и средостения, дифференцировать воспалительные и опухолевые изменения.
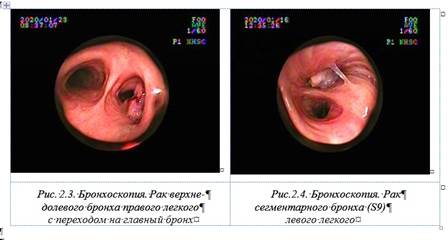
Бронхологическое исследование - обязательный метод в диагностике РЛ (рис.2.3 и рис.2.4). Бронхоскопия позволяет выявить даже начальные формы эндобронхиального рака и верифицировать диагноз с помощью щеточной или щипцевой биопсии и исследования промывных вод бронхов. Бронхоскопию необходимо выполнять всем больным с подозрением на РЛ при наличии кашля, признаков бронхиальной обструкции, а тем более - при кровохаркании. Флюоресцентная бронхоскопия повышает эффективность ранней диагностики эндобронхиального рака.
Чрезбронхиальная пункционная биопсия выполняется для морфологической верификации поражения медиастинальных лимфатических узлов, однако информативность метода невелика в связи с большим количеством ложноотрицательных результатов при оценке N2. Эндоскопическая пищеводная и эндобронхиальная сонография применяются для оценки состояния различных групп медиастинальных лимфатических узлов и для их тонкоигольной биопсии. Оба метода отличаются высокой чувствительностью (90-95%) и специфичностью (95-100%). Трансторакальная пункционная биопсия применяется для диагностики новообразований, расположенных в периферических отделах легких. Из наиболее серьезных осложнений метода следует отметить кровохарканье, пневмоторакс и воздушную эмболию. При развитии воздушной эмболии во время исследования необходимо немедленно придать больному горизонтальное положение с опущенной головой. Для своевременной диагностики пневмоторакса необходим аускультативный, а при необходимости - и рентгеновский, контроль в течение 3-4 часов после исследования. Плевральная пункция с последующим морфологическим исследованием применяется при наличии гидроторакса и является обязательной даже при минимальном количестве жидкости в плевральной полости. Пункция выполняется в проекции скопления жидкости, под местной анестезией, по верхнему краю нижележащего ребра. После исследования необходимо наблюдение за пациентом в течение 2 часов с целью своевременной диагностики пневмоторакса. Медиастиноскопия выполняется в условиях операционной под общим обезболиванием. Через разрез в яремной ямке в средостение проводится медиастиноскоп, через который под визуальным контролем выполняется биопсия медиастинальных лимфоузлов. Исследование показано для верификации метастатического поражения медиастинальных, паратрахеальных и бифуркационных лимфоузлов (N2).
Торакоскопия (видеоторакоскопия) также выполняется в условиях операционной под общим обезболиванием. Через торакоскоп, введенный в плевральную полость, тщательно осматриваются легкое и плевра, выполняется биопсия подозрительных участков плевры, легкого и лимфоузлов. Из других инструментальных методов исследования в диагностике рака легкого применяются трансбронхиальная пункция лимфатических узлов (во время бронхоскопии), биопсия надключичных лимфоузлов, радиоизотопное сканирование скелета (для выявления костных метастазов), цитологическое исследование мокроты. ЛЕЧЕНИЕ РАКА ЛЕГКОГО
Результаты лечения РЛ на сегодняшний день следует признать неудовлетворительными. Показатели 5-летней выживаемости больных за последние 20 лет практически не изменились и составляют в Европе для мужчин - 7%, для женщин - 12%, несколько выше - средние показатели выживаемости в США и Японии. Это обьясняется, прежде всего, высоким метастатическим потенциалом РЛ, а также тем, что 80-85% впервые выявленных больных РЛ на момент выявления - уже неоперабельны. Основным методом лечения РЛ остается хирургический, 5-летняя выживаемость после радикальных операций колеблется в пределах 30% и не изменилась на протяжении последних 40 лет. В специализированных онкоторакальных клиниках послеоперационная летальность не превышает 2- 3%. В связи с высокой частотой лимфогенного метастазирования РЛ и необходимостью удаления регионарных лимфатических узлов в хирургии опухолей легкого применяются операции в объеме удаления доли легкого (лобэктомия), двух долей справа (билобэктомия) и полное удаление легкого (пульмонэктомия), открытым, видеоторакоассистированным и видеоторакоскопическим способом. Видеоторакоскопические операции в несколько раз дороже открытых, из-за стоимости расходных материалов. Техника торакальных операций к настоящему времени базируется на следующих принципах: раздельная обработка элементов корня легкого; ипсилатеральная лимфодиссекция; хирургическая профилактика несостоятельности бронхиальной культи. Исследования последних лет показывают, что радикальные операции с расширенной лимфодиссекцией при опухолях T1-3N1-2М0 позволяют улучшить отдаленные результаты хирургического лечения РЛ на 10-20%. Наряду с этим, в хирургии РЛ получили признание бронхопластические операции в сочетании с современной комбинированной химиолучевой терапией, направленные на максимально возможное сохранение легочной паренхимы, разумеется, при условии соблюдения всех принципов радикализма. Паллиативные операции (при наличии отдаленных лимфо - или гематогенных метастазов) считаются при РЛ малооправданными, так как практически не продлевают жизнь больным. В то же время, вполне обоснованными являются малоинвазивные симптоматические вмешательства, направленные на восстановление бронхиальной проходимости, ликвидацию гидроторакса или болевого синдрома. Подобные вмешательства, не продлевая жизнь больным, позволяют значительно улучшить ее качество.
Результаты хирургического лечения РЛ прямо зависят от стадии процесса и, в первую очередь, от наличия лимфогенных метастазов. При Т1N0M0 пятилетняя выживаемость достигает 50-70%, при Т2Nt М0 - 30- 50%, при T1-3N1-2M0 - 25-35%. Считается, что больные, не подлежащие радикальному хирургическому лечению погибают преимущественно в течение года с момента установления диагноза. В связи с тем, что около 85% больных РЛ оказываются неоперабельными проблема консервативного лечения этого заболевания остается актуальной.
Химиотерапия РЛ Химиотерапия (ХТ) считается недостаточно эффективной при РЛ, но широко применяется в качестве компонента комбинированного лечения, а также для купирования осложнений опухолевого процесса (обтурационный пневмонит, плеврит, синдром сдавления верхней полой вены) и улучшения качества жизни. Наиболее выраженный эффект после ХТ отмечается при мелкоклеточном РЛ, вплоть до выраженной регрессии опухоли и метастазов. Однако ремиссия при мелкоклеточном раке, как правило, непродолжительна и гарантировать стойкий эффект лечения невозможно. Все остальные морфологические формы РЛ, объединеные в группу НМЛР, менее чувствительны к химиотерапии, эффективность которой в этой группе не превышает 30-35%. В ХТ при РЛ применяются различные препараты и множество схем полихимиотерапии (ПХТ) на основе их сочетания, в основном платиновые дуплеты. Системная ПХТ применяется в метастатических стадиях заболевания (N+), до (неоадьювантная) и после выполнения хирургического вмешательства (адьювантная) или при неоперабельном РЛ. При неоперабельном опухолевом процессе предполагается проведение 6 курсов терапии при наличии эффекта от лечения или 4 курсов в случаях, когда достигнута только стабилизация процесса. Дальнейшее прогрессирование заболевания является показанием для перехода на очередную линию ХТ. В последнее время все большее внимание уделяется предоперационной (неоадьювантной/индукционной) ПХТ, которая показана в тех случаях когда имеются признаки метастатического поражения медиастинальных лимфузлов или распространения опухоли на окружающие ткани и органы (стадии IIB - IIIA). Предоперационная ПХТ предполагает проведение 2-3 курсов лечения, после чего выполняется радикальная операция. Наблюдения показывают, что подобная тактика лечения при местнораспространенном НМРЛ (T2-3N1-2) позволяет значительно уменьшить количество местных рецидивов и улучшает результаты выживаемости.
Наиболее распространенные химиопрепараты для лечения РЛ: цисплатин (карбоплатин), гемцитабин, этопозид, винорельбин, доцетаксел, митотакс, иринотекан, топотекан, митоксантрон, митомицинС, циклофосфан, метотрексат, ифосфамид, блеомицин, винкристин, винбластин, доксорубицин, а также их аналоги и производные. Включение в схему третьего препарата незначительно повышает эффективность лечения, но приводит к существенному увеличению токсичности. При выявлении мутаций генов эпидермального фактора роста (ЕGFR) и гена анапластической лимфомы (ALK), которые выявляют при аденокарциномах легкого у 30-70% больных, назначают таргетные препараты: гефитиниб, эрлотиниб, кризотиниб, бевацизумаб и др. Несмотря на то, что современная ХТ не на много продлевает жизнь больным, ее применение оправдано с целью ликвидации осложнений РЛ, повышения резектабельности и улучшения качества жизни больных.
|
||||||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 102; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.137.243 (0.01 с.) |