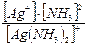Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Комплексные соединения в аналитической химии
Комплексные соединения находят широкое применение в аналитической химии. Комплексными называют соединения сложного состава, образованные из более простых структурных единиц (ионов, молекул). В составе комплексного соединения различают внутреннюю и внешнюю сферы. Внутренняя сфера комплексного соединения образована центральным атомом, в качестве которого наиболее часто выступает катион металла, и лигандами, которые координированы вокруг центрального атома. В качестве лигандов могут выступать как нейтральные так и заряженные частицы. Подавляющее большинство комплексных соединений в водных растворах являются сильными электролитами. Связь между внутренней и внешней сферой — ионная, поэтому комплексные соединения легко диссоциируют. Например: [Ag(NH3)2]Cl = [Ag(NH3)2]+ + Cl–. Связь между центральным ионом и лигандами более прочная, чем ионная, и близка к ковалентной. Эта связь образована по донорно-акцепторному механизму. Следует отметить, что комплексный ион также способен к диссоциации в растворе, при этом он проявляет свойства слабого электролита: [Ag(NH3)2]+ ↔ Ag+ +2NH3. Этот процесс является равновесным, поэтому в растворах всегда присутствуют комплексный ион и ионы комплексообразователя и лиганды. Равновесный процесс диссоциации комплексного иона в растворе определяет его нестойкость, которая описывается константой нестойкости. Для рассматриваемого случая константа нестойкости равна:
Кн = Чем больше константа нестойкости, тем в большей степени комплексный ион распадается на ионы. Значения констант нестойкости некоторых комплексных ионов приведены в Приложении (табл. 4). Вместо константы нестойкости часто для характеристики равновесного процесса диссоциации комплексного иона используют величину, обратную Кн, которую называют константой устойчивости: Куст = Чем больше константа устойчивости, тем в меньшей мере комплексный ион подвергается диссоциации и обладает большей устойчивостью в растворе. Комплексные соединения обладают рядом ценных свойств, благодаря чему широко используются в аналитической химии для обнаружения и маскировки ионов, осаждения и растворения осадков, разделения смеси ионов. Связывая какой-либо ион в комплексное соединение, можно фактически исключить его из раствора.
Обнаружение ионов проводят с помощью реакций комплексообразования, сопровождающихся изменением окраски растворов или образованием окрашенных осадков. Например, Fe3+ открывают по реакции образования с тиоцианатом калия комплексного соединения [Fe(SCN)3], имеющего красный цвет; ион Cu2+ с раствором аммиака образует комплексный ион [Cu(NH3)4]2+ синего цвета; о присутствии иона аммония судят по образованию малорастворимого комплексного соединения [Hg2ONH2]I красно-бурого цвета. Ионы комплексообразователя и лигандов, находясь в составе комплекса, практически отсутствуют в растворе и не всегда обнаруживаются химическими реакциями. Свойства ионов изменяются в составе комплексных соединений, что широко используется для разделения и маскировки ионов в анализе. Например, ион железа (III), мешающий обнаружению ряда катионов, маскируют, связывая его в комплекс фторид-ионом [FeF6]3–. Реакции комплексообразования избирательны и позволяют проводить анализ сложных смесей веществ без их разделения. Например, при осаждении гидроксидов катионов IV аналитической группы избытком раствора аммиака только катион цинка связывается в аммиачный комплекс и остается в растворе. Комплексообразование широко используется в анализе для перевода малорастворимых соединений в раствор и разделения ионов. Так, осадок HgI2 растворяется в избытке раствора КI, образуя комплексное соединение K2[HgI4]; осадок AgCl, не растворимый в кислотах и щелочах, хорошо растворяется при действии аммиака с образованием комплексного соединения [Ag(NH3)2]Cl, что используется для отделения Ag+ от других катионов и его обнаружения. Важным является тот факт, что реакции комплексообразования катионов металлов возможны с лигандами как неорганического, так и органического типа. При этом образуются продукты, которые обладают определенными аналитическими свойствами. Они позволяют упростить ход химического анализа, повысить чувствительность и избирательность аналитических реакций. Например, для обнаружения иона Ni2+ используют диметилглиоксим, иона алюминия — ализарин, цинка — дитизон.
Решение типовых задач
|
|||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 137; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.126.5 (0.005 с.) |