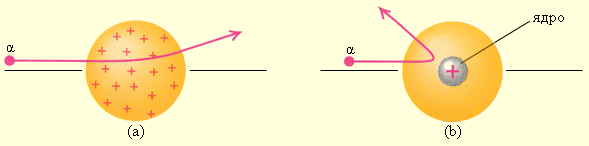Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Модель резерфорда. Ядро атома
Опыт заключался в бомбардировке тонкого листа золотой фольги пучком альфа-частиц, которые, как тогда уже было известно, представляют собой заряженные атомы гелия. Если бы модель Томсона была верна, то все альфа-частицы проходили бы через лист фольги, лишь немного отклоняясь от первоначального направления движения (рисунок а).
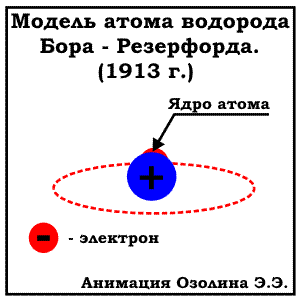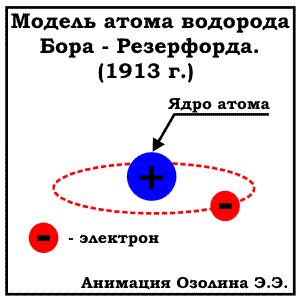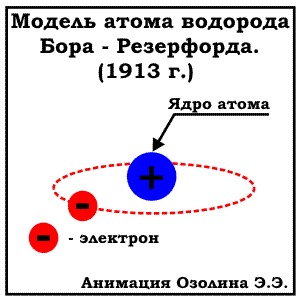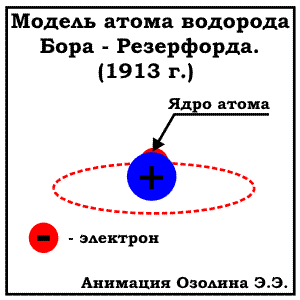
В действительности же результаты оказались удивительными: большинство альфа-частиц действительно отклонялось очень слабо, однако небольшая часть отклонялась на большие углы, а некоторые вообще отражались назад (рисунок b). Из результатов эксперимента Резерфорд сделал вывод, что «модель пудинга» была неверна, а в действительности же положительный заряд и подавляющая часть массы атома сосредоточены в небольшой области в центре атома, размеры которой значительно (более чем в тысячу раз) меньше размеров самого атома. Эта область позже получила название атомного ядра. В 1917 Резерфордом был открыт протон - положительно заряженная элементарная частица. Тогда же он предположил и о существовании нейтрально заряженных частиц - нейтронов, чье существование и было экспериментально подтверждено позже Дж. Чэдвиком. На основании полученных результатов Резерфордом была предложена следующая модель атома:. Атом состоит из положительно заряженного ядра и электронов вокруг него. МОДЕЛЬ БОРА (ПЛАНЕТАРНАЯ МОДЕЛЬ). ЭНЕРГЕТИЧЕСКИЕ УРОВНИ В 1913 Нильсом Бором была предложена модель строения атома, известная как "планетарная модель". По Бору электроны вращаются по орбитам расположены на строго определенном удалении от атомного ядра, точно также как планеты Солнечной системы вращаются вокруг солнца (отсюда и название модели). Эти орбиты (сейчас всем известны как энергетические уровни)- стационарные и вне их электрон существовать не может. К сожалению, объяснить это утверждение Бору на тот момент не удалось. Кроме того, предложенная модель Бора противоречила законам физики:
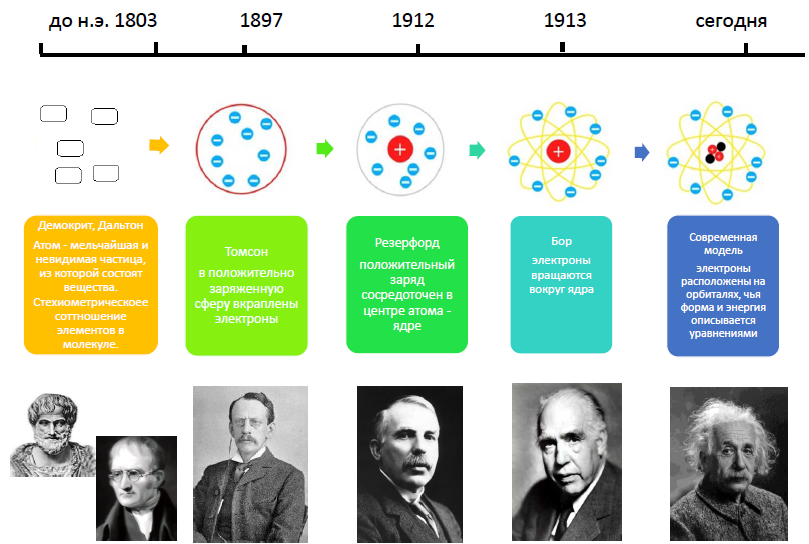
В начале прошлого века на смену планетарной модели строения атома пришла волновая модель, которая разрешила возникшие противоречия и на сегодняшний момент считается общепринятой. Современное представление о строении атома было бы невозможно без открытия явления радиоактивности, элементарных частиц (электрона, протона и нейтрона). Решающий вклад в установлении строения атома внесли Дальтон, Дж.Дж. Томпсон (или Томсон), Э. Резерфорд, Н. Бор, Э. Шредингер, М. Планк, Люис, Паули. История развития представлений о строении атома условно изображена на схеме ниже:
|
||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 413; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.8.110 (0.004 с.) |