
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кислотність води. Загальні відомості
Кислотність природних вод залежить в основному від вмісту розчиненого вільного діоксиду вуглецю, гумінових та інших слабких органічних кислот. Визначення кислотності проводять, як правило, одразу після відбору проби води. Під кислотністю води розуміють вміст у воді речовин, що реагують з 0,1 М розчином NaOH. Визначення кислотності проводять, як правило, одразу після відбору проби води. Кислотність природних незабруднених вод зумовлена: · вмістом розчиненого діоксиду вуглецю · вмістом гумінових й інших слабких органічних кислот. Величина рН таких природних вод більше за 4,4. Якщо рН води менша ніж 4,4, то така вода може бути забруднена сильними мінеральними кислотами або солями, що утворені сильними кислотами й слабкими гідроксидами, які у воді гідролізуються з утворенням кислого середовища. Кислотність води визначають титруванням проби води 0,1 М розчином NaOH [1]. Відомо, що при титруванні електрометричним методом за допомогою рН- метру, кінець титрування вільної кислотності має місце при рН ≈ 4,4, а загальної кислотності – при рН ≈ 8,3. При звичайному титруванні з використанням індикаторів метилового жовтогарячого (інтервал переходу забарвлення від – 3 до 4,4, а рТ = 4) і фенолфталеїну (інтервал переходу забарвлення рН – від 8,2 до10, а рТ = 9) кількість 0,1 М розчину NaOH, при використанні якого рН розчину досягає значення 4,4 (жовте забарвлення метилоранжу), відповідає вільній кислотності, а 9 (слабке рожеве забарвлення) – загальній кислотності. Якщо рН досліджуваної води більше за 9 (забарвлення фенолфталеїну рожеве), то її кислотність дорівнює нулю. 6.3.1. Методика визначення загальної кислотності ( рН від 0 до 9 ). У конічну колбу місткістю 200–250 мл піпеткою відібрати 100 мл досліджуваної води, додати 3–4 краплини фенолфталеїну і титрувати 0,1 М розчином NaOH (розчин лугу додавати краплинами) до появи слабкого рожевого забарвлення розчину, яке не повинно зникати протягом 2–3 хв. Титрування повторити декілька разів до отримання не менше, ніж трьох результатів, що відрізняються не більше, ніж на 0,1 мл. Загальну кислотність (ммоль/л) розраховують за формулою:
де
6.3.2. Методика визначення вільної кислотності (рН < 4,4) У конічну колбу місткістю 250–350 мл піпеткою налити 100 мл досліджуваної води, додати 3–4 краплини метилового жовтогарячого і титрувати 0,1 М розчином NaOH до зміни кольору від червоного до жовтого. Якщо при додаванні до проби води метилового жовтогарячого забарвлення води стає жовтим, то це означає, що вільна кислотність дорівнює нулю. Титрування повторюють кілька разів до отримання не менше, ніж трьох результатів, що відрізняються не більше, як на 0,1 мл. Вільну кислотність (ммоль/л) розраховують за формулою (6.1).
|
|||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 115; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.171.180 (0.004 с.) |
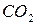 ;
;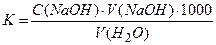 , (6.1)
, (6.1)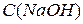 – молярна концентрація
– молярна концентрація 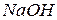 у розчині, моль/л;
у розчині, моль/л;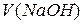 – об’єм робочого розчину
– об’єм робочого розчину 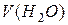 – об’єм проби води, мл.
– об’єм проби води, мл.


