
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Изучение химических свойств моно-, ди- и полисахаридов
Опыт 1. Взаимодействие сахаров с гидроксидом меди (II) в щелочном растворе. Реактивы и оборудование: 1 % растворы глюкозы, сахарозы, мальтозы, 10 % раствор гидроксида натрия, 5 % раствор сульфата меди (II), пробирки, спиртовка, пробиркодержатель. Ход работы: опыт одновременно проводят с несколькими сахарами. К 2 мл 1 % раствора глюкозы (1 пробирка), сахарозы (2 пробирка) и мальтозы (3 пробирка) добавляют 1 мл 10 % раствора гидроксида натрия и 2-3 капли Во второй пробирке наблюдаем ________________________________. В третьей пробирке наблюдаем__________________________________, и жидкости окрашиваются в __________________ цвет. Эта реакция доказывает _______________________________________________________, т. е. она характерна для многоатомных спиртов. Уравнение реакции взаимодействия глюкозы (цикличекая форма) с гидроксидом меди (II) имеет вид:
Затем осторожно нагревают в пламени спиртовки верхнюю часть жидкости в каждой пробирке до начала кипения. При этом в первой пробирке (глюкоза) наблюдаем _______________________________________. Во второй пробирке (сахароза): ____________________________________. В третьей пробирке (мальтоза):__________________________________. Эта реакция показывает, что ______________________________________. Уравнение реакции окисления глюкозы в глюконовую кислоту с Cu(OH)2:
Уравнение реакции окисления мальтозы в мальтобионовую кислоту с Cu(OH)2: Вывод: Опыт 2. Окисление глюкозы и сахарозы аммиачным раствором оксида серебра (реакция серебряного зеркала). Реактивы и оборудование: аммиачный раствор оксида серебра [Ag(NH3)2]OH, 1 % раствор глюкозы и сахарозы, предметное стекло, спиртовка, пробиркодержатель. Ход работы: опыт проводить одновременно с двумя сахарами. На предметное стекло нанести 3-4 капли аммиачного раствора оксида серебра и столько же 1 % раствора глюкозы (или сахарозы). Стекло слегка, стараясь избегать кипения, подогреть и наблюдать, в случае взаимодействия ___________ с аммиачным раствором оксида серебра, появление блестящего налета – ____________. Уравнение реакции имеет вид:
Вывод:
Опыт 3. Гидролиз (инверсия) сахарозы. Реактивы и оборудование: 1 %-й раствор сахарозы, 10 %-й раствор серной кислоты, сухой гидрокарбонат натрия, реактив Фелинга, пробирка, пробиркодержатель, спиртовка.
Ход работы: в пробирку наливают 3 мл 1 % раствора сахарозы и приливают 10 %-й раствор серной кислоты. Полученный раствор кипятят в течение 1-2 мин, затем охлаждают и нейтрализуют сухим гидрокарбонатом натрия (Осторожно!!! Жидкость вспенивается из-за выделяющегося СО2). После нейтрализации приливают равный объём реактива Фелинга и нагревают верхнюю часть жидкости до начинающегося кипения. При этом окраска реакционной смеси _______________________________________. Уравнение реакции гидролиза сахарозы имеет вид:
Вывод: Опыт 4. Взаимодействие крахмала с йодом. Реактивы и оборудование: 1 % раствор крахмального клейстера, раствор йода, пробирка, пробиркодержатель, спиртовка. Ход работы: в пробирку налить 1 мл 1 % раствора крахмального клейстера и добавить 1-2 капли раствора йода. При этом появляется____________________. Нагреваем полученную смесь, наблюдаем _____________________________________. При дальнейшем охлаждении окраска ______________________________. Схематично взаимодействие йода с крахмалом имеет вид:
Вывод: § 4.2. Аминокислоты Аминокислоты – это производные алифатических или ароматических углеводородов, содержащие одновременно амино (–NH2) и карбоксильную (–СООН) группы. · В зависимости от положения аминогруппы (у α-, β-, γ- углеродного атома) выделяют α-, β-, γ-аминокислоты. · Белки образованы остатками α-аминокислот. · Общая формула α-аминокислот: NH2 – СН(R) – СООН. · Виды изомерии: структурная (изомерия углеродного скелета, изомерия положения аминогруппы) и пространственная (оптическая для α-аминокислот). · Аминокислоты – это амфотерные соединения: основные свойства обусловлены наличием аминогруппы, кислотные – наличием карбоксильной группы. * в кислой среде аминокислоты – катионы; * в щелочной – анионы; * в нейтральной среде аминокислоты существуют в виде биполярных (или цвиттер) ионов, т. е. ионов, имеющих два полюса (+) и (–): NH2 – СН(R) – СООН <=> +NH3 – СН(R) – СОО–.
Задания для самостоятельной работы 96. Составьте формулы и назовите аминокислоты, изомерные γ-аминомаслянной кислоте. 97. Приведите формулы двух аминокислот, одна из которых имеет оптические изомеры, а другая нет.
98. Приведите примеры аминокислот, у которых преобладают: 99. Составьте схему образования амфиона аланина. 100. Напишите уравнения реакций, доказывающих амфотерность аланина (2-аминопропионовая кислота). 101. Составьте схему реакции получения пептида гли-фен-ала. К какому типу пептидов (ди-три-…поли) он относится, приведите полное название этого пептида, обозначьте пептидную связь. 102. Сколько трипептидов может быть получено из трёх аминокислот: цистеина, аланина и лизина? Приведите их формулы и назовите их. Лабораторная работа № 5 Аминокислоты Опыт 1. Отношение аминокислот к индикаторам. Реактивы и оборудование: 2 % раствор глицина, метиловый оранжевый, лакмус, пробирки. Ход работы: в две пробирки наливают по 1 мл 2 % раствора глицина и добавляют по 2 капли растворов индикаторов. Наблюдаем:_______________. То есть, водный раствор этой аминокислоты имеет _______________ реакцию среды. Моноаминомонокарбоновые кислоты в водных растворах существуют в виде биполярных ионов: Н2N – CH2 – COOH <=> Глицин Биполярный ион
Опыт 2. Образование медной соли аминоуксусной кислоты. Реактивы и оборудование: карбонат меди (II), 2 % раствор глицина, Ход работы: в сухую пробирку вносят 0,5 г карбоната меди (II) и Оставшуюся часть жидкости охлаждают в стакане с ледяной водой, протирая стенки пробирки стеклянной палочкой. Наблюдаем _________________________________________________________________.
2Н3N+ – CН2 – СОО– + СuCO3 →
CH2 – NH2 O – C = O
Приложение Таблица 1 Названия кислот и солей Кислота |
Кислотный остаток |
Название соли | |||||||
| Формула | Название | Формула (валентность указана черточками) | Валентность кислотного остатка | |||||||
| HI | Иодоводородная | ― I | I | Иодид | ||||||
| HClO4 | Хлорная | ― ClO4 | I | Перхлорат | ||||||
| HBr | Бромоводородная | ― Br | I | Бромид | ||||||
| HCl | Хлороводородная (соляная) | ― Cl | I | Хлорид | ||||||
| H2SO4 | Серная | = SO4 ― HSO4 | II I | Сульфат Гидросульфат | ||||||
| HMnO4 | Марганцовая | ― MnO4 | I | Перманганат | ||||||
| HNO3 | Азотная | ― NO3 | I | Нитрат | ||||||
| HClO3 | Хлорноватая | ― ClO3 | I | Хлорат | ||||||
| CCl3COOH | Трихлоруксусная | CCl3COO ― | I | Трихлорацетат | ||||||
| H2CrO4 | Хромовая | = CrO4 | II | Хромат | ||||||
| H2MnO4 | Марганцовистая | = MnO4 | II | Манганат | ||||||
| H2C2O4 | Этандиовая (щавелевая) | = C2O4 ― HC2O4 | II I | Оксалат Гидрооксалат | ||||||
| CHCl2COOH | Дихлоруксусная | CHCl2COO― | I | Дихлорацетат | ||||||
| H2Cr2O7 | Двухромовая (дихромовая) | = Cr2O7 | II | Дихромат | ||||||
| H2SO3 | Сернистая | = SO3 ― HSO3 | II I | Сульфит Гидросульфит | ||||||
| HClO2 | Хлористая | ― ClO2 | I | Хлорит | ||||||
| H3PO4 | Ортофосфорная (фосфорная) | ≡ PO4 = HPO4 ― H2PO4 | III II I | Фосфат Гидрофосфат Дигидрофосфат | ||||||
| CH2ClCOOH | Хлоруксусная | CH2ClCOO― | I | Хлорацетат | ||||||
| HF | Фторофодородная (плавиковая) | ― F | I | Фторид | ||||||
| HNO2 | Азотистая | ― NO2 | I | Нитрит | ||||||
| HCOOH | Метановая (муравьиная) | HCOO― | I | Формиат | ||||||
| C6H5COOH | Бензойная | C6H5COO― | I | Бензоат | ||||||
| CH3COOH | Этановая (уксусная) | CH3COO― | I | Ацетат | ||||||
| H2CO3 | Угольная | = CO3 ― HCO3 | II I | Карбонат Гидрокарбонат | ||||||
| H2S | Сероводородная | = S ― HS | II I | Сульфид Гидросульфид | ||||||
| HClO | Хлорноватистая | ― ClO | I | Гипохлорит | ||||||
| HCN | Циановодородная (синильная) | ― CN | I | Цианид | ||||||
| H2SiO3 | Ортокремниевая | = SiO3 | II | Силикат | ||||||
| C6H5OH | Фенол (карболовая) | C6H5O― | I | Фенолят | ||||||
| HAlO2 | Метаалюминиевая | ― AlO2 | I | Метаалюминат | ||||||
| H2ZnO2 | Цинковая | = ZnO2 | II | Цинкат | ||||||
Таблица 2
|
|
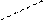
 → О = С – О NH2 – CH2
→ О = С – О NH2 – CH2
 │ Cu │ + H2O + CO2↑
│ Cu │ + H2O + CO2↑


