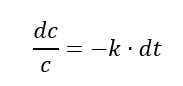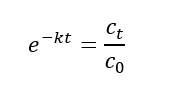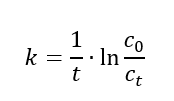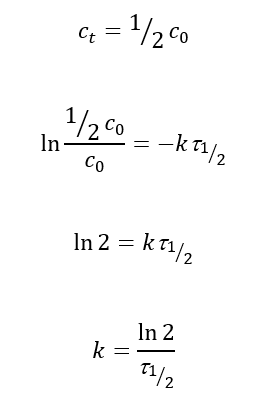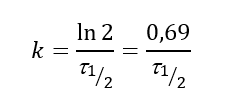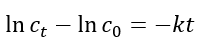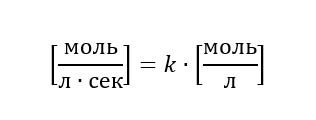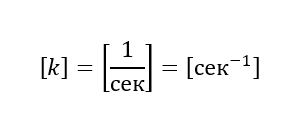Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Реакции первого порядка. Выражение для константы скорости, времени полупревращения.
Реакции первого порядка – это реакции, в которых показатель степени в уравнении зависимости скорости от концентрации, в которую возводится концентрация, равен единице. Все реакции радиоактивного распада являются реакциями первого порядка. Также можно привести в пример реакции изомеризации, распада некоторых молекул в газовой фазе: N2O5, CH3-O-CH3 и т. д. Выражение для мгновенной скорости реакции по какому-либо из реагентов записывается в виде: , где v – мгновенная скорость, dc – бесконечно малое изменение молярной концентрации, dt – бесконечно малый промежуток времени. Напомним, что знак минус перед правой частью уравнения ставиться для того, чтобы скорость была положительной величиной (изменение концентрации реагента – величина отрицательная, так как концентрация реагентов во время протекания реакции уменьшается). По закону действующих масс – закону Гульберга-Вааге, скорость реакции прямо пропорциональная концентрации. Для реакций первого порядка (порядок – показатель степени, в которую возводится концентрация) математическое выражение этого закона принимает вид:
Приравняем правые части приведённых выше уравнений друг к другу:
Разнесём переменные:
Для того чтобы понять сколько вещества вступит в реакцию за определенный интервал времени, нам необходимо решить данное дифференциальное уравнение, т. е. найти его первообразную. Запишем выражение для вычисления определённого интеграла, чтобы в дальнейшем не решать задачу Коши (решение дифференциального уравнения, удовлетворяющего начальным условиям, для нас это исходная концентрация и исходное время). Хотя, можно поступить иначе и вычислить неопределённый интеграл данного уравнения, а затем через начальные условия определить константу интегрирования (т. е. решить задачу Коши).
Для нахождения интеграла вспомним, что:
, где С – постоянная интегрирования Результат интегрирования следующий:
Запишем уравнение иначе:
Потенцируем уравнение:
Отсюда найдем уравнение для нахождения концентрации регента в момент времени t:
Если изменить порядок действий, то легко прийти к уравнению для нахождения константы реакции первого порядка:
Выведем уравнение для нахождения константы реакции первого порядка через период полупревращения.
Период полупревращения – время, которое необходимо для превращения половины исходного количества вещества. Т. е. к моменту времени t молярная концентрация вещества будет равна ½ её исходного значения:
Для решения расчётных задач можно использовать формулу:
Из формулы видно, что время полупревращения для реакций первого порядка не зависит от количества, или концентрации исходного вещества. Приведём уравнение
к виду
Это уравнение есть ни что иное как линейная зависимость ln(c) от t. Построим график этой зависимости.
Отсюда, константа скорости реакции первого порядка численно равна тангенсу угла наклона прямой к оси t.
Определим размерность константы реакции первого порядка. Для этого в уравнение:
подставим размерности скорости и молярной концентрации:
Отсюда размерность константы реакции первого порядка.
|
|||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 205; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.174.168 (0.004 с.) |

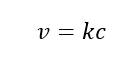 , где k – константа скорости.
, где k – константа скорости.