Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Показатели процесса электролиза
Понятие о выходе по току, удельном расходе электрической энергии, выходе по энергии Как и всякий электрохимический процесс, электролиз криолитоглинозёмного расплава подчиняется законам Фарадея, установленным им при изучении электролиза водных растворов. Первый закон. Масса вещества, выделившегося на электроде при прохождении постоянного электрического тока через электролит, прямо пропорциональна количеству затраченного электричества, т.е. силе тока и времени его прохождения: m = k * I * τ (1) Коэффициент пропорциональности k называют электрохимическим эквивалентом. Если подставить в уравнение I = 1А, τ = 1 час, то m = k, т.е. электрохимический эквивалент представляет собой массу вещества, выделившегося на электроде при силе тока 1А за 1 час. Значит, он измеряется в: г /(А*ч) или кг /(кА*ч) k = Второй закон Электрохимические эквивалентывеществ пропорциональны их грамм – эквивалентам: k = где Э - грамм – эквивалент выделившегося вещества на электроде; F – число Фарадея, равно 26,8 А*ч Грамм – эквивалент Э - это масса вещества в граммах, численно равная химическому эквиваленту Х Х = где Ам – атомная масса вещества; n – валентность вещества. Тогда, подставив в уравнение (3) значение Э = Х, получим: k = Отсюда, численные значения электрохимического эквивалента будут для: Al = 0,335 г/(А*ч) Mg = 0,454 г/(А*ч) Cl = 1,323 г/(А*ч) На практике количества металла, который выделяется при электролизе всегда меньше, чем должно было выделиться по закону Фарадея, для определения эффективности работы электролизера (тока) ввели показатель выход по току. Выходом по току η называют отношение массы вещества, фактически полученного при электролизе, к его количеству, теоретически ожидаемому за то же время, согласно закону Фарадея:
где Рпр -производительность электролизера т.е. количество алюминия, фактически наработанное определенным количеством электричества (I*τ); Рт - теоретическое количество алюминия, выделяемое тем же количеством электричества, по закону Фарадея. Производительность электролизера по закону Фарадея пропорционально силе тока, времени и выходу по току: Р = k * I * τ* ηт
Удельный расход электрической энергии является важным показателем работы электролизера, т.к. процесс электролиза является очень энерго затратным. Удельный расход энергии показывает затраты электрической энергии на выпуск единицы продукции (Вт*ч/ кг; кВт*ч/т) Удельный расход электроэнергии W, кВт*ч/т равен: W = где Uср – среднее напряжение на электролизере, В η т –выход по току, % Выход по энергии ηэ, г/(кВт*ч) величина обратная удельному расходу электроэнергии и показывает сколько грамм алюминия выделится при затратах 1 кВт*ч энергии, определяется
|
|||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 264; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.217.203.172 (0.006 с.) |
 (2)
(2) 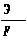 (3)
(3)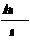 (4)
(4) (5)
(5)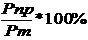 ηт =
ηт =