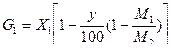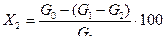Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: получение фенола и ацетона из изопропилбензола
Теоретические основы Фенол и ацетон являются важными продуктами органического синтеза, которые широко используются в народном хозяйстве. Особенно многообразны области применения фенола, а именно: производство синтетических смол, пластических масс, синтетического волокна, поверхностно-активных веществ, средств защиты растений, лекарственных препаратов и др. В настоящее время основным промышленным методом получения фенола является процесс окисления изопропилбензола в гидропероксид и разложение гидропероксида изолропилбензола на фенол и ацетон. Процесс производства фенола и ацетона включает три основные стадии: а) алкилирование бензола пропиленом в изопропилбензол
С6Н6+СН2=СНСН3
б) окисление изопропилбензола в гидропероксид
С6Н5-С(СН3)2+О2→С6Н5-С(СН3)2 | | Н ООН
в) разложение гидропероксида изопропилбензола в фенол и ацетон
С6Н5-С(СН3)2→С6Н5ОН+СН3-С-СН3 | || ООН О
Цель работы Изучение процессов окисления изопропилбензола в гидропероксид и разложения гидропероксида изопропилбензола в фенол и ацетон.
Окисление изопропилбензола в гидропероксид
В промышленности изопропилбензол окисляют в гидропероксид кислородом воздуха в тарельчатых колоннах непрерывного действия. Для устранения индукционного периода к изопропилбензолу, поступающему на окисление, добавляют до 1% гидропероксида и ведут окисление при 105—120°С и 0,4 МПа. Повышение температуры хотя и ускоряет процесс образования гидропероксида изопропилбензола, но одновременно приводит к усилению реакции его разложения, причем при температуре выше 120 °С реакция разложения может принять взрывной характер. Время реакции подбирают таким образом, чтобы глубина конверсии изопропилбензола не превышала 30—35%. В этом случае селективность процесса по гидропероксиду достигает ≈ 90%. Основными побочными продуктами процесса окисления являются ацетофенон и диметилфенилкарбинол, которые образуются в результате дальнейших превращений гидропероксида изопропилбензола и гидропероксидного радикала:
Поскольку процесс окисления протекает по радикально-цепному механизму, то изопропилбензол, поступающий на окисление, должен быть свободен от соединений серы, ненасыщенных углеводородов, фенола, стирола и других соединений, которые являются ингибиторами радикальных реакций. Внимание! На всех стадиях получения и разложения гидропероксида изопропилбензола строго соблюдать правила работы с гидропероксидными соединениями, так как они легко взрываются.
Методика выполнения работы
Реактивы Изопропилбензол 90,2 г (105 мл) Гидропероксид изопропилбензола 2 г Воздух или технический кислород (из баллона) Уксусная кислота ледяная 200 мл Иодид калия, 50%-ный водный раствор 50 мл Тиосульфат натрия, 0,1 н. водный раствор 700 мл Крахмал, водный раствор 40 мл Изопропилбензол окисляют в гидропероксид на установке, схема которой приведена на рисунке 13. Установка состоит из игольчатого вентиля 1 для регулирования подачи сжатого воздуха, трубки 2 с активированным углем, трубки 3 сбезводным хлоридом кальция, реометра 4 для измерения скорости подачи воздуха, предохранительной склянки 5, реактора 8, контактного термометра 9, обратного холодильника 10, сепаратора 11, реле-регулятора 14 и автотрансформатора 15. Перед началом опыта проверяют правильность сборки, герметичность всех соединений установки и надежность работы системы для поддержания в реакторе заданной температуры. Реактор изготовлен из термостойкого стекла (d =24 мм, h = 250 мм) и снабжен барботером 7 для подачи воздуха, отводной трубкой с краном 13 для отбора проб, электроспиралью 6 для нагрева реакционной массы. В сухой чистый реактор наливают 100 мл 3%-ного изопропилбензольного раствора гидропероксида изопропилбензола (или 100 мл изопропилбензола), 0,03 г стеарата кобальта и 0,03 г гидроксида кальция. Подают воду в обратный холодильник и включают обогрев реактора. По достижении в реакторе заданной температуры 115±0,5°С и стабилизации ее включают подачу воздуха со скоростью 800 мл/мин. Момент включения подачи воздуха принимают за начало опыта. В ходе опыта каждые 30 мин в колбы емкостью 100 мл с притертыми пробками, предварительно взвешенные на аналитических весах, отбирают две параллельные пробы по 1 мл для определения концентрации гидропероксида изопропилбензола в реакционной массе. Перед отбором проб отводную трубку с краном 13 продувают воздухом при помощи резиновой груши.
Рисунок 13 - Установка для окисления изопропилбензола в гидропероксид изопропилбензола: 1 - игольчатый вентиль; 2 — трубка с активированным углем; 3 — трубка с безводным хлоридом кальция; 4 — реометр; 5 — предохранительная склянка; 6 — электроспираль; 7 — барботер; 8 — реактор; 9 — контактный термометр; 10 — обратный холодильник; 11 — сепаратор; 12 — трехходовой кран; 13 — кран; 14 — реле-регулятор; 15 — автотрансформатор.
Окисление изопропилбензола заканчивают по достижении концентрации гидропероксида в реакционной массе, ≈20% (масс.). Продолжительность опыта 3—4 ч. По окончании опыта выключают подачу воздуха, обогрев реактора и сразу отсоединяют линию воздуха от реактора для предотвращения засасывания в нее реакционной массы. Реакционную массу после охлаждения выливают в предварительно взвешенную колбу емкостью 150 мл, определяют массу, состав и составляют материальный баланс опыта. Массу продуктов реакции G 1 в пересчете на изопропилбензол вычисляют по формуле:
Общую массу G 2 взятых на анализ проб (g i) в пересчете на изопропилбензол вычисляют по формуле:
Потери изопропилбензола рассчитывают по формуле:
где М1, M 2 — молекулярные массы изопропилбензола и гидропероксида изопропилбензола; gi — масса i -той пробы, г; yi — концентрация гидропероксида изопропилбензола в i -той пробе, % (масс.); п — число проб, взятых на анализ. На основании полученных данных строят график зависимости: концентрация гидропероксида изопропилбензола (в % масс.) — продолжительность реакции (в мин); формулируют свои выводы о выполненной работе.
Контрольные вопросы 1. Применение фенола и ацетона в промышленности. 2. Стадии производства фенола и ацетона. 3. Формула по определению массы продуктов реакции. 4. Для чего в лабораторную установку включена трубка с безводным хлоридом кальция?
Литература 1. Одабашян Г.В. Лабораторный практикум по химии ТООНХС. М., Химия, 1982, с. 111-119. 2. Воскресенский П.И. Техника лабораторных работ. 10-е изд. М.. Химия, 1973, 717 с.
Лабораторная работа №14
|
||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 442; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.69.143 (0.013 с.) |
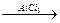 С6Н5СН(СН3)2
С6Н5СН(СН3)2