
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Использование реакций гидролиза
В качественном анализе Явление гидролиза широко используется в химическом анализе для различных целей. 1. Для подавления гидролиза, что позволяет получать устойчивые при хранении растворы. Для этой цели в растворы вводят тот продукт гидролиза, который является более сильным электролитом, при этом равновесие смещается влево, гидролиз уменьшается. Растворы солей, гидролизующихся по катиону (Fe3+, Al3+, Zn2+ и др.) подкисляют, а к растворам солей, гидролизующихся по аниону добавляют избыток щелочи. Например: раствор (NH4)2СО3 будет сохраняться дольше, если в приготовленный раствор добавить концентрированный раствор аммиака. В раствор сульфида аммония также вводят избыток аммиака. Для предотвращения гидролиза к водным растворам солей сурьмы и висмута всегда добавляется соответствующая кислота, вследствие чего эти растворы имеют кислую реакцию. Следовательно, если данный для анализа раствор не имеет осадка и рН = 7 (нейтральная среда), то это является первым признаком отсутствия катионов сурьмы и висмута. 2. Для обнаружения некоторых ионов, соли которых образуют при гидролизе нерастворимые соединения. Например: открытие ионов сурьмы и висмута проводят, разбавляя исследуемый раствор водой. Соль висмута, гидролизуясь по катиону, дает белый осадок оксо-висмутила BiOCl. Bi3+ + H2O Û BiOH2+ + H+ BiOH2+ + H2O Û Bi(OH)2+ + H+ Bi(OH)2+ Û BiO+ + H2O BiCl3 + H2O Û BiOCl↓ + 2HCl Явление гидролиза используется и при открытии ацетат-иона. Если к раствору ацетата натрия или калия прилить раствор хлорида железа (III), то появляется красно-бурое окрашивание вследствие образования выпадающей при нагревании в осадок основной соли Fe(OH)2CH3COO: Fe3+ + 3CH3COO- + 2H2O 3. Для разделения ионов. Например, для разделения ионов хрома Cr3+ и алюминия Al3+ к анализируемому раствору приливают избыток щелочи. При этом образуются растворимые в воде комплексные ионы [Al(OH)6]3- и [Cr(OH)6]3- Al3+ + 3OH- = Al(OH)3↓ Al(OH)3 + 3OH- = [Al(OH)6]3- После кипячения раствора комплексный ион алюминия остается в растворе, а ион, содержащий хром, гидролитически расщепляется с образованием осадка гидроксида хрома: [Cr(OH)6]3- При выполнении многих аналитических реакций необходимо учитывать возможность протекания реакций гидролиза, как самих реагентов, так и продуктов их взаимодействия. Например, при сливании растворов сульфата меди и карбоната натрия в результате ряда реакций гидролиза идет образование осадка основного карбоната меди (аналогичный пример разобран в §5)
Суммарное уравнение реакции имеет следующий вид: 2СuSO4 + 2Na2CO3 + H2O = Cu2(OH)2CO3↓ + CO2↑ + 2Na2SO4 При взаимодействии ионов Al3+, Cr3+ с сульфидом аммония (NH4)2S образуются осадки гидроксидов Al(OH)3, Cr(OH)3, а не осадки сульфидов этих металлов. Объясняется это тем, что сульфид аммония гидролизуется: NH4+ + S2- + H2O Û HS- + NH4OH Концентрация ионов ОН-, образующихся при диссоциации гидроксида аммония: NH4OH = NH4+ + ОН- оказывается достаточной для достижения произведения растворимости гидроксидов алюминия и хрома, результатом чего является выпадение в осадок гидроксидов Al(OH)3 и Cr(OH)3. Реакции, протекающие при сливании растворов соли хрома и сульфида аммония, можно записать в следующем виде: 6NH4+ + 3S2- + 3H2O = 3NH4OH + 3HS- + 3NН4+ Cr3+ + 3NH4OH = Cr(OH)3↓ + 3NН4+ ---------------------------------------------------------------- Cr3+ + 3S2- + 3H2O = Cr(OH)3↓ + 3HS- 3(NH4)2S + CrCl3 + 3H2O = Cr(OH)3↓ + 3NH4HS + 3NH4Cl Т.к. ионы HS- способны частично гидролизоваться дальше (2-я ступень) HS- + H2O = Н2S + ОН-, то возможна и вторая реакция: 2Cr3+ + 3S2- + 6H2O = 2Cr(OH)3↓ + 3H2S 2CrCl3 + 3(NH4)2S + 6H2O = 2Cr(OH)3↓ + 3H2S↑ + 6NH4Cl 4. Для усиления или ослабления кислотности или щелочности водного раствора. Например, для повышения щелочности добавляют ацетат или карбонат натрия, гидролизующиеся по уравнениям: СН3СОО- + Н2О Û СН3СООН + ОН- СО32- + Н2О Û НСО3- + ОН- c образованием свободного гидроксила (рН среды увеличивается). Так поступают при осаждении ионов бария в виде хромата BaCrO4, действуя бихроматом K2Cr2O7 в присутствии ацетата натрия. Образующийся при гидролизе ионы ОН-, связывают ионы водорода в молекулу воды:
2H2O 2СН3СОО- + 2Н2О Û 2СН3СООН + 2ОН- ------------------------------------------------------------------------------- 2Ba2+ + Cr2O72- + H2O + 2СН3СОО- Û 2BaCrO4↓ + 2СН3СООН Для повышения кислотности водных растворов к ним добавляют соли аммония сильных кислот, которые гидролизуясь дают ионы водорода (рН растворов понижается). Например, для снижения щелочности раствора алюмината, гидролизующегося с образованием свободных ОН-, к нему добавляют NH4Cl, связывающий ионы ОН- (накопление которых смещает равновесие влево и препятствует полному гидролизу алюмината) в слабый электролит NH4ОН:
3H2O 3NН4+ + 3H2O Û 3NH4OH + 3H+ ---------------------------------------------------------------- AlO33- + 3H2O + 3NН4+ Û Al(OH)3↓ + 3NH4OH Решение типовых задач Задача 1. Вычислить константу гидролиза Кгидр, степень гидролиза hгидр и рН 0,01 М раствора хлорида аммония при t = 25 оС. Решение. Запишем уравнение реакции гидролиза: NH4+ + H2O Û NH4ОН + H+ Для расчетов используем выведенные ранее соответствующие уравнения для солей, гидролизующихся по катиону:
Задача 2. Вычислить константу гидролиза hгидр и рН 0,01 М раствора ацетата калия при t = 25 оС. Решение. Запишем уравнение реакции гидролиза: СН3СОО- + Н2О ↔ СН3СООН + ОН- Для расчетов используем выведенные ранее соответствующие уравнения для солей, гидролизующихся по аниону:
Задача 3. Вычислить константу гидролиза hгидр и рН раствора цианида аммония. Решение. Запишем уравнение реакции гидролиза NH4CN: NH4+ + СN- + H2O Û HCN + NH4ОН Для расчетов используем выведенные ранее соответствующие уравнения для солей, гидролизующихся по аниону:
КHCN = 6,2·10-10, рКHCN = 9,21
hгидр + 0,96 hгидр = 0,96; hгидр ≈ 0,49 (49%);
рН = 7 + 1/2·9,21 – 1/2·4,76 = 7 + 4,605 – 2,38 ≈ 9,23. Задача 4. Вычислить константу гидролиза hгидр и рН 0,1 М раствора карбоната калия по 1- ой ступени. Решение. Запишем уравнение реакции гидролиза карбоната калия по 1-ой ступени. Соль гидролизуется по аниону: СО32- + Н2О Û НСО3- + ОН- Вычисления проводим по формулам, выведенным для бинарных солей, гидролизующихся по аниону:
Из таблицы 1 берется константа ионизации угольной кислоты по 2-ой ступени, т.к. гидролиз по первой ступени идет до иона НСО3-
рН = 7 + 1/2·10,32 – 1/2·lg10 -1 = 7 + 5,16 – 0,5 = 11,66.
4.11. Вопросы и задачи для самостоятельного решения 1. Что такое гидролиз? Какие из перечисленных солей будут подвергаться гидролизу: K2CO3, KCl, Li2SO3, Hg(NO3)2, MgCl2, Cr2(SO4)3, SbCl3, Zn(CH3COO)2, Bi(NO3)3, FeSO4? Укажите реакцию среды водных растворов указанных солей. 2. Как гидролизуются многозарядные ионы? Приведите примеры. 3. Могут ли гидролизоваться кислые и основные соли? От чего зависит реакция растворов таких солей? 4. Как изменяется степень гидролиза при разбавлении, при нагревании? Почему? 5. Можно ли в растворах солей, подвергающихся гидролизу, предотвратить гидролиз? Как это сделать? 6. При гидролизе каких солей рН раствора близка к 7? Почему это возможно? Приведите примеры. 7. В случае каких солей в растворах равной концентрации степень гидролиза будет больше: Cu(NO3)2 или Zn(NO3)2; NaCN или NaNO2? 8. Как сместиться равновесие гидролиза следующих солей: ZnSO4, KNO2, Al(OH)SO4 при добавлении к раствору HCl, KOH, NH4Cl? 9. Составьте молекулярные и ионные уравнения гидролиза солей: CH3COOK, Cr2(SO4)3, Al(NO3)3. Какое значение рН (больше или меньше 7) имеют растворы этих солей? 10. Какое значение рН (больше или меньше 7) имеют растворы солей: K2S, Al2(SO4)3, FeCl3, (NH4)2S? Составьте молекулярные и ионные уравнения гидролиза. 11. Составьте молекулярные и ионные уравнения гидролиза солей: (NH4)2СО3, Pb(NO3)2, Na2SO3, ZnSO4. Какое значение рН (больше или меньше 7) имеют растворы этих солей? 12. Составьте молекулярные и ионные уравнения гидролиза соли, раствор которой имеет: щелочную реакцию; кислую реакцию.
13. Составьте молекулярные и ионные уравнения реакций, происходящих при смешивании растворов сульфата алюминия и карбоната натрия. 14. Какие из солей – NaBr, Na2S, K2CO3, CoCl2, K2SO4 подвергаются гидролизу? Составьте молекулярные и ионные уравнения гидролиза соответствующих солей. 15. Какие из солей – NaNO3, CrCl3, Cu(NO3)2, KCl, KJ – подвергаются гидролизу? Составьте молекулярные и ионные уравнения гидролиза соответствующих солей. 16. Составьте молекулярные и ионные уравнения гидролиза, происходящего при смешивании растворов CrCl3 и Na2S (образуются Cr(OH)3 и H2S). 17. Какое значение рН (больше или меньше 7) имеют растворы следующих солей: MnCl2, K2CO3, Ni(NO3)2? Составьте молекулярные и ионные уравнения гидролиза. 18. Какие из солей – Na2SO4, AlCl3, MnSO4, KCl подвергаются гидролизу? Составьте молекулярные и ионные уравнения гидролиза соответствующих солей. 19. Выразите молекулярным и ионным уравнениями процесс, происходящий при смешивании концентрированных растворов FeCl3 и Na2CO3. 20. Какие из солей – NaJ, FeCl2, K2SO4, KNO3, Co(NO3)2 подвергаются гидролизу? Составьте молекулярные и ионные уравнения гидролиза соответствующих солей. 21. При смешивании растворов Al2(SO4)3 и Na2S образуются Al(OH)3 и H2S. Выразите этот гидролиз молекулярным и ионным уравнениями 22. Составьте молекулярное и ионное уравнения гидролиза соли, в результате которого образуется: кислая соль; основная соль. 23. В каких случаях при гидролизе соли образуется: кислая соль; основная соль? Ответ подтвердите соответствующими молекулярными и ионными уравнениями реакций. 24. Какое значение рН (больше или меньше 7) имеют растворы солей: NiSO4, K3PO4, NaOCl? Составьте молекулярные и ионные уравнения гидролиза. 25. Составьте молекулярные и ионные уравнения гидролиза солей: CuSO4, Na3PO4, Li2S. Какое значение рН (больше или меньше 7) имеют растворы этих солей? 26. Какие из солей: NaCl, Cr2(SO4)3, CuCl2, KBr, Zn(NO3)2 подвергаются гидролизу? Составьте молекулярные и ионные уравнения гидролиза соответствующих солей. 27. Составьте молекулярное и ионное уравнения реакций, происходящих при смещении растворов CuSO4 и Na2CO3. 28. Составьте молекулярные и ионные уравнения гидролиза солей: NiCl2, CH3COOK, FeSO4. Какое значение рН (больше или меньше 7) имеют растворы этих солей? 29. В растворе, какой соли при одинаковой концентрации и температуре реакция среды более кислая: NH4CN или NH4NO2? 30. От каких факторов зависит степень гидролиза солей?
31. Определите степень гидролиза и рН 0,02 М раствора нитрита калия. Ответ: 2,7·10-3 %; 7,85. 32. Вычислите степень гидролиза и рН в 0,18 М растворе бромида аммония. Ответ: 0,0055%; 5 33. Вычислите степень гидролиза раствора сульфида аммония (NH4)2S по первой ступени. Ответ: 99,86 % 34. Вычислите константы гидролиза следующих солей: NH4Cl, KCN, K2CO3 (по первой ступени), NaNO2. Какая из указанных солей гидролизуется сильнее других при прочих равных условиях? Ответ: 5,68·10-10; 2·10-5; 2,08·10-4; 1,45·10-11 35. Приведите примеры использования реакций гидролиза в анализе. 36. Вычислите степень гидролиза по первой ступени 0,5 М раствора сульфата цинка. Ответ: 0,36 %.
|
||||||||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 1202; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.30.253 (0.052 с.) |
 Fe(OH)2CH3COO↓ + 2CH3COOH↑
Fe(OH)2CH3COO↓ + 2CH3COOH↑ 2Ba2+ + Cr2O72- + H2O Û 2BaCrO4↓ + 2H+
2Ba2+ + Cr2O72- + H2O Û 2BaCrO4↓ + 2H+ AlO33- + 3H2O Û Al(OH)3↓ + 3ОН-
AlO33- + 3H2O Û Al(OH)3↓ + 3ОН-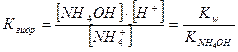 ;
;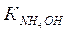 = 1,76·10-5 (рК = 4,75) (см. табл.1)
= 1,76·10-5 (рК = 4,75) (см. табл.1)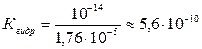
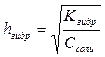 ;
; 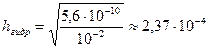 (2,37·10-2 %)
(2,37·10-2 %)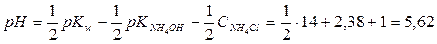 ;
;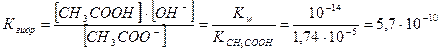 ;
;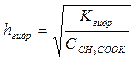 ;
; 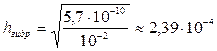 (2,39·10-2 %)
(2,39·10-2 %)
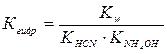
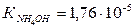 , рК
, рК 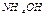 = 4,76
= 4,76
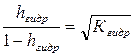 ;
; 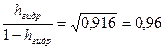 ;
; ;
;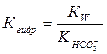 ; К
; К 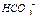 = 4,8·10-11; рК = 10,32.
= 4,8·10-11; рК = 10,32.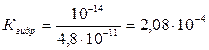 ;
;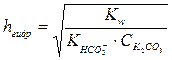
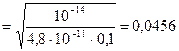 (4,56%)
(4,56%)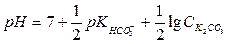 ;
;


