
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Комплексные соединения, их состав и строение
Комплексными соединениями называют определенные молекулярные соединения, при сочетании компонентов которых образуются положительно или отрицательно заряженные ионы, способные существовать как в кристалле, так и в растворе. (Гринберг А.А.) Первые представления о комплексных соединениях возникли в конце 19 века на основе координационной теории Вернера (предложена в 1893 г.), которая обобщила многочисленные результаты исследований явления комплексообразования. Комплексные соединения имеют «центральное строение». В центре стоит ион комплексообразователь, который называют центральным атомом или ионом. В непосредственной близости к нему располагаются ионы или молекулы (заместители, лиганды*, адденды**), образующие внутреннюю координационную сферу комплексного соединения. Комплексообразователь характеризуют координационным числом, а лиганды – дентатностью. Число групп, непосредственно связанных с центральным атомом, называют координационным числом. Дентатность*** - это способность лигандов к образованию координационной связи. Например: монодентатные лиганды (образуют одну связь): CN-, F-, Cl-, NH3, CO, H2O и др.; полидентатные (две и более связей): PO В настоящее время принято обозначать внутреннюю сферу термином комплекс и при написании формул заключать в квадратные скобки. Если комплексное соединение носит ионный характер, то у него есть внешняя сфера, образованная ионами, имеющими знак заряда, противоположный знаку заряда внутренней сферы. Разница между ионами внутренней и внешней сферы существенна. Связь центрального атома с лигандами осуществляется по донорно-акцепторному механизму, а ионы внешней сферы удерживаются за счет сил электростатического притяжения. В настоящее время для описания электронной структуры комплексных соединений, их строения, устойчивости, физических и химических свойств используют различные теоретические подходы, в том числе, в основном, теорию валентных связей, теорию кристаллического поля и теорию молекулярных орбиталей. Наиболее просто и, вместе с тем, достаточно обоснованно образование комплексных соединений, широко используемых в аналитической химии, можно объяснить с позиций теории валентных связей. Например, образование аммиакатов можно рассматривать как образование комплексных ионов [NH4]+. Этот процесс осуществляется за счет неподеленной пары электронов атома азота в молекуле аммиака, при этом атом азота – донор электронов, а ион водорода – акцептор электронов.
В общем случае донорно-акцепторные координационные гибридные связи образуются за счет неподеленных пар электронов лигандов и свободных орбиталей ионов комплексообразователей. Лиганд играет роль донора, а комплексообразователь – роль акцептора электронов. Координационные связи возникают при перекрывании вакантных орбиталей центрального атома заполненными орбиталями лигандов. Тип гибридизации и строение комплексных ионов в основном определяются электронной конфигурацией центрального атома и природой лигандов. Рассмотрим образование комплексного иона [Cu(NH3)4]2+. Для этого запишем электронные конфигурации* атома меди, иона меди (II) и образующегося комплексного иона:
Четыре пары неподеленных электронов азота (донор) в 4-х молекулах аммиака дают 4 координационные связи и образуется комплексный ион:
4 пары электронов Для иона [Cu(NH3)4]2+ характерна sp3 гибридизация, он имеет структуру плоского квадрата. Приведем еще несколько примеров различной гибридизации при образовании комплексных ионов. Запишем электронную формулу иона Ni2+ и комплексного иона [Ni(NH3)6]2+:
6 пар электронов для него характерна sp3d2 гибридизация и октаэдрическое строение.
В комплексном ионе [Со(NH3)6]3+ орбитали гибридизованы по типу sp3d2. Электронные конфигурации атома, иона Со3+ и комплексного иона [Со(NH3)6]3+ запишутся:
Гибридизация идет за счет внутренних 3d – орбиталей. Особенно устойчивы комплексы, в которых 4, 8, 12 или 16 связывающих электронов (координационные числа – 2, 4, 6 и 8). К ним относятся и комплексы с d2sp3 гибридизацией. Примером может служить комплексный ион [Fe(CN)6]4-. Разберем электронный механизм его образования. Атом железа имеет электронную формулу – 1s22s22p63s23p63d64s2. В гексацианоферрат (II) – ионе электронная оболочка центрального иона имеет 24 электрона (Fe2+, 26 – 2 = 24 электрона):
Ион Fe2+ имеет 4 незаполненных 3d орбитали, при возбуждении электроны спариваются и три 3d орбитали оказываются заполненными полностью, а две 3d орбитали освобождаются. Шесть лигандов CN- за счет шести неподеленных пар электронов атомов углерода (донор) предоставляют 12 электронов для образования 6 донорно-акцепторных (координативных) связей. При этом атом железа приобретает устойчивую электронную конфигурацию криптона (24 + 12 = 36 электронов). Электронная формула комплексного иона запишется:
6 пар электронов Подобным образом можно представить строение и других комплексных соединений. Теория валентных связей, хотя и не дает достаточно полного объяснения природы координационной связи, все-таки позволяет предвидеть возможность замены одних лигандов в комплексном ионе другими, т.е. целенаправленно проводить процессы образования и разрушения комплексов, используемых в аналитической практике.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 730; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.86.134 (0.01 с.) |
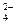 , C2O
, C2O  и др. Комплексы, образованные полидентатными лигандами, называют хелатами, внутрикомплексными соединениями.
и др. Комплексы, образованные полидентатными лигандами, называют хелатами, внутрикомплексными соединениями.






