
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Факторы, влияющие на степень гидролиза солей
Степень гидролиза – hгидр – дает количественную характеристику способности солей вступать в реакции гидролиза. Она зависит от природы гидролизующейся соли (чем меньше степень электролитической диссоциации образующегося при гидролизе электролита, тем сильнее идет гидролиз, табл. IV.1); от концентрации соли (при разбавлении раствора степень гидролиза увеличивается для солей, гидролизующихся по Kt+ или по An- и не зависит для солей, гидролизующихся одновременно и по Kt+ и по An-); от температуры (с повышением температуры степень гидролиза увеличивается). Все эти закономерности хорошо иллюстрируются формулами, позволяющими вычислить степень гидролиза - hгидр (вывод формул дан выше в §6):
Приведем несколько примеров. Степень гидролиза цианистого калия – KCN (hгидр = 1,2·10-2) выше, чем степень гидролиза ацетата натрия – CH3COONa (hгидр = 7,0·10-3), т.к. синильная кислота – более слабый электролит, чем уксусная, - константа ионизации синильной кислоты меньше, чем уксусной (КHCN = 7,0·10-10; К При повышении температуры степень гидролиза увеличивается, т.к. реакции гидролиза протекают с поглощением тепла (эндотермичны) и в соответствии с принципом Ле-Шателье повышение температуры раствора смещает равновесие в сторону образования продуктов гидролиза. Кроме этого, при повышении температуры константа диссоциации воды возрастает значительно сильнее, чем константы диссоциации продуктов гидролиза. Сочетание нескольких факторов дает возможность значительно усилить процесс гидролиза. Например, в холодных концентрированных растворах сульфата алюминия гидролиз практически идет по первой ступени до AlOH2+. При нагревании разбавленного раствора становится возможной и вторая ступень гидролиза до Al(OH)2+. При добавлении по каплям раствора соли хлорида железа (III) к кипящей воде возможна и третья ступень гидролиза, т.к. при значительном нагревании улетучивается хлороводород и равновесие реакции смещается в сторону образования продуктов гидролиза. Повышение температуры еще более усиливает гидролиз, если он идет по катиону и по аниону, особенно для многозарядных ионов. Например, ацетат алюминия при 20оС гидролизуется до иона AlOH2+, а при нагревании до Al(OH)2+, образуется осадок дигидроксоацетата алюминия, и процесс становится практически необратимым, т.к. оба продукта гидролиза покидают сферу взаимодействия (CH3COOН при нагревании улетучивается в виде газа):
Al(CH3COO)3 + Н2О Û AlОН(CH3COO)2 + CH3COOН AlОН(CH3COO)2 + Н2О
|
|||||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 820; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.161.116 (0.004 с.) |
 (по Kt+) (IV.7)
(по Kt+) (IV.7) (по Аn-) (IV.21)
(по Аn-) (IV.21) (по Kt+ и Аn-) (IV.27)
(по Kt+ и Аn-) (IV.27) = 1,8·10-5). При 25оС в 0,1 М растворе карбоната натрия hгидр = 3%, а в 0,001 М растворе hгидр = 35%.
= 1,8·10-5). При 25оС в 0,1 М растворе карбоната натрия hгидр = 3%, а в 0,001 М растворе hгидр = 35%.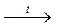 Al(ОН)2CH3COO↓ + CH3COOН↑
Al(ОН)2CH3COO↓ + CH3COOН↑


