
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Высшие оксиды и гидроксиды химических элементов III периода. Закономерности в изменении их свойств в связи с положением химических элементов в периодической системе.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Характер оксида и гидроксида зависит от атома который его образует. Металлы со степенью окисления +1 и +2 образуют основные оксиды и основания, со степенью окисления +3 – амфотерные оксиды и гидроксиды. Атомы неметаллов со степенью окисления +4, +5, +6, +7 образуют кислотные оксиды и кислоты. Чем больше степень окисления, тем сильнее кислота.
Вывод: в периоде с увеличением числа электронов на внешней оболочке атома свойства оксидов и гидроксидов изменяются от основных через амфотерные к кислотным.
Билет №13 (2) Жиры, их состав, свойства. Понятие о синтетических моющих средствах. Защита природы от загрязнения синтетических моющих средств. 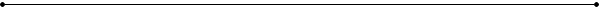 Жиры – сложные эфиры трёхатомного спирта глицерина и различных карбоновых кислот.
,где R1, R2, и R3 – одинаковые или различные углеводородные радикалы карбоновых кислот.
Жиры наряду с углеводами и белками входят в состав организмов животных и растений. Они являются составной частью пищи человека и животных. При расщеплении жиров выделяется большое количество энергии. Основным свойством жиров является гидролиз, который в организме человека происходит под действием ферментов. Глицерин и карбоновые кислоты либо подвергаются дальнейшему окислению (до СО2), либо расходуются на формирование собственных жиров организма (реакция обратная гидролизу) Жидкие и твёрдые мыла являются продуктом технической переработки. Один из видов синтетических моющих средств (СМС) – натриевые соли сложных эфиров высших спиртов и серной кислоты R−CH2−OSO3−Na+. Имея полярный и неполярный (R) концы, молекулы натурального мыла и СМС растворяются в воде и обеспечивают моющий эффект. СМС обладают высокими моющими свойствами в любой воде, однако, их попадание в почву и водоёмы наносит значительный экологический урон, так как они разлагаются очень медленно. Предотвращение слива неочищенных от СМС сточных вод и создание более экологически безопасных СМС – путь к сохранению окружающей природы.
Билет №14 (1) Кислоты, их классификация и свойства на основе представлений об электролитической диссоциации, практическое применение.  Кислоты – сложные вещества состоящие из атомов водорода и кислотных остатков: H 2SO4, H Cl, H NO3, CH3COO H. Кислоты – электролиты, при диссоциации которых в качестве катионов образуется только катион водорода. HCl ⇄ H+ + Cl–; H2SO4 ⇄ 2H+ + SO42– Классификация:
Химические свойства: 1) Изменяют окраску индикаторов: HNO3 ⇄ H+ + NO3– 2) Реагируют с основаниями: а) HNO3 + NaOH → NaNO3 + H2O H+ + NO3– + Na+ + OH– → Na+ + NO3– + H2O H+ + OH– → H2O б) 2HNO3 + Cu(OH)2 → Cu(NO3)2 + 2H2O Cu(OH)2 + 2H+ → Cu2+ + 2H2O 3) С основными оксидами: CuO + 2HCl → CuCl2 + H2O CuO + 2H+ → Cu2+ + H2O 4) С солями: H2SO4 + BaCl2 → BaSO4 + 2HCl SO42– + Ba2+ → BaSO4 5) С металлами (левее водорода): 2HCl + Fe → FeCl2 + H2↑
Практическое значение: В химической промышленности: 1) H2SO4 – уровень развития химической промышленности; 2) красители; 3) минеральные удобрения; 4) очистка нефтепродуктов; 5) получение взрывчатых веществ (H2SO4 и HNO3), получение искусственного шёлка (ацетаты), глюкозы, сахарозы, солей и др. Билет №14 (2)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 1586; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.73 (0.006 с.) |





