Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Окислительные свойства простых веществ неметаллов
Окислительные свойства неметаллов проявляются в первую очередь при их взаимодействии с металлами (как вы знаете, металлы всегда восстановители):
2.Окислительные свойства хлора Cl2 выражены сильнее, чем у серы, поэтому и металл Fe, который имеет в соединениях устойчивые степени окисления +2 и +3, окисляется им до более высокой степени окисления.
3.Большинство неметаллов проявляют окислительные свойства при взаимодействии с водородом. В результате образуются летучие водородные соединения.
4 Любой неметалл выступает в роли окислителя в реакциях с теми неметаллами, которые имеют более низкое значение электроотрицательности
5.Электроотрицательность серы больше, чем у фосфора, поэтому она здесь проявляет окислительные свойства.
95
6.Электроотрицательность фтора больше, чем у всех остальных химических элементов, поэтому он проявляет свойства окислителя. 7.Фтор F2 – самый сильный окислитель из неметаллов, проявляет в реакциях только окислительные свойства. 8.Окислительные свойства неметаллы проявляют и в реакциях с некоторыми сложными веществами. Отметим в первую очередь окислительные свойства неметалла кислорода в реакциях со сложными веществами: a)
Восстановительные свойства простых веществ – неметаллов В зависимости от значений их электроотрицательности один из них проявляет свойства окислителя, а другой – свойства восстановителя. 1. По отношению к фтору все неметаллы (даже кислород) проявляют восстановительные свойства. 2. Разумеется, неметаллы, кроме фтора, служат восстановителями при взаимодействии с кислородом:
3. В результате реакций образуются оксиды неметаллов: несолеобразующие и солеобразующие кислотные. И хотя галогены непосредственно с кислородом не соединяются, известны их оксиды , 4.Многие неметаллы могут выступать в роли восстановителя в реакциях со сложными веществами-окислителями:
а)
Высшие оксиды неметаллов. Водородные соединения. Высшие оксиды неметаллов.
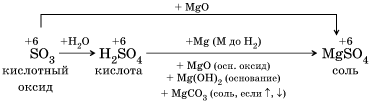
В оксидах неметаллов связь между атомами ковалентная полярная. Среди оксидов молекулярного строения есть газообразные СО2, SO2, N2O, CO, NO и др., жидкие (летучие) SO3, N2O3, твердые (летучие) P2O5, N2O5, SeO2. Твердый, очень тугоплавкий оксид SiO2 – вещество с атомной кристаллической решеткой. Оксиды неметаллов делят на две группы: несолеобразующие и coлеобразующие. К несолеобразующим оксидам относятся SiO, N2O, NO, NO2, CO. Все остальные оксиды неметаллов являются солеобразующими, кислотными. При растворении их в воде образуются гидраты оксидов – гидроксиды, по своему характеру являющиеся кислотами. Кислоты и кислотные оксиды в результате химических реакций образуют соли, в которых неметалл сохраняет степень окисления. Например:
Кислотный оксид SiO2 нерастворим в воде, но ему также соответствует гидрат в виде кислоты Н2SiO3 и соли:
Оксиды и соответствующие им гидроксиды – кислоты, в которых неметалл проявляет степень окисления, равную номеру группы, то есть высшее ее значение, называют высшими. При рассмотрении Периодического закона мы уже характеризовали их состав и свойства, например:
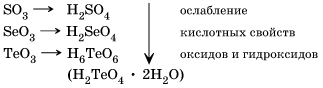
В пределах одной главной подгруппы, например, VI группы действует следующая закономерность изменения свойств высших оксидов и гидроксидов:
Если неметалл образует два или более кислотных оксидов, а значит, и соответствующих кислородсодержащих кислот, то их кислотные свойства усиливаются с увеличением степени окисления неметалла.
Оксиды и кислоты, в которых неметалл имеет высшую степень окисления, могут проявлять только окислительные свойства.
Особенности сильнейших окислителей Оксиды и кислоты, где неметалл имеет промежуточную степень окисления, могут проявлять и окислительные, и восстановительные свойства. 1. а) б) 2. а) б)
Водородные соединения. Общим свойством всех неметаллов является образование летучих водородных соединений, в большинстве которых неметалл имеет низшую степень окисления.
Среди приведенных формул веществ много тех, свойства, применение и получение которых вы изучали ранее: СН4, NH3, H2O, H2S, HCl.
Известно, что наиболее просто эти соединения можно получить непосредственно взаимодействием неметалла с водородом, то есть синтезом: Все водородные соединения неметаллов образованы ковалентными полярными связями, имеют молекулярное строение и при обычных условиях являются газами, кроме воды (жидкость). Для водородных соединений неметаллов характерно различное отношение к воде. Метан и силан в ней практически нерастворимы. Аммиак при растворении в воде образует слабое основание – гидрат аммиака NH3 ∙ H2O. При растворении в воде сероводорода, селеноводорода, теллуроводорода, а также галогеноводородов образуются кислоты с той же формулой, что и сами водородные соединения: H2S, Н2Se, H2Те, HF, HCl, НВr, HI.
Если сравнить кислотно-основные свойства водородных соединений, образованных неметаллами одного периода, например второго (NH3, H2O, HF) или третьего (PH3, H2S, HCl), то можно сделать вывод о закономерном усилении их кислотных свойств и соответственно ослаблении основных. Это, очевидно, связано с тем, что увеличивается полярность связи Э — Н (где Э – неметалл). Кислотно-основные свойства водородных соединений неметаллов одной подгруппы также отличаются. Например, в ряду галогеноводородов HF, HCl, HBr, HI прочность связи Э — Н уменьшается, так как увеличивается длина связи. В растворах НСl, HBr, HI диссоциируют практически полностью – это сильные кислоты, причем их сила увеличивается от HF к HI. При этом HF относится к слабым кислотам, что обусловлено еще одним фактором – межмолекулярным взаимодействием, образованием водородных связей... Н—F... Н—F... Атомы водорода связаны с атомами фтора F не только своей молекулы, но еще и соседней. Обобщая сравнительную характеристику кислотно-основных свойств водородных соединений неметаллов, сделаем вывод об усилении кислотных и ослаблении основных свойств этих веществ по периодам и главным подгруппам с увеличением атомных номеров образующих их элементов.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-01-22; просмотров: 30; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.12.205 (0.019 с.) |
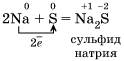


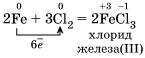
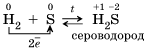
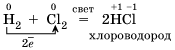
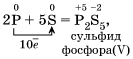







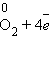

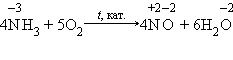
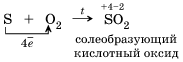

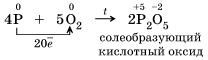
 ,
, 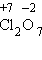 ,
, 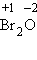 ,
, 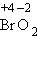 , и др., которые получают косвенным путем.
, и др., которые получают косвенным путем.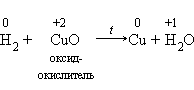
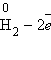



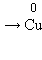
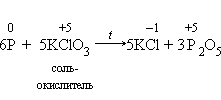
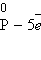



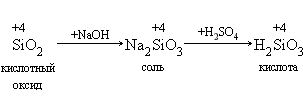


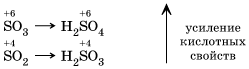

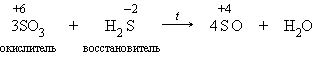
 и
и 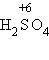 (конц.) проявляются в реакциях с металлами, неметаллами, органическими веществами.
(конц.) проявляются в реакциях с металлами, неметаллами, органическими веществами.