Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Механизмы возникновения и следствия диареи
Диарея – увеличение массы стула свыше 250 граммов в сутки, причем содержание воды в стуле при этом превышает 60-85%. В том случае, если масса стула не более 250 граммов в сутки, но возрастает количество дефекаций, принято говорить о гипердефекации или псевдодиарее. Классификация диареи По механизму возникновения диареи различают следующие виды: 1. Осмотическая 2. Секреторная 3. Экссудативная 4. Диарея, связанная с нарушением моторной функции кишечника По причине, её вызвавшей, диарея может быть инфекционной и неинфекционной. В зависимости от продолжительности диареи, она может быть острой (длительность её не превышает 2 – 3 недели) и хронической (в этом случае её продолжительность составляет 4 – 6 недель и больше).
Осмотическая диарея Она является следствием увеличения содержания в просвете кишечника электролитов, вслед за которыми по градиенту концентрации устремляется вода. Этот механизм диареи наблюдается при: ü Приёме слабительных препаратов (например, солевых слабительных), а так же антацидных препаратов, содержащих Mg 2+; ü Употреблении в пищу продуктов с высоким содержанием в них ксилита, сорбитола, маннитола (ксилит и сорбитол содержатся в жевательных резинках); ü Приёме некоторых лекарственных препаратов (лактулозы, холестирамина, неомицина и др.); ü Наследственном дефиците дисахаридаз (лактазы, сахаразы – изомальтазы, трегалазы). В результате дефицита и/ или нарушения активности этих ферментов нарушается расщепление нереабсорбируемых из просвета кишечника дисахаридов до моносахаридов, способных к всасыванию. При этом реабсорбция воды из просвета кишечника замедляется, и возникает диарея. ü Нарушении всасывания в кишечнике глюкозы, галактозы или фруктозы; ü Целиакии (глютеновой энтеропатии); ü Недостаточности экзокринной функции поджелудочной железы. Механизм возникновения осмотической диареи при этом следующий: недостаточное образование ферментов, участвующих в переваривании углеводов и жиров, приводит к тому, что эти вещества, достигая толстого кишечника, гидролизуются кишечной микрофлорой до органических соединений с невысокой молекулярной массой. Количество этих веществ значительно превышает возможности слизистой оболочки толстого кишечника к их абсорбции. Увеличение осмолярности содержимого толстого кишечника приводит к диарее.
Важной особенностью осмотической диареи является её прекращение в течение 2- 3 суток после голодания. Секреторная диарея Эта разновидность диареи возникает в результате значительного повышения секреторной функции эпителиоцитов слизистой оболочки кишечника. Секреторная диарея может быть неинфекционной и инфекционной. Неинфекционная секреторная диарея наблюдается при приёме некоторых слабительных препаратов (сенны, касторового масла, фенолфталеина, бисакодила, и др.); некоторых других лекарственных препаратов (холиномиметиков, ингибиторов холинэстеразы, тиазидных диуретиков и др.); интоксикациях (солями мышьяка, токсинами некоторых грибов и др.). Гормонопродуцирующие опухоли, характеризующиеся избыточной продукцией стимуляторов секреции, также приводят к секреторной диарее. Стимуляторами кишечной секреции являются: вазоинтестинальный пептид (ВИП), ацетилхолин, субстанция Р, серотонин, нейротензин, гистамин, брадикинин, аденозин, эндотелин-1 и др. Рассмотрим некоторые заболевания, обусловленные гиперпродукцией стимуляторов кишечной секреции. ВИПома, или панкреатическая холера – заболевание, обусловленное опухолью клеток поджелудочной железы, вырабатывающих ВИП. Он стимулирует аденилатциклазу эпителиоцитов слизистой оболочки кишечника. В этих клетках увеличивается содержание цАМФ, который вызывает потери со стулом Na+, K+ и воды. При этой форме патологии наблюдаются тяжелая водянистая диарея, гипокалиемия и гипохлоргидрия желудочного сока. Гипохлоргидрия развивается потому, что ВИП ингибирует секрецию соляной кислоты в желудке. Синдром Золлингера – Эллисона (гастринома). Гастринома – опухоль, субстратом которой являются клетки, продуцирующие гастрин. Эта опухоль чаще располагается в поджелудочной железе, реже – в 12-перстной кишке. Гастрин стимулирует продукцию соляной кислоты в желудке. Это приводит, во-первых, к развитию язвенной болезни, и, во-вторых, к возникновению диареи. Диарея при этом заболевании обусловлена тем, что гиперхлоргидрия желудочного сока вызывает закисление содержимого тонкого кишечника. В условиях низких значений рН снижается активность ферментов поджелудочной железы, поступающих в просвет тонкого кишечника. Желчные кислоты преципитируются, и возникает синдром мальабсорбции. Увеличивается секреция воды и солей в просвет кишечника.
Карциноидный синдром. Карциноидные опухоли, часто поражающие кишечник и бронхи, могут сопровождаться диареей. Её вызывают избыточные количества серотонина, брадикинина, субстанции Р и гистамина, которые образуются клетками этих опухолей. Медуллярная карцинома щитовидной железы. Клетки этой опухоли секретируют кальциотонин и простагландины, стимулирующие секрецию солей и воды энтероцитами. В настоящее время известно две редко встречающиеся формы наследственной диареи, при которых нарушена абсорбция жидкости из просвета кишечника. Обе эти формы патологии наследуются по аутосомно-рециссивному типу. Наследственная хлоридная диарея возникает в результате мутации гена, ответственного за синтез белка щёточной каемки энтероцитов, осуществляющего Cl-/HCO3- обмен. При этом увеличиваются потери ионов хлора со стулом, рН стула смещается в кислую сторону, а у пациентов часто развивается метаболический алкалоз. Наследственная хлоридная диарея относительно часто встречается в Финляндии, Саудовской Аравии, Кувейте, и реже – в Польше. Наследственная диарея с повышенной секрецией Na + - следствие мутации гена, кодирующего образования белка щеточной каемки энтероцитов, который обменивает ионы Na+ на протоны Н+. Обе эти формы наследственной диареи проявляются ещё у плода, а у беременной женщины обнаруживают многоводие. Классическим примером заболевания, при котором возникает секреторная инфекционная диарея, является холера. Энтеротоксин Vibrio cholerae состоит из двух субъединиц: А и В. В-субъединицы очень прочно связываются с компонентами щёточной каёмки энтероцитов, а субъединица А ковалентно связывается с a-субъединицей G-протеина, стимулирующего аденилатциклазу. Увеличение образования цАМФ в энтероцитах приводит к повышению секреции ионов Na+. Вслед за Na+ по законам осмоса в просвет кишечника устремляется вода. В содержимом кишечника также возрастает концентрация анионов Cl- и HCO3-. В плазме же крови концентрация Na+, Cl- и HCO3- падает. Диарея при холере выраженная, объём секретируемой жидкости может достигать 10 л/сут, что приводит к гипогидратации, нарушениям электролитного баланса и кислотно-основного равновесия крови. Секреторная инфекционная диарея также встречается при инфицировании человека токсигенными штаммами E. с oli. Эти микроорганизмы образуют два вида энтеротоксинов, вызывающих диарею. Один из них, термолабильный энтеротоксин, активирует аденилатциклазу в энтероцитах, что приводит к увеличению секреции этими клетками ионов Na+, Cl- и HCO3-. Второй, термостабильный энтеротоксин, повышает активность гуанилатциклазы в клетках кишечного эпителия. В результате еще больше возрастает секреция Cl- и HCO3- в просвет кишечника. Попадание некоторых других микроорганизмов в просвет кишечника (Helicobacter jejuni, Yersinia enterocolitica, Clostridium difficile, Staphylococcus aureus и др.) является еще одной частой причиной секреторной диареи.
Экссудативная диарея Возникновение этой разновидности диареи обусловлено повреждением эпителиальных клеток кишечника и утратой плотных межклеточных контактов между соседними энтероцитами под действием патогенного фактора. При этом из кровеносных и лимфатических сосудов в просвет кишечника начинают усиленно проникать вода, электролиты, белки и иногда – эритроциты и лейкоциты. По этиологии экссудативная диарея может быть инфекционной и неинфекционной. Инфекционную диарею вызывают патогенные штаммы Shigella, Salmonella, Yersinia, Escherichia, Aeromonas и др., а также некоторые вирусы (ротавирусы, аденовирусы, ВИЧ и др.) и простейшие (амебы). Неинфекционная экссудативная диарея часто встречается у пациентов, страдающих неспецифическим язвенным колитом. Отличительным признаком экссудативной диареи является присутствие в каловых массах примеси крови и высокое содержание полиморфноядерных нейтрофилов.
Диарея, развивающаяся в результате нарушений моторной функции кишечника Как усиление моторики кишечника, так и ее ослабление могут приводить к диарее. Одним из примеров диареи, развивающейся в результате повышения моторной функции кишечника, является диарея при некоторых разновидностях синдрома раздраженного кишечника. У некоторых таких пациентов миоэлектрическая активность толстого кишечника снижена, зато имеет место дисбаланс нейротрансмиттеров и гиперчувствительность слизистой оболочки толстого кишечника. Это приводит к ускорению пассажа кишечного содержимого и частым дефекациям. Поэтому у таких больных часто отмечается не истинная диарея, а псевдодиарея. Усиленная моторика кишечника также является одним из звеньев патогенеза демпинг-синдрома, развивающегося после удаления желудка или его частей и создании желудочно-кишечных анастомозов. При этом синдроме нарушаются процессы перемешивания пищи, и большое количество химуса поступает в кишечник. Выделение большого количества веществ, стимулирующих моторную и секреторную функции кишечника, спсообствует возникновению диареи в течение первого часа после приема пищи. Ускорение прохождения пищи по кишечнику наблюдается и при гипертирозе, особенно при тиротоксикозе. При этом уменьшается продолжительность переваривания и всасывания жиров, что приводит к диарее и стеаторее. Диарея прекращается при нормализации функции щитовидной железы.
Снижение моторной функции кишечника у больных с диабетической полинейропатией, системными заболеваниями соединительной ткани (например, склеродермией, дерматомиозитом), и у пациентов с дивертикулами кишечника также может вызывать диарею. Рассмотрим подробнее механизм ее возникновения при диабетической полинейропатии: некорригируемый (или плохо корригируемый) сахарный диабет ® диабетическая полинейропатия ® дегенерация адренергических нервных окончаний в стенке кишечника ® снижение моторной функции кишечника ® рост патогенной кишечной микрофлоры и колонизация ею верхних отделов толстого и части тонкого кишечника ® деконъюгация и дегидроксилирование патогенной микрофлорой желчных кислот ® уменьшение концентрации в просвете кишечника солей желчных кислот ® нарушение переваривания жиров ® гидроксилирование жиров микрофлорой кишечника с превращением их в амфифильные соединения ® стимуляция секреции кишечными энтероцитами солей и воды ® диарея.
Следствия диареи Выраженная диарея может приводить к гиповолемии, гипо- и дегидратации, нарушениям электролитного баланса и кислотно-основного равновесия крови. Особенно опасна диарея у новорожденных и детей 1-го года жизни, так как обезвоживание у них развивается особенно быстро и вызывает развитие дегидратационного шока, ДВС-синдрома и полиорганной недостаточности. Гибель может наступить от нарушений сердечной деятельности.
Принципы лечения диареи Принципы лечения диареи заключаются в следующем: 1. Лечение начинается после установления причины диареи и основного механизма ее развития. 2. При неинфекционной диарее необходимо лечение основного заболевания, приведшего к ее появлению. 3. При секреторной диарее патогенетически обоснованным является перроральная регидратация, а при невозможности ее выполнения или ее неэффективности осуществляется инфузионная терапия. Целесообразность перроральной регидратации при секреторной диарее объясняется тем, что при этом виде диареи абсорбционная способность энтероцитов, как правило, не нарушена. Растворы для перроральной регидратации, помимо электролитов в изоосмотических концентрациях, должны содержать глюкозу из-за наличия механизмов ее Na+-зависимого транспорта из просвета кишечника в энтероциты. При секреторной диарее также могут использоваться ингибиторы энкефалиназы – фермента, деградирующего энкефалины. В результате их применения в слизистой оболочке кишечника увеличивается содержание энкефалинов, которые обладают антисекреторным действием. 4. При выраженной диарее, вызванной бактериями или простейшими, проводится этиотропная терапия, т.е. назначаются антибиотики или антибактериальные препараты. 5. Диарея, возникающая в результате усиления моторной функции кишечника, требует назначения препаратов, угнетающих ее. Одним из таких препаратов является лоперамид (имодиум).
6. В том случае, если диарея обусловлена гормон-продуцирующей опухолью, необходимо ее удаление. При невозможности оперативного лечения таким пациентам назначают препарат октреотид – аналог соматостатина. Он предотвращает избыточное образование гормоноподобных веществ клетками опухоли и тем самым подавляет секреторную активность энтероцитов. 7. В настоящее время разработаны принципиально новые классы антидиарейных препаратов, которые проходят различные стадии испытаний. К таким препаратам относятся блокаторы анионных каналов энтероцитов и антагонисты цАМФ-зависимых калиевых каналов. По предварительным данным, оба класса этих препаратов эффективно подавляют механизмы возникновения секреторной диареи.
СИНДРОМ РАЗДРАЖЕННОГО КИШЕЧНИКА
Термин «синдром раздраженного кишечника появился сравнительно недавно, несмотря на то, что клинические проявления этого синдрома известны уже несколько веков. В 1849 г. английский врач Cumming так описывал синдром раздраженного кишечника: «… больного в одно время беспокоят запоры, в другое время этого же больного слабит. Как эта болезнь одновременно проявляется такими разными симптомами, я объяснить не в состоянии». Синдром раздраженного кишечника представляет собой самое распространенное функциональное расстройство кишечника, не связанное со структурными поражениями его слизистой оболочки или других органов ЖКТ. Частота встречаемости этого расстройства в общей популяции составляет не менее 10%, причем женщины страдают им примерно в 3 раза чаще, чем мужчины. В зависимости от преобладания тех или иных признаков выделяют следующие формы этого синдрома: 1. Болевой вариант 2. С преобладанием диареи 3. С преобладанием запоров 4. Вариант, при котором запоры чередуются с диареей. Считается, что основными механизмами развития синдрома раздраженного кишечника являются действие психосоциальных факторов, нарушения моторики и висцеральной чувствительности кишечника. В настоящее время предложено несколько теорий, пытающихся объяснить патогенез синдрома раздраженного кишечника. 1. Нарушение моторной функции толстого кишечника. Существенная роль в нарушении моторики толстого кишечника принадлежит дисбалансу медиаторов, высвобождаемых энтерохромаффинными клетками кишечника. Энтерохромаффинные клетки осуществляют «переключение» воспринимаемых ими механических и химических сигналов. Эти клетки вырабатывают ацетилхолин, а также субстанцию Р и К, стимулирующие сокращение мышц кишечника в проксимальном направлении. ВИП и NO, образуемые энтерохромаффинными клетками, вызывают расслабление мускулатуры кишечника в каудальном направлении. При нарушении баланса между этими веществами моторика кишечника может либо усиливаться, либо, наоборот, ослабляться. 2. Формирование висцеральной гиперчувствительности. Увеличение чувствительности слизистой оболочки кишечника к действию стимулов, которые в обычных условиях не воспринимаются как болевые, может происходить по разным причинам. Во-первых, это наблюдается после острого воспаления слизистой оболочки кишечника, когда увеличивается чувствительность расположенных в ней нервных окончаний. Во-вторых, к висцеральной гиперчувствительности приводит изменение интенсивности стимулов, исходящих от слизистой оболочки кишечника и воспринимаемых нейронами задних рогов спинного мозга. В-третьих, различные нарушения функций лимбической нервной системы сопровождаются изменениями механизмов супраспинальной модуляции информации, поступающей от рецепторов слизистой оболочки кишечника. Формирование гиперчувствительности слизистой оболочки кишечника приводит к тому, что неболевые импульсы начинают восприниматься как боль. 3. Действие психосоциальных факторов. Неблагоприятные социальные условия, частые стрессы, эмоциональная неуравновешенность, нарушения характера и режима питания, несоблюдение режима дня и т.п. приводят формированию висцеральной гиперчувствительности слизистой оболочки кишечника, боли и нарушениям дефекации. Кроме того, действие психосоциальных факторов может приводить к активации нейронов префронтальной коры головного мозга, что модулирует процессы восприятия и переработки афферентных импульсов от слизистой оболочки кишечника. 4. Наличие предшествующих инфекционных заболеваний кишечника. В результате воспаления слизистой оболочки кишечника увеличивается ее проницаемость для низкомолекулярных сахаров; уменьшается количество энтерохромаффинных клеток, а также увеличивается число CD3-клеток в слизистой оболочек кишечника. Итогом этих событий может быть нарушение моторной функции кишечника.
Упрощенно патогенез синдрома раздраженного кишечника можно представить в виде следующей схемы:
Рис. Патофизиологические механизмы синдрома раздраженного кишечника (Horwitz B. J., Fisher R. S., 2001)
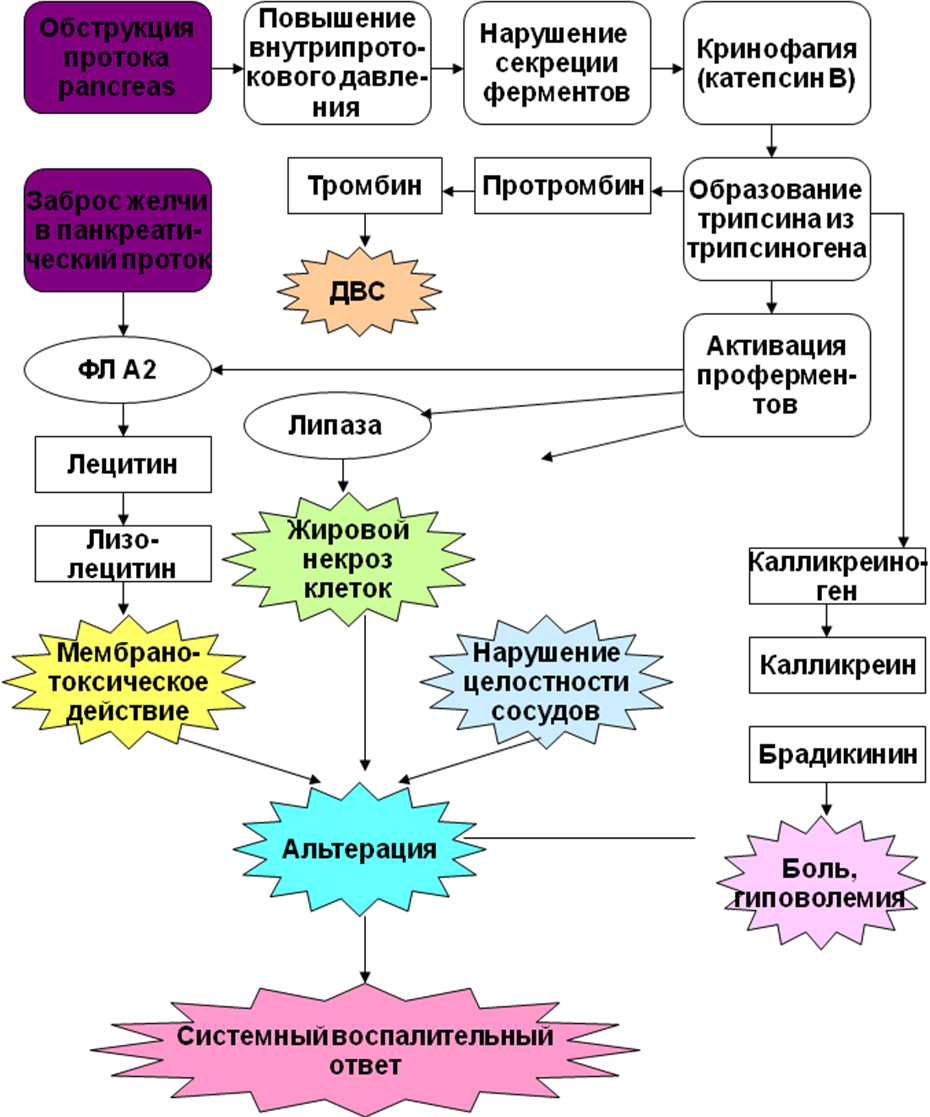
ПАНКРЕАТИТЫ Панкреатит – воспалительное заболевание поджелудочной железы, характеризующееся преимущественным поражением ее ацинусов. Различают острый и хронический панкреатит. Острый панкреатит В физиологических условиях клетки поджелудочной железы, продуцирующие пищеварительные ферменты, защищены от самопереваривания благодаря наличию уникальных механизмов. Во-первых, эти ферменты вырабатываются в виде неактивных форм. Во-вторых, субклеточные компартменты, содержащие зимогенные гранулы, анатомически разделены. В-третьих, проферменты в секреторных гранулах упакованы в комплексе с ингибиторами протеаз и окружены белком паракристаллином. И, наконец, в-четвертых, в зимогенных гранулах присутствуют низкие концентрации ионизированного кальция, а рН внутренней среды гранул смещено в кислую сторону, что препятствует преждевременной активации проферментов в клетках поджелудочной железы. При несостоятельности этих механизмов создаются условия для внутриклеточной активации проферментов и самопереваривания (аутодигестии) клеток поджелудочной железы, т.е. для развития острого панкреатита. Причины, вызывающие острый панкреатит, бывают экзогенные и эндогенные. К экзогенным причинам относятся: ü прием больших доз алкоголя, особенно при наличии сопутствующей желчнокаменной болезни (ЖКБ); ü вирусы (эпидемического паротита, Коксаки и др.); ü травмы, хирургические вмешательства, инвазивные диагностические исследования; ü прием некоторых лекарственных препаратов (диуретиков тиазидового ряда, этакриновой кислоты, фуросемида; азатиоприна, вальпроевой кислоты, эстроген-содержащих препаратов, тетрациклина, сульфаниламидов, пентамидина и др.); ü укус скорпиона. Острый панкреатит может быть вызван эндогенными причинами: ü обструкцией общего желчного протока конкрементами при ЖКБ, а также рефлюксом желчи в панкреатические протоки; ü отеком или спазмом сфинктера Одди; ü гиперкальциемией, например, при гиперфункции паращитовидных желез; ü пенетрацией в поджелудочную железу пептической язвы. Дислипопротеинемии I, IV, V типов, заболевания соединительной ткани и почечная недостаточность также часто осложняются развитием острого панкреатита. Иногда точную причину острого панкреатита установить не удается, и в этом случае говорят об идиопатическом остром панкреатите. Патогенез острого панкреатита можно представить в виде схемы: (1) действие патогена ® развитие универсальных механизмов повреждения экзокринных клеток поджелудочной железы («окислительный» и «нитрозилирующий» стресс, уменьшение образования АТФ, увеличение содержания внутриклеточного ионизированного кальция) ® повреждения структуры внутриклеточных микротрубочек и микрофиламентов ® нарушение выделения зимогенных гранул в панкреатические протоки ® ”панкреастаз” ® смешивание содержимого гранул лизосом и зимогенных гранул ® внутриклеточная активация трипсиногена и превращение его в трипсин ® запуск каскада активации остальных проферментов и других биологически активных веществ. Трипсин способен активировать панкреатическую липазу, которая разрушает мембраны клеток поджелудочной железы и вызывает их жировой некроз. Активация фосфолипазы А2 (ФЛ А2) под влиянием трипсина приводит к расщеплению лецитина клеточных мембран до лизолецитина, лизолецитина, обладающего мембранотоксическим действием и усугубляющим выраженность повреждения клеток поджелудочной железы. Трипсин также способствует превращению панкреатической проэластазы в активную эластазу. Последняя нарушает целостность кровеносных сосудов поджелудочной железы и увеличивает их проницаемость, способствуя тем самым усилению отека поджелудочной железы. Кроме того, под влиянием трипсина из калликреиногена образуются большие количества калликреина и брадикинина. Эти медиаторы воспаления способны активировать эндотелиоцитарную конституциональную NO-синтазу кровеносных сосудов не только поджелудочной железы, но и всего организма. Увеличение образования оксида азота в кровеносных сосудах ведет к снижению их тонуса, увеличению их проницаемости, отеку поджелудочной железы и артериальной гипотензии. Брадикинин, взаимодействуя с соответствующими рецепторами, вызывает боль, которая при остром панкреатите может быть нестерпимой; некоторые пациенты характеризуют ее как «чувство вбитого кола в подреберье». Трипсин также способствует превращению протромбина в тромбин, что, совместно с активацией тромбоцитов провоспалительными цитокинами и другими медиаторами воспаления приводит к развитию ДВС-синдрома. (2) Попадание содержимого секреторных гранул в интерстиций поджелудочной железы ® хемоаттрактантное действие компонентов гранул ® привлечение в очаг воспаления клеток лейкоцитарного ряда ® активация нейтрофилов и макрофагов ® выделение в интерстициальное пространство АФК и АФА, а также протеаз – катепсинов B, D, G, коллагеназы и эластазы; образование макрофагами провоспалительных цитокинов ФНО-a, ИЛ-6, ИЛ-8 ® амплификация локального воспаления ® развитие системного воспалительного ответа.
Рис. Патогенез острого панкреатита
Существуют некоторые особенности механизмов возникновения острого панкреатита при действии различных патогенов. Так, одна из наиболее частых причин острого панкреатита – употребление чрезмерных количеств алкоголя. В этом случае развитию панкреатита способствуют: стимуляция этанолом внешнесекреторной функции поджелудочной железы; спазм или острый отек сфинктера Одди под действием этанола, приводящие к увеличению давления в протоках поджелудочной железы; повышение активности окислительного пути деградации этанола в поджелудочной железе и гибель части ее паренхиматозных клеток в результате «окислительного» стресса. При ЖКБ могут наблюдаться спазм или отек сфинктера Одди, либо заброс желчи и содержимого 12-перстной кишки в протоки поджелудочной железы. При этом внутриклеточной активации проферментов предшествует активация фосфолипазы А2. Морфологически острый панкреатит может проявляться острым отеком поджелудочной железы, геморрагическим воспалением, панкреонекрозом и гнойным воспалением. Достаточно часто при остром панкреатите пациенты погибают из-за развития системных осложнений. Таблица
|
|||||||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 44; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.158.47 (0.048 с.) |