Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Исследование равновесия в системе газ-жидкость
Процессы, протекающие в системе «газ-жидкость», условно можно разделить на две группы:
У = К – Ф + 2 = 2- 2 +2 = 2. Это означает, что при постоянном давлении равновесные концентрации СЖ и СГ установятся при определенной температуре.
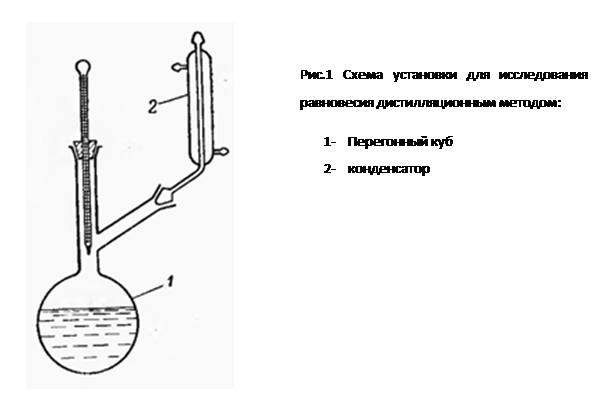
Для идеальных газожидкостных систем равновесие описывается законами Рауля и Дальтона. Однако в реальных производственных условиях практически не существует идеальных систем, поэтому равновесные соотношения «жидкость – газ (пар)» могут быть определены только экспериментальным путем. Исследование равновесия в системе «газ-жидкость» статическим методом Простейшим методом изучения равновесия в этой системе является дистилляционный. Суть метода состоит в следующем.
Из куба, имеющего большой объем, отбирается на анализ небольшое количество пара (при разделении смесей берут малый объем). Объем отбираемой пробы должен быть минимальным, так как отбор больших количеств вносит неточности при проведении исследований. Недостатки метод:
Этот метод причислен к раритетным и практически не применяется.
В настоящее время для исследования равновесия в системе «газ-жидкость» используется циркуляционный метод.
Перегонный куб заполняют на 1/5 высоты жидкостью и доводят до кипения. Обогрев куба может производится с помощью газовой горелки, наружного или внутреннего электронагревателя. Образующийся пар поступает в паровую трубку, затем проходит к холодильнику, оттуда после полной конденсации поступает в приемник. Пары, окружающие паровую трубку, предотвращают частичную конденсацию на стенках. Первые порции дистиллята промывают приемник и кран для отбора проб и их сливают, после чего конденсат собирают в приемник. Во время опыта температура непрерывно повышается, вследствие этого кубовая жидкость обедняется легколетучим компонентом. После заполнения приемника конденсат через затвор поступает в перегонный куб, после чего температура падает. После многократного обмена содержимого приемника достигается равновесное состояние, при котором фазовые составы жидкости и дистиллята не изменяются. В среднем процесс установления равновесия занимает от 30 до 60 мин. Также равновесное состояние характеризуется постоянством температуры. Источники ошибок: • В трубке, отводящей пар к холодильнику, необходимо предотвращать частичную конденсацию пара. Особенно это актуально для высококипящих систем. Особое внимание необходимо уделять теплоизоляции верхней части прибора или проводить дополнительный обогрев с помощью электрической спирали;
• Необходимо избегать перегрева стенок куба, так как это приводит к полному испарению капелек, разбрызганных по стенкам и нарушению равновесия. Как правило, в этом случае достаточно просто обеспечить перемешивание жидкости (добавить «кипелки»); • Следует помнить, что температура измеренная в паровой фазе, не всегда соответствует истинной температуре кипения.
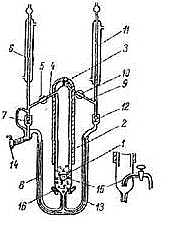
Прибор Бушмакена
В данном приборе использован тот же принцип, что в приборе Отмера, - термостатирование пространства, по которому отбираются пары кипящей жидкости с помощью этих же паров. Принципиальное отличие от вышерассмотренной установки - термостатирование производится движущимся потоком пара.
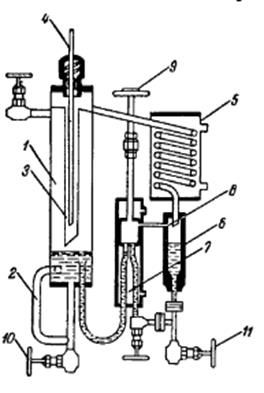
Пробы жидкости и конденсата пара могут отбираться при работающем приборе или после его остановки и охлаждения. В первом случае пробу следует отбирать в охлаждаемый сосуд Определение равновесия при высоких давлениях Установки для работы при высоких давлениях выполняются из нержавеющей стали, краны заменяются вентилями для высоких давлений. Методика работы и основные части аналогичны оборудованию, предназначенному для работы при обычном и пониженном давлениях. Куб прибора представляет собой цилиндрический сосуд 1, снабженный выносным кипятильником 2. По внутренней трубке 3, в которую помещен термометр 4, пар поступает в конденсатор 5. Конденсат стекает в приемник 6, соединенный с охлаждаемым гидравлическим затвором 7, который необходим для поддержания постоянного уровня жидкости в приемнике конденсата. Давление в приборе создается с помощью инертного газа. После установления равновесия пробы жидкой и паровой фаз отбираются с помощью вентилей 10 и 11.
При проведении исследований при повышенном давлении необходимо учитывать тот факт, что растворимость газов увеличивается с повышением давления. Даже при весьма тщательном контроле измерений давления и температуры может иметь место несоответствие результатов, полученных разными исследователями. До настоящего времени не создан прибор, позволяющий получать достоверные результаты для разных систем. Большинство новейших приборов позволяют достигнуть точности, достаточной для проведения необходимых расчетов. Одним из путей повышения точности является проведение измерений концентраций без отбора жидкости в кубе или конденсата в паре. В последнее время применяется проточный рефрактометр. Благодаря его использованию время достижения равновесия сократилось до 10 мин, в то время как при использовании циркуляционного прибора Отмера оно составляло несколько часов.
ЛЕКЦИЯ № 6
|
|||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 107; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.126.5 (0.006 с.) |