"Жизнь, есть способ существования белковых тел"
Ф. Энгельс.
Прочитайте материал:
Ни один из известных нам живых организмов не обходится без белков. Белки служат питательными веществами, они регулируют обмен веществ, исполняя роль ферментов – катализаторов обмена веществ, способствуют переносу кислорода по всему организму и его поглощению, играют важную роль в функционировании нервной системы, являются механической основой мышечного сокращения, участвуют в передаче генетической информации и т.д.
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями. В состав этих биополимеров входят мономеры 20 типов. Такими мономерами являются аминокислоты. Каждый белок по своему химическому строению является полипептидом. Некоторые белки состоят из нескольких полипептидных цепей. В составе большинства белков находится в среднем 300-500 остатков аминокислот. Известно несколько очень коротких природных белков, длиной в 3-8 аминокислот, и очень длинных биополимеров, длиной более чем в 1500 аминокислот. Образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот:
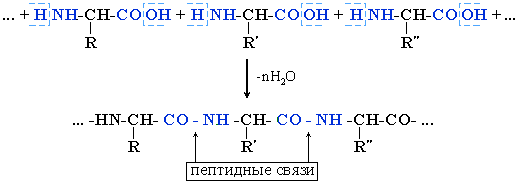 Аминокислоты соединяются друг с другом за счёт образования новой связи между атомами углерода и азота – пептидной (амидной):
Аминокислоты соединяются друг с другом за счёт образования новой связи между атомами углерода и азота – пептидной (амидной):
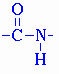 Из двух аминокислот (АК) можно получить дипептид, из трёх – трипептид, из большего числа АК получают полипептиды (белки).
Функции белков
Функции белков в природе универсальны. Белки входят в состав мозга, внутренних органов, костей, кожи, волосяного покрова и т.д. Основным источником α - аминокислот для живого организма служат пищевые белки, которые в результате ферментативного гидролиза в желудочно-кишечном тракте дают α - аминокислоты. Многие α - аминокислоты синтезируются в организме, а некоторые необходимые для синтеза белков α - аминокислоты не синтезируются в организме и должны поступать извне. Такие аминокислоты называются незаменимыми. К ним относятся валин, лейцин, треонин, метионин, триптофан и др. (см. таблицу). При некоторых заболеваниях человека перечень незаменимых аминокислот расширяется.
· Каталитическая функция - осуществляется с помощью специфических белков - катализаторов (ферментов). При их участии увеличивается скорость различных реакций обмена веществ и энергии в организме.
Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации ДНК и матричного синтеза РНК. Известно несколько тысяч ферментов. Среди них такие, как, например пепсин, расщепляют белки в процессе пищеварения.
· Транспортная функция - связывание и доставка (транспорт) различных веществ от одного органа к другому.
Так, белок эритроцитов крови гемоглобин соединяется в легких с кислородом, превращаясь в оксигемоглобин. Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород, необходимый для обеспечения окислительных процессов в тканях.
· Защитная функция - связывание и обезвреживание веществ, поступающих в организм или появляющихся в результате жизнедеятельности бактерий и вирусов.
Защитную функцию выполняют специфические белки (антитела - иммуноглобулины), образующиеся в организме (физическая, химическая и иммунная защита). Так, например, защитную функцию выполняет белок плазмы крови фибриноген, участвуя в свертывании крови и тем самым уменьшая кровопотери.
· Сократительная функция (актин, миозин) – в результате взаимодействия белков происходит передвижение в пространстве, сокращение и расслабление сердца, движение других внутренних органов.
Структурная функция - белки составляют основу строения клетки. Некоторые из них (коллаген соединительной ткани, кератин волос, ногтей и кожи, эластин сосудистой стенки, кератин шерсти, фиброин шелка и др.) выполняют почти исключительно структурную функцию.
В комплексе с липидами белки участвуют в построении мембран клеток и внутриклеточных образований.
· Гормональная (регуляторная) функция - способность передавать сигналы между тканями, клетками или организмами.
Выполняют белки-регуляторы обмена веществ. Они относятся к гормонам, которые образуются в железах внутренней секреции, некоторых органах и тканях организма.
· Питательная функция - осуществляется резервными белками, которые запасаются в качестве источника энергии и вещества.
Например: казеин, яичный альбумин, белки яйца обеспечивают рост и развитие плода, а белки молока служат источником питания для новорожденного.
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
Физические свойства белков
Белки – очень длинные молекулы, которые состоят из звеньев аминокислот, сцепленных пептидными связями. Это – природные полимеры, молекулярная масса белков колеблется от нескольких тысяч до нескольких десятков миллионов. Например, альбумин молока имеет молекулярную массу 17400, фибриноген крови – 400.000, белки вирусов – 50.000.000. Каждый пептид и белок обладают строго определенным составом и последовательностью аминокислотных остатков в цепи, это и определяет их уникальную биологическую специфичность. Количество белков характеризует степень сложности организма (кишечная палочка – 3000, а в человеческом организме более 5 млн. белков).
Первый белок, с которым мы знакомимся в своей жизни, это белок куриного яйца альбумин - хорошо растворим в воде, при нагревании свертывается (когда мы жарим яичницу), а при долгом хранении в тепле разрушается, яйцо протухает. Но белок спрятан не только под яичной скорлупой. Волосы, ногти, когти, шерсть, перья, копыта, наружный слой кожи - все они почти целиком состоят из другого белка, кератина. Кератин не растворяется в воде, не свертывается, не разрушается в земле: рога древних животных сохраняются в ней так же хорошо, как и кости. А белок пепсин, содержащийся в желудочном соке, способен разрушать другие белки, это процесс пищеварения. Белок инрерферон применяется при лечении насморка и гриппа, т.к. убивает вызывающие эти болезни вирусы. А белок змеиного яда способен убивать человека.
Классификация белков
Из двух аминокислот (АК) можно получить дипептид, из трёх – трипептид, из большего числа АК получают полипептиды (белки).
Функции белков
Функции белков в природе универсальны. Белки входят в состав мозга, внутренних органов, костей, кожи, волосяного покрова и т.д. Основным источником α - аминокислот для живого организма служат пищевые белки, которые в результате ферментативного гидролиза в желудочно-кишечном тракте дают α - аминокислоты. Многие α - аминокислоты синтезируются в организме, а некоторые необходимые для синтеза белков α - аминокислоты не синтезируются в организме и должны поступать извне. Такие аминокислоты называются незаменимыми. К ним относятся валин, лейцин, треонин, метионин, триптофан и др. (см. таблицу). При некоторых заболеваниях человека перечень незаменимых аминокислот расширяется.
· Каталитическая функция - осуществляется с помощью специфических белков - катализаторов (ферментов). При их участии увеличивается скорость различных реакций обмена веществ и энергии в организме.
Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации ДНК и матричного синтеза РНК. Известно несколько тысяч ферментов. Среди них такие, как, например пепсин, расщепляют белки в процессе пищеварения.
· Транспортная функция - связывание и доставка (транспорт) различных веществ от одного органа к другому.
Так, белок эритроцитов крови гемоглобин соединяется в легких с кислородом, превращаясь в оксигемоглобин. Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород, необходимый для обеспечения окислительных процессов в тканях.
· Защитная функция - связывание и обезвреживание веществ, поступающих в организм или появляющихся в результате жизнедеятельности бактерий и вирусов.
Защитную функцию выполняют специфические белки (антитела - иммуноглобулины), образующиеся в организме (физическая, химическая и иммунная защита). Так, например, защитную функцию выполняет белок плазмы крови фибриноген, участвуя в свертывании крови и тем самым уменьшая кровопотери.
· Сократительная функция (актин, миозин) – в результате взаимодействия белков происходит передвижение в пространстве, сокращение и расслабление сердца, движение других внутренних органов.
Структурная функция - белки составляют основу строения клетки. Некоторые из них (коллаген соединительной ткани, кератин волос, ногтей и кожи, эластин сосудистой стенки, кератин шерсти, фиброин шелка и др.) выполняют почти исключительно структурную функцию.
В комплексе с липидами белки участвуют в построении мембран клеток и внутриклеточных образований.
· Гормональная (регуляторная) функция - способность передавать сигналы между тканями, клетками или организмами.
Выполняют белки-регуляторы обмена веществ. Они относятся к гормонам, которые образуются в железах внутренней секреции, некоторых органах и тканях организма.
· Питательная функция - осуществляется резервными белками, которые запасаются в качестве источника энергии и вещества.
Например: казеин, яичный альбумин, белки яйца обеспечивают рост и развитие плода, а белки молока служат источником питания для новорожденного.
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
Физические свойства белков
Белки – очень длинные молекулы, которые состоят из звеньев аминокислот, сцепленных пептидными связями. Это – природные полимеры, молекулярная масса белков колеблется от нескольких тысяч до нескольких десятков миллионов. Например, альбумин молока имеет молекулярную массу 17400, фибриноген крови – 400.000, белки вирусов – 50.000.000. Каждый пептид и белок обладают строго определенным составом и последовательностью аминокислотных остатков в цепи, это и определяет их уникальную биологическую специфичность. Количество белков характеризует степень сложности организма (кишечная палочка – 3000, а в человеческом организме более 5 млн. белков).
Первый белок, с которым мы знакомимся в своей жизни, это белок куриного яйца альбумин - хорошо растворим в воде, при нагревании свертывается (когда мы жарим яичницу), а при долгом хранении в тепле разрушается, яйцо протухает. Но белок спрятан не только под яичной скорлупой. Волосы, ногти, когти, шерсть, перья, копыта, наружный слой кожи - все они почти целиком состоят из другого белка, кератина. Кератин не растворяется в воде, не свертывается, не разрушается в земле: рога древних животных сохраняются в ней так же хорошо, как и кости. А белок пепсин, содержащийся в желудочном соке, способен разрушать другие белки, это процесс пищеварения. Белок инрерферон применяется при лечении насморка и гриппа, т.к. убивает вызывающие эти болезни вирусы. А белок змеиного яда способен убивать человека.
Классификация белков
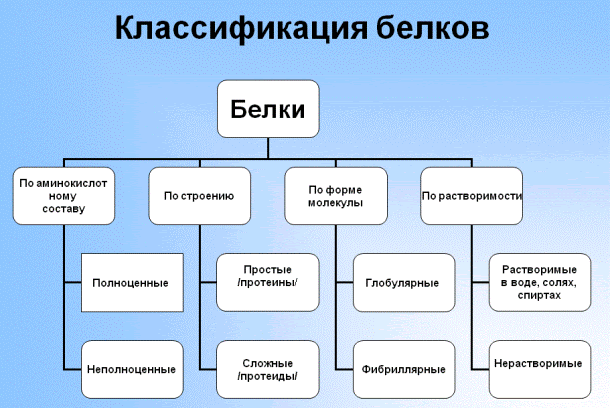 С точки зрения пищевой ценности белков, определяемой их аминокислотным составом и содержанием так называемых незаменимых аминокислот, белки подразделяются на полноценные и неполноценные. К полноценным белкам относятся преимущественно белки животного происхождения, кроме желатины, относящейся к неполноценным белкам. Неполноценные белки — преимущественно растительного происхождения. Однако некоторые растения (картофель, бобовые и др.) содержат полноценные белки. Из животных белков особенно большую ценность для организма представляют белки мяса, яиц, молока и др.
В состав многих белков помимо пептидных цепей входят и неаминокислотные фрагменты, по этому критерию белки делят на две большие группы — простые и сложные белки (протеиды). Простые белки содержат только аминокислотные цепи, сложные белки содержат также неаминокислотные фрагменты (Например, гемоглобин содержит железо).
По общему типу строения белки можно разбить на три группы:
С точки зрения пищевой ценности белков, определяемой их аминокислотным составом и содержанием так называемых незаменимых аминокислот, белки подразделяются на полноценные и неполноценные. К полноценным белкам относятся преимущественно белки животного происхождения, кроме желатины, относящейся к неполноценным белкам. Неполноценные белки — преимущественно растительного происхождения. Однако некоторые растения (картофель, бобовые и др.) содержат полноценные белки. Из животных белков особенно большую ценность для организма представляют белки мяса, яиц, молока и др.
В состав многих белков помимо пептидных цепей входят и неаминокислотные фрагменты, по этому критерию белки делят на две большие группы — простые и сложные белки (протеиды). Простые белки содержат только аминокислотные цепи, сложные белки содержат также неаминокислотные фрагменты (Например, гемоглобин содержит железо).
По общему типу строения белки можно разбить на три группы:
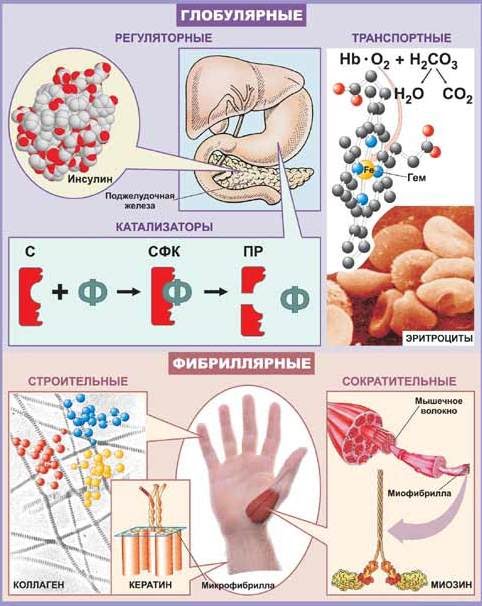 1. Фибриллярные белки — нерастворимы в воде, образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Белки, имеющие вытянутую нитевидную структуру. Полипептидные цепи многих фибриллярных белков расположены параллельно друг другу вдоль одной оси и образуют длинные волокна (фибриллы) или слои.
Большинство фибриллярных белков не растворяются в воде. К фибриллярным белкам относят например, α-кератины (на их долю приходится почти весь сухой вес волос, белки шерсти, рогов, копыт, ногтей, чешуи, перьев), коллаген — белок сухожилий и хрящей, фиброин — белок шёлка).
2. Глобулярные белки — водорастворимы, общая форма молекулы более или менее сферическая. Среди глобулярных и фибриллярных белков выделяют подгруппы. К глобулярным белкам относятся ферменты, иммуноглобулины, некоторые гормоны белковой природы (например, инсулин) а также другие белки, выполняющие транспортные, регуляторные и вспомогательные функции.
3. Мембранные белки — имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ. Белки-транспортеры специфичны, каждый из них пропускает через мембрану только определённые молекулы или определённый тип сигнала.
Белки – неотъемлемая часть пищи животных и человека. Живой организм отличается от неживого в первую очередь наличием белков. Для живых организмов характерно огромное разнообразие белковых молекул и их высокая упорядоченность, что и определяет высокую организацию живого организма, а также способность двигаться, сокращаться, воспроизводиться, способность к обмену веществ и к многим физиологическим процессам.
Строение белков
1. Фибриллярные белки — нерастворимы в воде, образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Белки, имеющие вытянутую нитевидную структуру. Полипептидные цепи многих фибриллярных белков расположены параллельно друг другу вдоль одной оси и образуют длинные волокна (фибриллы) или слои.
Большинство фибриллярных белков не растворяются в воде. К фибриллярным белкам относят например, α-кератины (на их долю приходится почти весь сухой вес волос, белки шерсти, рогов, копыт, ногтей, чешуи, перьев), коллаген — белок сухожилий и хрящей, фиброин — белок шёлка).
2. Глобулярные белки — водорастворимы, общая форма молекулы более или менее сферическая. Среди глобулярных и фибриллярных белков выделяют подгруппы. К глобулярным белкам относятся ферменты, иммуноглобулины, некоторые гормоны белковой природы (например, инсулин) а также другие белки, выполняющие транспортные, регуляторные и вспомогательные функции.
3. Мембранные белки — имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ. Белки-транспортеры специфичны, каждый из них пропускает через мембрану только определённые молекулы или определённый тип сигнала.
Белки – неотъемлемая часть пищи животных и человека. Живой организм отличается от неживого в первую очередь наличием белков. Для живых организмов характерно огромное разнообразие белковых молекул и их высокая упорядоченность, что и определяет высокую организацию живого организма, а также способность двигаться, сокращаться, воспроизводиться, способность к обмену веществ и к многим физиологическим процессам.
Строение белков
 Фишер Эмиль Герман, немецкий химик-органик и биохимик. В 1899 начал работы по химии белков. Используя созданный им в 1901 эфирный метод анализа аминокислот, Ф. впервые осуществил качественные и количественные определения продуктов расщепления белков, открыл валин, пролин (1901) и оксипролин (1902), экспериментально доказал, что аминокислотные остатки связываются между собой пептидной связью; в 1907 синтезировал 18-членный полипептид. Ф. показал сходство синтетических полинептидов и пептидов, полученных в результате гидролиза белков. Ф. занимался также изучением дубильных веществ. Ф. создал школу химиков-органиков. Иностранный член-корреспондент Петербургской АН (1899). Нобелевская премия (1902).
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
Фишер Эмиль Герман, немецкий химик-органик и биохимик. В 1899 начал работы по химии белков. Используя созданный им в 1901 эфирный метод анализа аминокислот, Ф. впервые осуществил качественные и количественные определения продуктов расщепления белков, открыл валин, пролин (1901) и оксипролин (1902), экспериментально доказал, что аминокислотные остатки связываются между собой пептидной связью; в 1907 синтезировал 18-членный полипептид. Ф. показал сходство синтетических полинептидов и пептидов, полученных в результате гидролиза белков. Ф. занимался также изучением дубильных веществ. Ф. создал школу химиков-органиков. Иностранный член-корреспондент Петербургской АН (1899). Нобелевская премия (1902).
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
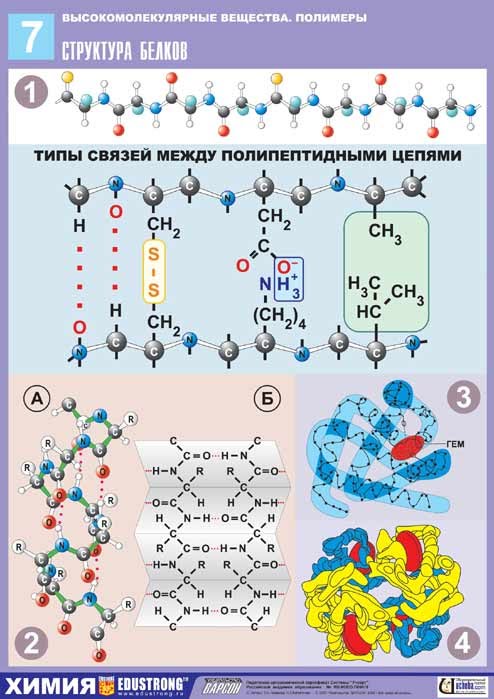 Выделяют 4 уровня структурной организации белков:
Выделяют 4 уровня структурной организации белков:
| 1. Первичная структура - определенная последовательность α-аминокислотных остатков в полипептидной цепи.
|
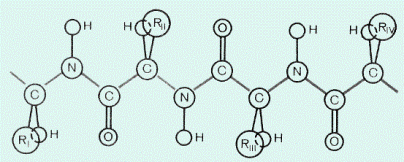
| | 2. Вторичная структура –
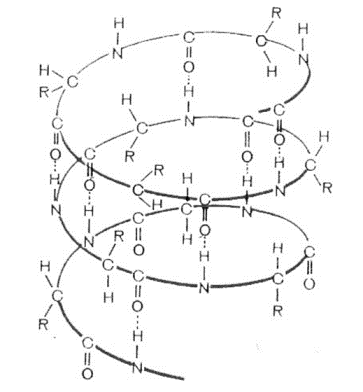
А) конформация полипептидной цепи, закрепленная множеством водородных связей между группами N-H и С=О. Одна из моделей вторичной структуры - α-спираль.
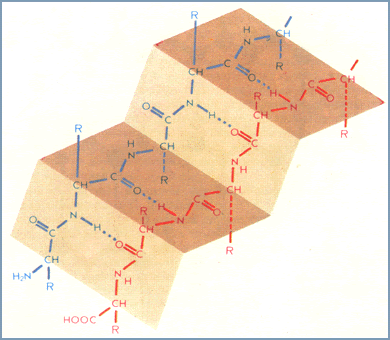
Б) Другая модель - β-форма ("складчатый лист"), в которой преобладают межцепные (межмолекулярные) Н-связи.
| А
 Б
Б
| | 3. Третичная структура - форма закрученной спирали в пространстве, образованная главным образом за счет дисульфидных мостиков -S-S-, водородных связей, гидрофобных и ионных взаимодействий.
|
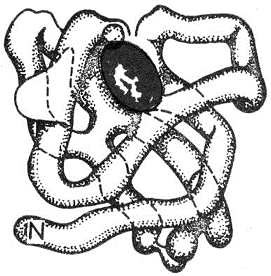
| | 4. Четвертичная структура - агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей
|

| |


 Аминокислоты соединяются друг с другом за счёт образования новой связи между атомами углерода и азота – пептидной (амидной):
Аминокислоты соединяются друг с другом за счёт образования новой связи между атомами углерода и азота – пептидной (амидной):
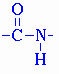 Из двух аминокислот (АК) можно получить дипептид, из трёх – трипептид, из большего числа АК получают полипептиды (белки).
Функции белков
Функции белков в природе универсальны. Белки входят в состав мозга, внутренних органов, костей, кожи, волосяного покрова и т.д. Основным источником α - аминокислот для живого организма служат пищевые белки, которые в результате ферментативного гидролиза в желудочно-кишечном тракте дают α - аминокислоты. Многие α - аминокислоты синтезируются в организме, а некоторые необходимые для синтеза белков α - аминокислоты не синтезируются в организме и должны поступать извне. Такие аминокислоты называются незаменимыми. К ним относятся валин, лейцин, треонин, метионин, триптофан и др. (см. таблицу). При некоторых заболеваниях человека перечень незаменимых аминокислот расширяется.
· Каталитическая функция - осуществляется с помощью специфических белков - катализаторов (ферментов). При их участии увеличивается скорость различных реакций обмена веществ и энергии в организме.
Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации ДНК и матричного синтеза РНК. Известно несколько тысяч ферментов. Среди них такие, как, например пепсин, расщепляют белки в процессе пищеварения.
· Транспортная функция - связывание и доставка (транспорт) различных веществ от одного органа к другому.
Так, белок эритроцитов крови гемоглобин соединяется в легких с кислородом, превращаясь в оксигемоглобин. Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород, необходимый для обеспечения окислительных процессов в тканях.
· Защитная функция - связывание и обезвреживание веществ, поступающих в организм или появляющихся в результате жизнедеятельности бактерий и вирусов.
Защитную функцию выполняют специфические белки (антитела - иммуноглобулины), образующиеся в организме (физическая, химическая и иммунная защита). Так, например, защитную функцию выполняет белок плазмы крови фибриноген, участвуя в свертывании крови и тем самым уменьшая кровопотери.
· Сократительная функция (актин, миозин) – в результате взаимодействия белков происходит передвижение в пространстве, сокращение и расслабление сердца, движение других внутренних органов.
Структурная функция - белки составляют основу строения клетки. Некоторые из них (коллаген соединительной ткани, кератин волос, ногтей и кожи, эластин сосудистой стенки, кератин шерсти, фиброин шелка и др.) выполняют почти исключительно структурную функцию.
В комплексе с липидами белки участвуют в построении мембран клеток и внутриклеточных образований.
· Гормональная (регуляторная) функция - способность передавать сигналы между тканями, клетками или организмами.
Выполняют белки-регуляторы обмена веществ. Они относятся к гормонам, которые образуются в железах внутренней секреции, некоторых органах и тканях организма.
· Питательная функция - осуществляется резервными белками, которые запасаются в качестве источника энергии и вещества.
Например: казеин, яичный альбумин, белки яйца обеспечивают рост и развитие плода, а белки молока служат источником питания для новорожденного.
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
Физические свойства белков
Белки – очень длинные молекулы, которые состоят из звеньев аминокислот, сцепленных пептидными связями. Это – природные полимеры, молекулярная масса белков колеблется от нескольких тысяч до нескольких десятков миллионов. Например, альбумин молока имеет молекулярную массу 17400, фибриноген крови – 400.000, белки вирусов – 50.000.000. Каждый пептид и белок обладают строго определенным составом и последовательностью аминокислотных остатков в цепи, это и определяет их уникальную биологическую специфичность. Количество белков характеризует степень сложности организма (кишечная палочка – 3000, а в человеческом организме более 5 млн. белков).
Первый белок, с которым мы знакомимся в своей жизни, это белок куриного яйца альбумин - хорошо растворим в воде, при нагревании свертывается (когда мы жарим яичницу), а при долгом хранении в тепле разрушается, яйцо протухает. Но белок спрятан не только под яичной скорлупой. Волосы, ногти, когти, шерсть, перья, копыта, наружный слой кожи - все они почти целиком состоят из другого белка, кератина. Кератин не растворяется в воде, не свертывается, не разрушается в земле: рога древних животных сохраняются в ней так же хорошо, как и кости. А белок пепсин, содержащийся в желудочном соке, способен разрушать другие белки, это процесс пищеварения. Белок инрерферон применяется при лечении насморка и гриппа, т.к. убивает вызывающие эти болезни вирусы. А белок змеиного яда способен убивать человека.
Классификация белков
Из двух аминокислот (АК) можно получить дипептид, из трёх – трипептид, из большего числа АК получают полипептиды (белки).
Функции белков
Функции белков в природе универсальны. Белки входят в состав мозга, внутренних органов, костей, кожи, волосяного покрова и т.д. Основным источником α - аминокислот для живого организма служат пищевые белки, которые в результате ферментативного гидролиза в желудочно-кишечном тракте дают α - аминокислоты. Многие α - аминокислоты синтезируются в организме, а некоторые необходимые для синтеза белков α - аминокислоты не синтезируются в организме и должны поступать извне. Такие аминокислоты называются незаменимыми. К ним относятся валин, лейцин, треонин, метионин, триптофан и др. (см. таблицу). При некоторых заболеваниях человека перечень незаменимых аминокислот расширяется.
· Каталитическая функция - осуществляется с помощью специфических белков - катализаторов (ферментов). При их участии увеличивается скорость различных реакций обмена веществ и энергии в организме.
Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации ДНК и матричного синтеза РНК. Известно несколько тысяч ферментов. Среди них такие, как, например пепсин, расщепляют белки в процессе пищеварения.
· Транспортная функция - связывание и доставка (транспорт) различных веществ от одного органа к другому.
Так, белок эритроцитов крови гемоглобин соединяется в легких с кислородом, превращаясь в оксигемоглобин. Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород, необходимый для обеспечения окислительных процессов в тканях.
· Защитная функция - связывание и обезвреживание веществ, поступающих в организм или появляющихся в результате жизнедеятельности бактерий и вирусов.
Защитную функцию выполняют специфические белки (антитела - иммуноглобулины), образующиеся в организме (физическая, химическая и иммунная защита). Так, например, защитную функцию выполняет белок плазмы крови фибриноген, участвуя в свертывании крови и тем самым уменьшая кровопотери.
· Сократительная функция (актин, миозин) – в результате взаимодействия белков происходит передвижение в пространстве, сокращение и расслабление сердца, движение других внутренних органов.
Структурная функция - белки составляют основу строения клетки. Некоторые из них (коллаген соединительной ткани, кератин волос, ногтей и кожи, эластин сосудистой стенки, кератин шерсти, фиброин шелка и др.) выполняют почти исключительно структурную функцию.
В комплексе с липидами белки участвуют в построении мембран клеток и внутриклеточных образований.
· Гормональная (регуляторная) функция - способность передавать сигналы между тканями, клетками или организмами.
Выполняют белки-регуляторы обмена веществ. Они относятся к гормонам, которые образуются в железах внутренней секреции, некоторых органах и тканях организма.
· Питательная функция - осуществляется резервными белками, которые запасаются в качестве источника энергии и вещества.
Например: казеин, яичный альбумин, белки яйца обеспечивают рост и развитие плода, а белки молока служат источником питания для новорожденного.
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
Физические свойства белков
Белки – очень длинные молекулы, которые состоят из звеньев аминокислот, сцепленных пептидными связями. Это – природные полимеры, молекулярная масса белков колеблется от нескольких тысяч до нескольких десятков миллионов. Например, альбумин молока имеет молекулярную массу 17400, фибриноген крови – 400.000, белки вирусов – 50.000.000. Каждый пептид и белок обладают строго определенным составом и последовательностью аминокислотных остатков в цепи, это и определяет их уникальную биологическую специфичность. Количество белков характеризует степень сложности организма (кишечная палочка – 3000, а в человеческом организме более 5 млн. белков).
Первый белок, с которым мы знакомимся в своей жизни, это белок куриного яйца альбумин - хорошо растворим в воде, при нагревании свертывается (когда мы жарим яичницу), а при долгом хранении в тепле разрушается, яйцо протухает. Но белок спрятан не только под яичной скорлупой. Волосы, ногти, когти, шерсть, перья, копыта, наружный слой кожи - все они почти целиком состоят из другого белка, кератина. Кератин не растворяется в воде, не свертывается, не разрушается в земле: рога древних животных сохраняются в ней так же хорошо, как и кости. А белок пепсин, содержащийся в желудочном соке, способен разрушать другие белки, это процесс пищеварения. Белок инрерферон применяется при лечении насморка и гриппа, т.к. убивает вызывающие эти болезни вирусы. А белок змеиного яда способен убивать человека.
Классификация белков
 С точки зрения пищевой ценности белков, определяемой их аминокислотным составом и содержанием так называемых незаменимых аминокислот, белки подразделяются на полноценные и неполноценные. К полноценным белкам относятся преимущественно белки животного происхождения, кроме желатины, относящейся к неполноценным белкам. Неполноценные белки — преимущественно растительного происхождения. Однако некоторые растения (картофель, бобовые и др.) содержат полноценные белки. Из животных белков особенно большую ценность для организма представляют белки мяса, яиц, молока и др.
В состав многих белков помимо пептидных цепей входят и неаминокислотные фрагменты, по этому критерию белки делят на две большие группы — простые и сложные белки (протеиды). Простые белки содержат только аминокислотные цепи, сложные белки содержат также неаминокислотные фрагменты (Например, гемоглобин содержит железо).
По общему типу строения белки можно разбить на три группы:
С точки зрения пищевой ценности белков, определяемой их аминокислотным составом и содержанием так называемых незаменимых аминокислот, белки подразделяются на полноценные и неполноценные. К полноценным белкам относятся преимущественно белки животного происхождения, кроме желатины, относящейся к неполноценным белкам. Неполноценные белки — преимущественно растительного происхождения. Однако некоторые растения (картофель, бобовые и др.) содержат полноценные белки. Из животных белков особенно большую ценность для организма представляют белки мяса, яиц, молока и др.
В состав многих белков помимо пептидных цепей входят и неаминокислотные фрагменты, по этому критерию белки делят на две большие группы — простые и сложные белки (протеиды). Простые белки содержат только аминокислотные цепи, сложные белки содержат также неаминокислотные фрагменты (Например, гемоглобин содержит железо).
По общему типу строения белки можно разбить на три группы:
 1. Фибриллярные белки — нерастворимы в воде, образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Белки, имеющие вытянутую нитевидную структуру. Полипептидные цепи многих фибриллярных белков расположены параллельно друг другу вдоль одной оси и образуют длинные волокна (фибриллы) или слои.
Большинство фибриллярных белков не растворяются в воде. К фибриллярным белкам относят например, α-кератины (на их долю приходится почти весь сухой вес волос, белки шерсти, рогов, копыт, ногтей, чешуи, перьев), коллаген — белок сухожилий и хрящей, фиброин — белок шёлка).
2. Глобулярные белки — водорастворимы, общая форма молекулы более или менее сферическая. Среди глобулярных и фибриллярных белков выделяют подгруппы. К глобулярным белкам относятся ферменты, иммуноглобулины, некоторые гормоны белковой природы (например, инсулин) а также другие белки, выполняющие транспортные, регуляторные и вспомогательные функции.
3. Мембранные белки — имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ. Белки-транспортеры специфичны, каждый из них пропускает через мембрану только определённые молекулы или определённый тип сигнала.
Белки – неотъемлемая часть пищи животных и человека. Живой организм отличается от неживого в первую очередь наличием белков. Для живых организмов характерно огромное разнообразие белковых молекул и их высокая упорядоченность, что и определяет высокую организацию живого организма, а также способность двигаться, сокращаться, воспроизводиться, способность к обмену веществ и к многим физиологическим процессам.
Строение белков
1. Фибриллярные белки — нерастворимы в воде, образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Белки, имеющие вытянутую нитевидную структуру. Полипептидные цепи многих фибриллярных белков расположены параллельно друг другу вдоль одной оси и образуют длинные волокна (фибриллы) или слои.
Большинство фибриллярных белков не растворяются в воде. К фибриллярным белкам относят например, α-кератины (на их долю приходится почти весь сухой вес волос, белки шерсти, рогов, копыт, ногтей, чешуи, перьев), коллаген — белок сухожилий и хрящей, фиброин — белок шёлка).
2. Глобулярные белки — водорастворимы, общая форма молекулы более или менее сферическая. Среди глобулярных и фибриллярных белков выделяют подгруппы. К глобулярным белкам относятся ферменты, иммуноглобулины, некоторые гормоны белковой природы (например, инсулин) а также другие белки, выполняющие транспортные, регуляторные и вспомогательные функции.
3. Мембранные белки — имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ. Белки-транспортеры специфичны, каждый из них пропускает через мембрану только определённые молекулы или определённый тип сигнала.
Белки – неотъемлемая часть пищи животных и человека. Живой организм отличается от неживого в первую очередь наличием белков. Для живых организмов характерно огромное разнообразие белковых молекул и их высокая упорядоченность, что и определяет высокую организацию живого организма, а также способность двигаться, сокращаться, воспроизводиться, способность к обмену веществ и к многим физиологическим процессам.
Строение белков
 Фишер Эмиль Герман, немецкий химик-органик и биохимик. В 1899 начал работы по химии белков. Используя созданный им в 1901 эфирный метод анализа аминокислот, Ф. впервые осуществил качественные и количественные определения продуктов расщепления белков, открыл валин, пролин (1901) и оксипролин (1902), экспериментально доказал, что аминокислотные остатки связываются между собой пептидной связью; в 1907 синтезировал 18-членный полипептид. Ф. показал сходство синтетических полинептидов и пептидов, полученных в результате гидролиза белков. Ф. занимался также изучением дубильных веществ. Ф. создал школу химиков-органиков. Иностранный член-корреспондент Петербургской АН (1899). Нобелевская премия (1902).
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
Фишер Эмиль Герман, немецкий химик-органик и биохимик. В 1899 начал работы по химии белков. Используя созданный им в 1901 эфирный метод анализа аминокислот, Ф. впервые осуществил качественные и количественные определения продуктов расщепления белков, открыл валин, пролин (1901) и оксипролин (1902), экспериментально доказал, что аминокислотные остатки связываются между собой пептидной связью; в 1907 синтезировал 18-членный полипептид. Ф. показал сходство синтетических полинептидов и пептидов, полученных в результате гидролиза белков. Ф. занимался также изучением дубильных веществ. Ф. создал школу химиков-органиков. Иностранный член-корреспондент Петербургской АН (1899). Нобелевская премия (1902).
Разнообразные функции белков определяются α-аминокислотным составом и строением их высокоорганизованных макромолекул.
 Выделяют 4 уровня структурной организации белков:
Выделяют 4 уровня структурной организации белков:

 Б
Б






