Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ионный транспорт: каналы и насосы
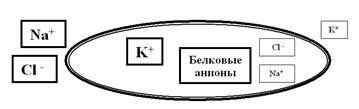
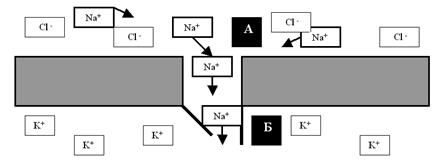
Рассмотрим подробнее функции каналов и насосов, ведь именно их работа обеспечивает формирование и изменение зарядов мембраны. Определяя особенности функционирования этих транспортных белков, мы использовали очень важное понятие: химический градиент ионов. Хочется напомнить, что в растворе молекулы диссоциируют на ионы. Наш организм, на 70% состоящий из воды, не исключение: в нём присутствуют и неорганические ионы (Na+, K+, Ca2+, Cl– и т.д.), и органические (например, белковые анионы). При этом распределение этих ионов по разные стороны мембраны далеко не одинаково. Так, в межклеточном пространстве чрезвычайно высока концентрация катионов Na+ и Ca2+, а также анионов Cl–. В цитоплазме этих ионов, наоборот, очень мало, зато там высоки концентрации катионов K+, а также белковых анионов. Таким образом, мы видим, что мембрана возбудимых (да и не только возбудимых) клеток разделяет две химически неоднородные среды (внутри клетки и снаружи) с существенно разными концентрациями ионов (рис. 7). То есть на мембране можно обнаружить (померить) химический градиент.
Рис. 7. Схема иллюстрирует ярко выраженное неравновесие ионов по разные стороны мембраны. Внутри клетки явно выше концентрация K+ и белковых анионов, а снаружи преобладают ионы Na+ и Cl–.
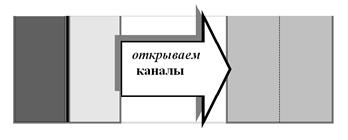
А теперь представьте себе простой опыт. Небольшой аквариум разделён пополам непроницаемой перегородкой. Перегородка состоит из двух слоёв: стеклянной пластинки (абсолютно непроницаемой для исследуемых нами веществ) и полимерной плёнки, через микроскопические поры которой могут проходить ионы какого-то одного вида. Наливаем в левую половинку аквариума концентрированный раствор интересующего нас вещества (например, простой поваренной соли, которая в водной среде диссоциирует на ионы: NaCl «Na++Cl-), а в правую — такой же раствор, но очень разбавленный (рис. 8).
Рис. 8. Выравнивание концентраций вещества в растворах, разделённых полупроницаемой перегородкой. Ионы через каналы (поры) просачиваются по градиенту концентрации.
Очевидно, что любые доступные способы измерения покажут наличие существенной разницы концентраций (наличие химического градиента) этого вещества по разные стороны перегородки. Убедившись в этом, выдёргиваем стеклянную перегородку. Остаётся только полупроницаемая полимерная мембрана. Очень скоро мы сможем убедиться, что концентрации по обе стороны мембраны начали выравниваться: ионы по градиенту концентрации начали перебираться из более концентрированной среды в менее концентрированную. Понадобилась для этого дополнительная энергия? Нет, достаточным оказалось предоставить системе возможность самостоятельно решить «проблему социальной справедливости» (всех уравнять!), разблокировав каналы утечки. Именно каналы, ведь через них идёт пассивный транспорт, не требующий дополнительной энергии, по градиенту.
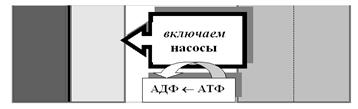
А вот теперь представим себе обратную задачу: нам надо вернуть исходное состояние неравновесия концентраций в нашем аквариуме (рис. 9). Понятно, что без затрат энергии это не получится (попробуйте достать воду из колодца, не прилагая усилий!). Именно поэтому перекачка ионов против градиента концентрации — работа уже не каналов, а насосов, и на эту работу расходуется энергия АТФ (между прочим, электронасос накачает Вам ведро воды мигом, но посмотрите на счётчик — сколько энергии Вы сожгли!).
Рис. 9. Для создания химического градиента требуется приложить энергию. Используя энергию распада АТФ, насосы перекачивают ионы против градиента концентрации.
Мы коснулись чрезвычайно важных моментов в проблеме биоэлектрогенеза. Проанализируем эти два механизма ионного транспорта детальнее. Во-первых, как устроены ионные каналы? Принятая сегодня модель ионного канала основывается на множестве достаточно убедительных, но всё же косвенных измерений. Хочется ещё раз предостеречь читателей от популярного заблуждения: на самом деле очень многое из того, что мы знаем о микроорганизации нейронов (на молекулярном, мембранном уровнях), является результатом мысленных, технических, компьютерных, математических и т.п. реконструкций объектов по многочисленным физико-химическим измерениям; то есть это гипотетические модели объектов, а вовсе не сами объекты, как может показаться из ряда современных книжек. Поэтому используемые повсеместно в нейробиологии словосочетания «селективная пора», «ворота» и т.д. нужно понимать как более или менее удачные метафоры, а не как прямое описание объектов (в данном случае — каналов). Унывать, однако, не вижу оснований: технологическая база исследований развивается очень быстро, и то, что недоступно сегодня, становится рутинной повседневностью завтра. Надеюсь, что скоро сможем убедиться в правильности (или неправильности) модельных реконструкций, в том числе и моделей каналов. Подождём немного?
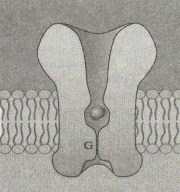
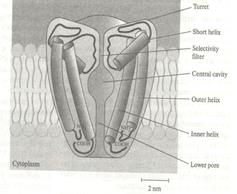
Так вот, согласно принятой сегодня модели ионные каналы — это белковые комплексы, состоящие из нескольких субъединиц — молекул белка (рис. 10). Эти белковые комплексы пронизывают липидную мембрану насквозь, что и позволяет происходить трансмембранному переносу ионов.
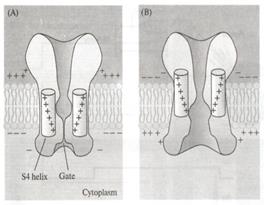
В канале выделяют два функциональных компонента (рис. 11): селективную пору, обеспечивающую выбор (селекцию) тех ионов, которые этот конкретный канал может пропускать, и так называемые ворота, которые обеспечивают дискретность (прерывность) работы канала (как правило, канал активируется только на очень короткий промежуток времени, всё остальное время он закрыт и ионы не пропускает).
Рис. 11. Условная схема, иллюстрирующая работу ионного канала. А — селективная пора, через которую у данного вида канала диффундируют только ионы Na+, тогда как ионы Cl– и K+ сквозь мембрану не проходят. Б — ворота; у данного вида канала в данный конкретный момент времени активационная створка ворот (слева) полуоткрыта, а инактивационная (справа) открыта полностью. Напоминаю, что и селективная пора, и ворота — не более чем относительно удачная метафора.
Нет времени (да и необходимости) рассматривать многочисленные гипотезы, объясняющие тонкие электрохимические механизмы функционирования обоих компонентов канала. Гораздо более важным является то, что эти механизмы обеспечивают высокую специфичность работы каналов. Существуют каналы Na+, K+, Ca2+, Cl– и др., то есть благодаря отбору в селективной поре эти каналы избирательно пропускают только один из перечисленных видов ионов, препятствуя транспорту остальных. Необходимо подчеркнуть, что эта селективность, избирательность не является абсолютной: как и положено живой системе, каналы имеют право на ошибку и могут случайным образом пропускать и «неправильные» ионы, однако их доля в общем ионном токе незначительна. Принято различать высокоселективные каналы (например, на мембране аксона — Na+ или K+) и низкоселективные (например, на постсинаптической мембране — Na+— K+ или Cl– — K+). Воротный механизм (или просто ворота) — второй функциональный компонент ионного канала. Естественно, ворота — это весьма вольная метафора, однако она вполне отражает задачу этого механизма: переводить канал из закрытого состояния в открытое и наоборот — снова
Это очень упрощённая классификация (по транспортируемым ионам и механизму активации). Так как сегодня обнаружено более 150 видов каналов, существуют и более глубинные принципы объединения каналов в группы, учитывающие целый ряд дополнительных факторов, но мы в эти подробности вдаваться не будем.
Единственное, на что хотелось бы обратить внимание, — это существование не только активационных, но и инактивационных ворот. Вопреки бытующему мнению задача этих ворот состоит вовсе не в закрывании ионного канала, а в переводе его в такое состояние, в котором он определённое время не может активироваться. Подобный механизм есть далеко не у всех каналов, но обнаружен, например, у потенциалзависимых Na+-каналов мембраны аксона.
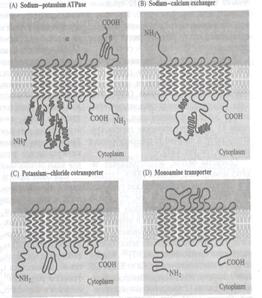
Второй механизм ионного транспорта, который мы обозначили, —активный транспорт с помощью насосов. Мембранных насосов известно много (рис. 14). Они могут иметь разную молекулярную структуру, но функция у них одна и та же: перенос веществ (молекул, ионов, протонов… — не принципиально) против градиента концентрации данного конкретного вещества. Стало быть, такой перенос требует затрат энергии. Как правило, источником энергии является АТФ.
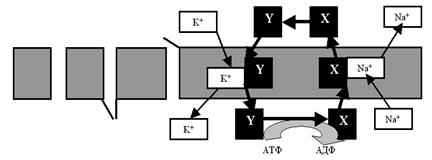
Напомним, что аденозинтрифосфат (АТФ) — уникальный по своей безотказности молекулярный аккумулятор энергии. При расщеплении макроэргических (высокоэнергетичных) связей между остатками фосфорной кислоты и соответственно частичном разрушении молекулы АТФ выделяется поразительное для такой субмикроскопической структуры количество энергии, идущей на «хозяйственные нужды» клетки. При этом аккумулятор, естественно, разряжается (АТФ→АДФ), а на его зарядку (восстановление целостности молекулы АТФ) требуется чуть больше энергии, чем было получено при распаде. Откуда берётся эта энергия? По крайней мере, отчасти мы едим для «зарядки» АТФ (отчасти, потому что с едой мы ещё поставляем клеткам стройматериалы, а иногда ещё и получаем удовольствие), а уж дышим и вообще только ради этого. Но вернёмся к насосам. Попробуем понять принцип их работы на примере так называемой Na+-K+-помпы, которая обеспечивает уже обсуждавшееся нами неравновесие ионов Na и K+ по разные стороны мембраны нейрона. Более или менее убедительно показано, что этот насос представляет собой достаточно тяжёлый белок, обладающий, как минимум, двумя активными конформациями, в одной из которых (назовём её X) он имеет повышенное сродство к ионам Na+, а в другой (пусть будет Y) — к ионам K+. На рис. 15 показана очень упрощённая схема работы Na+-K+-помпы.
Рис. 15. Условная схема, иллюстрирующая механизм работы ионного насоса. В качестве примера представлена Na+-K+-помпа. Объяснения в тексте.
В подмембранном пространстве белок-транспортер в конформации X связывается с ионом Na+ и переносит его на наружную поверхность возбудимой клетки (при этом удаётся «обмануть» градиент Na+, который, как вы помните, направлен внутрь). Там белок расстаётся с Na+ и переходит в конформационное состояние Y. Теперь «на борт» берётся уже ион K+ (снова обманут градиент, ведь K+ транспортируется через мембрану в связанном с белком виде — это другое вещество, совсем не K+!), и челнок ныряет внутрь клетки. Здесь — скорое расставание с K+ и возвращение в конформацию X. Круг (цикл) замкнулся. А куда же уходит энергия АТФ? Вспомните, мы говорили о том, что у белков определённому уровню внутренней энергии соответствует определённое конформационное состояние. Отсюда и решение обратной задачи: если конформация изменилась, значит, что-то произошло с энергетикой белковой молекулы, то есть энергия АТФ расходуется на конформационные изменения.
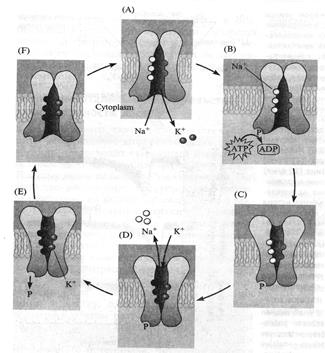
И вот здесь очередная демонстрация фантастического совершенства жизни: оказывается, энергетической подпитки требует только переход Y®X (внутри клетки), а обратное изменение конформации (X®Y) происходит самопроизвольно. Объяснение очевидно: состояние Y энергетически более выгодно для данного белка-транспортера (в этом конформационном состоянии у него меньше свободной энергии, он менее возбуждён), чем состояние X. Таким образом, получается, что энергия АТФ тратится только на внутриклеточный переход Y®X. Мало того, работа помпы настолько экономична, что одна молекула АТФ обеспечивает перекачку через мембрану сразу 5 ионов (3+2), то есть 2,5 «оборота» насоса. Этому способствует и так называемая электрогенность насоса, его способность использовать, кроме АТФ, и энергию электрических зарядов, формирующихся на мембране. Если после чтения предыдущей пары страниц Вам всё ещё кажется, что такое объяснение работы насоса слишком уж мудрено, взгляните на рис. 16: идея-то та же, просто графически представлена в другом, уже знакомом Вам виде. Думаю, Вы без труда сами проследите всю цепочку событий. Только ещё раз прошу не забывать, что это всего лишь более или менее правдоподобные модели: не будете же Вы всерьёз думать, что ионы так похожи на шарики для пинг-понга?!
Рис. 16. Ещё одна иллюстрация на тему Na+-K+-помпы. Попробуйте самостоятельно пройти по всему циклу A-B-C-D-E-F-A.
|
|||||||||||||||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 215; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.34.146 (0.023 с.) |