Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вторичные энзимопатии. Измерение активности ферментов с целью диагностики болезней.Стр 1 из 24Следующая ⇒
Билет 1
Вторичные энзимопатии. Измерение активности ферментов с целью диагностики болезней. Вторичные энзимопатии являются следствием тех или иных патологических процессов, сопровождающихся нарушением активности ферментов. Все инфекционные болезни (вирусные, бактериальные) протекают с растройством ферментных систем, что связано с выделением экзо- и эндотоксинов, блокирующих ряд ферментов. Другой причиной является гипо- и гиперфункция эндокринных желез. Также причиной может быть резкое изменение условий среды, в которой работает фермент (ацидоз или алкалоз).
Энзимодиагностика: используется достаточно ограниченный набор ферментов для небольшого числа болезней. Уровень липазы, амилазы, трипсина и химотрипсина резко увеличен при диабете, злокачественных поражениях поджелудочной железы, болезнях печени и др. При инфаркте миокарда - резкое повышение в сыворотке крови аминотрансфераз, креатинкиназы и лактатдегидрогеназы. Бета-Окисление жирных кислот. Последовательность реакций. Энергетическое значение. 1) Активация жирной кислоты: R-CO-S-KoA + АТФ = R-CO-S-Koa + АМФ + ФФн (ацил-Коа-синтаза);
2) Перенос в матрикс митохондрий: R-CO-S-Koa + (CH3)3N(+)-CH2(OH)-CH2-COOH (карнитин) =(обратимая)= HS-KoA + (CH3)3N(+)-CH2-CH-O-C(OR)-CH2-COOH (ацилкарнитин в цитоплазме) (карнитинацил-трансфераза (ц));
3) Расщепление ацилкарнитина в митохондрии: (CH3)3N(+) - CH2-CH-O-C(OR)-CH2-COOH + HS-KoA =(обратимая)= R-CO-S-Koa + (CH3)3N(+)-CH2(OH)-CH2-COOH (карнитинацил-трансфераза (м));
4) Окисление ацил-КоА в митохондриях (первая стадия дегидрирования): R-CH2-CH2-CH2-CO-S-Koa + ФАД =(обратимая)= R-CH2-CH = CH-CO-S-Koa (еноил-КоА) + ФАДН2 (ацил-КоА-дегидрогеназа);
5) Стадия гидратации: R-CH2-CH=CH-CO-S-Koa + Н2О =(обратимая)= R-CH2-CH(ОН)-CH2-CO-S-Koa (бетта-оксиацил-КоА (3-оксиацил-КоА) (еноил-КоА-гидратаза);
6) Вторая стадия дегидрирования: R-CH2-CH(ОН)-CH2-CO-S-Koa + НАД+ =(обратимая)= R-CH2-CО-CH2-CO-S-Koa (бетта-кетоацил-Коа (3-оксоацил-КоА) + НАДН2 (3-оксиацил-КоА-дегидрогеназа);
7) Тиолазная реакция: R-CH2-CО-CH2-CO-S -Koa + HS-KoA =(обратимая)= R-CH2-CО-CO-S-KoА (снова вовлекается в бетта-окисление) + CH3-CO-S-KoA (идет в ЦТК) (ауетил-КоА-ацил-трансфераза).
((n/2)-1) - циклы окисления. [((n/2)-1)*5+((n/2)*12)]-1 = энергия
Билет 2
Реакции трансаминирования, ферменты, их коферментная группа. Биологическое значение реакций. Определение аминотрансфераз с диагностической целью.
Трансаминирование - реакции межмолекулярного переноса аминогруппы от аминокислоты на альфа-кетокислоту без промежуточного образования аммиака. Эти реакции протекают при участии специфических ферментов - аминотрансфераз. В переносе аминогруппы активное участие принимает кофермент трансаминаз - пиридоксальфосфат (производное витамина В6), который в процессе реакции обратимо превращается в пиридоксаминфосфат. Для реакций трансаминирования характерен общий механизм. Ферменты трансаминирования катализируют перенос амино-группы не на альфа-кетокислоту, а сначала на кофермент - пиридоксальфосфат. Образуется альфа-кетокислота и пиридоксаминфостфат, который взаимодействует с любой другой альфа-кетокислотой, что приводит к синтезу новой а/к и освобождению пиридоксальфосфата. 1) R1-CH(NH2)-COOH + O=CH-ПФ = R1-CO-COOH + H2N-CH2-ПФ 2) H2N-CH2-ПФ + R2-CO-COOH = O=CH-ПФ + R2-CH(NH2)-COOH Для клинических целей наибольшее значение имею две трансаминазы сыворотки крови: АсАТ (аспартат) и АлАТ (аланин). В сыворотке крови здоровых людей активность этих трансфераз гораздо ниже, чем в паренхиматозных органах. Поэтому при деструктивных поражениях органов происходит выход трансаминаз из очага поражения в кровь. При инфаркте миокарда уровень АсАТ сыворотки крови уже через 3-5 ч после инфаркта резко повышается (в20-30 раз). В клинике трансаминазный тест используется не только для постановки диагноза, но и для проверки эффективности метода лечения. При гепатите также наблюдается гипертрансаминаземия (за счет преимущественного повышения уровня АлАТ).
Взрослые - 65-85 г/л Лет - 58-76 г/л У этого ребёнка снижено содержание общего белка в крови, что может быть связано с болезнями ЖКТ (панкреатит, патологии печени) или же с ожогами или иными серьёзными травмами.
Билет 3
Билет 4
1. Понятие об изоферментах (на примере лактатдегидрогеназы и креатинкиназы). Изоферменты - множественные формы фермента, отличающиеся по сродству, максимальной скорости катализируемой реакции (активности) или регуляторным свойствам.
Фермент ЛДГ катализирует превращение пвк в молочную. Существует 5 изоферментов ЛДГ - в сердечной мышце ЛДГ1; в почках - ЛДГ1 (ЛДГ2 и 3); печень и скелетные мышцы - ЛДГ5. Фермент креатинкиназа представлен тремя изоферментными формами, составленными из двух типов субъединиц˸ M (мышца) и B (мозг). Креатинкиназа-1 состоит из субъединиц типа B и локализуется в головном мозге; креатинкиназа-2 – по одной М и В субъединице, активна в миокарде; креатинкиназа-3 содержит две М-субъединицы, специфична для скелетной мышцы.
Билет 7 Билет 8 Билет 9 Кетоновые тела в моче. Ответ: Кетоновые тела представлены группой соединений, в которую входят ацетон, бета-гидроксимасляная и ацетоуксусная кислота. В организме они служат резервным поставщиком энергии, расщепляются при нехватке глюкозы в плазме или при недостаточном количестве инсулина. В таких случаях для обеспечения функционирования клеток начинает использоваться жировая ткань. Жирные кислоты поступают в печень, где превращаются в ацетоацетат (уксусную кислоту) и бета-гидроксибутират (бета-гидроксимасляную кислоту) – соединения, способные проходить через гематоэнцефалический барьер и служить источником энергии для клеток организма. Часть из них преобразуется в ацетон, который выводится через почки, легкие и пищеварительный тракт. Кетоны в моче в основном представлены ацетоном. Повышение его уровня называется кетонурией и свидетельствует о недостатке глюкозы и/или инсулина. Такое состояние свидетельствует о нарушении углеводного обмена и развивается при голодании, интенсивной нагрузке на мышцы, длительном стрессе, инфекциях, сахарном диабете.
Билет 10
Про желудочный сок. Ответ (ну, тут я вообще хз, распишу всё): Нормы: Концентрация соляной кислоты в желудке - 160 ммоль/л. рН желудочного сока (верхняя зона) – 1,5-2,3 Общая кислотность – 40-60 титр. ед. Уровень свободной соляной кислоты – 20-40 титр. ед. Количественные изменения желудочной секреции выражаются в форме гиперсекреции и гипосекреции желудочного сока. Качественные изменения проявляются: 1) в повышении кислотности сока – гиперацидитас или гиперхлоргидрия 2) в понижении кислотности сока - гипоацидитас или гипохлоргидрия, 3) в отсутствии соляной кислоты - анацидитас или ахлоргидрия. Гиперсекреция желудочного сока обычно сопровождается повышением кислотности сока и количества пепсиногенов в нем, то есть гиперхилией, проявляющейся увеличением переваривающей способности сока. ↑ HCl: Ø При функциональных расстройствах ЦНС Ø Действие других органов (рефлекторно) Ø Органические изменения слизистой (язва) Ø Гипертрофический гастрит (острый или хронический) Общая кислотность у взрослого человека при этом становится выше 60 титр. ед., а свободная соляная кислота – выше 40 титр. ед. Гипосекреция желудочного сока обычно характеризуется снижением кислотности сока и количества пепсиногенов в нем, вплоть до полного их отсутствия – ахилии. Это приводит к уменьшению или полному исчезновению переваривающей способности сока. Гипосекреция · Общая кислотность – ниже 30 единиц (иногда снижается до 10-20 ед) · Свободная HCl – может быть до 0 ед. · Бывает при хронической и реже при остром гастритах
· Часто зависит от нарушения ЦНС (депрессивная травма) К наиболее тяжелым нарушениям секреторной деятельности желудка относится ахилия, т.е. полное отсутствие секреции желудочного сока. Ахилия может быть, как функционального, так и органического происхождения.
Билет 11
Билет 12 Общий белок крови 50 г/л. Ответ (см. билет 2): норма белка: Взрослые - 65-85 г/л Лет - 58-76 г/л У пациента снижено содержание общего белка в крови, что может быть связано с болезнями ЖКТ (панкреатит, патологии печени) или же с ожогами или иными серьёзными травмами.
Билет 13 Гиповитаминозы Нехватка витаминов ведет к развитию патологических процессов в виде специфических гиповитаминозов или авитаминозов. Широко распространенные скрытые формы витаминной недостаточности не имеют ярко выраженных внешних проявлений и симптомов, но оказывают отрицательное влияние на работоспособность, общий тонус организма и его устойчивость к разным неблагоприятным факторам.
Гипервитаминозы Жирорастворимые витамины при увеличении дозы накапливаются и могут вызывать гипервитаминозы с рядом общих симптомов (потеря аппетита, расстройство ЖКТ, сильные головные боли, повышенная возбудимость нервной системы, выпадение волос, шелушение кожи) и со специфическими признаками. Яркая картина гипервитаминозов отмечается только для витаминов А и D.
Билет 14 Билет 15 Вопрос не знаю. Ответ: нет лактазы. Лактаза - это фермент из семейства β-галактозидаз, лактаза гидролизует гликозидные связи и принимает участие в гидролизе дисахарида лактозы, содержащейся в молоке. У человека лактаза в основном экспрессируется в энтероцитах кишечника и располагается на плазматических мембранах дифференцированных энтероцитов тонкой кишки. Недостаточность лактазы приводит к непереносимости лактозы. Билет 16 Билет 17 Итог: 20 – 30г/л. Показатель повышен. Причины повышения: (всего подряд) - острые или хронические воспалительные заболевания; - цирроз печени; - язвенная болезнь; - беременность; - стресс; - сахарный диабет;
Билет 18 Билет 19 Этап (окислительный) 1) Глюкозо-6-ф-т = 6-фосфоглюконо-дельта-лактон (глюкозо-6-фДГ) НАДФ+ до НАДФН2; 2) 6-фосфоглюконо-дельта-лактон = 6-фосфоглюконат (6-ф-гл-лактоназа) + Н2О;
3) 6-фосфоглюконат = рибулозо-5-ф-т (6-ф-глюконатДГ) НАДФ+ до НАДФН2; 4) Р-5-ф-т =(обратимая)= рибозо-5-ф-т (изомераза)/ р-5-ф-т=(обратимая)= ксилулозо-5-ф-т (эпимераза); Билет 20 Билет 21 1. Четвертичная структура белков. Особенности строения на примере гемоглобина. Кооперативность изменения конформации протомеров. Четвертичная структура белков - способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой или разной первичной, вторичной и третичной структурой, и формирование единого в структурном и функциональном отношениях макромолекулярного образования. Молекула гемоглобина состоит из двух α- и двух β-полипептидных цепей, т.е. представляет собой тетрамер. Каждая из этих полипептидных цепей окружет группу гема (пигмента, придающего кови ее характерный расный цвет). Кооперативные изменения конформации протомеров. Так как протомер связан с остальными протомерами, а белки обладают конформационной лабильностью, происходит изменение конформации всего белка. Конформационные изменения, произошедшие в других протомерах, облегчают присоединение следующей молекулы кислорода,что вызывает новые конформационные изменения в белке и ускорение связывания следующей молекулы кислорода.Четвертая молекула кислорода присоединяется к гемоглобину в 300 раз легче первой. Изменение конформации (а следовательно и функциональных свойств) всех протомеров олигомерного белка при присоединение лиганда только к одному из них носит название кооперативного изменения конформации протомеров. Билет 22 Кальций 2,1 ммоль/л. Ответ: Норма кальция в крови взрослого человека - 2,15 - 2,5 ммоль/л. Гипокальциемия. Причины: - низкий уровень паратиреоидного гормона (гипопаратиреоз), который возникает при поражении паращитовидных желез - расстройство функции почек, которое приводит к повышенному выведению кальция с мочой - недостаточное потребление кальция; - заболевания, которые снижают всасывание кальция.
Билет 23 Билет 24
Билет 25
Типы РНК: особенности строения, локализация в клетке, функции. Образование аминоацил - тРНК. Биосинтез РНК (транскрипция). мРНК - синтезируется в ядре на матрице ДНК и поступает в рибосому, выполняя матричную функцию при синтезе белка; тРНК - перенос аминокислот к месту белкового синтеза; рРНК - содержатся в малой и большой субъединицах рибосом.
Особенности строения РНК заключаются в том, что РНК - одноцепочечная молекула и набор нуклеотидов в ней несколько отличается от ДНК - вместо тимина урацил, и углевод РНК - рибоза.
Образование аминоацил-тРНК.
1.аминокислота + АТФ → аминоацил-АМФ + ФФн — АТФ активирует аминокислоту 2.аминоацил-AМФ + тРНК → аминоацил-тРНК + АМФ — активированная аминокислота соединяется с соответствующей тРНК Суммарное уравнение двух реакций: аминокислота + тРНК + АТФ → аминоацил-тРНК + АМФ + ФФн
Пониженный гемоглобин.
Ответ: Норма: женщины – 115-145 г/л мужчины – 130-160 г/л Низкий уровень гемоглобина может свидетельствовать о железодефицитной анемии или кровопотере. Билет 26 Сниженная плотность мочи. Ответ: норма плотности - 1,018 - 1,025 г/л. Гипостенурия – низкая плотность мочи (ни в одной из порций плотность мочи не превышает 1,012–1,013 г/мл) указывает на нарушение концентрационной способности почек, причиной может быть: хроническая почечная недостаточность; сердечная недостаточность; несахарный диабет.
Билет 27 Холестерин 6,5 ммоль/л. Ответ: норма - 2,8-5,2 ммоль/л. Наблюдается гиперхолистеринэмия. Причины: - ожирение (индекс массы тела более 30); - злоупотребление продуктами, содержащими трансжиры, холестерин и жиры животного происхождения; - малоподвижный образ жизни; - курение и алкоголь; - болезни печени; - сахарный диабет; - повышенное артериальное давление.
Билет 29 Билет 30 1. АТФ и другие высокоэнергетические соединения, пути образования и использования АТФ. Образование АТФ в процессе метаболизма идет двумя путями – окислительного и субстратного фосфорилирования. (дых цепь ЦТК гликолиз). Возникновение макроэргической связи в момент окисления субстрата с дальнейшей активацией неорганического фосфата и его переносом на АДФ с образованием АТФ называют субстратным фосфорилированием(10% всей энергии). Реакцией субстратного фосфорилирования являются две реакции гликолиза – окисление 3-фосфоглицеринового альдегида в 1,3-дифосфоглицериновую кислоту, и окисление 2-фосфоглицериновой кислоты в 2-фосфоэнолпировиноградную кислоту; а также одна реакция ЦТК - окисление сукцинил-КоА в янтарную кислоту. Основная масса АТФ образуется путем окислительного фосфорилирования. В процессе окислительного фосфорилирования окисляемый субстрат участия не принимает, а активирование неорганического фосфата сопряжено с переносом электронов и протонов водорода с коферментов дегидрогеназ (принимающих участие в окислении субстрата) к молекулярному кислороду. Сопряжение окисления с фосфорилированием АДФ и последующим образованием АТФ называют окислительным фосфорилированием. Процессы сопряжения окисления и фосфорилирования идут в дыхательной цепи. Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов. Всё это реакции синтеза сложных веществ в организме: осуществление активного переноса молекул через биологические мембраны, в том числе и для создания трансмембранного электрического потенциала; осуществления мышечного сокращения. Помимо энергетической АТФ выполняет в организме ещё ряд других не менее важных функций: · Вместе с другими нуклеозидтрифосфатами АТФ является исходным продуктом при синтезе нуклеиновых кислот. · Кроме того, АТФ отводится важное место в регуляции множества биохимических процессов. Являясь аллостерическим эффектором ряда ферментов, АТФ, присоединяясь к их регуляторным центрам, усиливает или подавляет их активность. · АТФ является также непосредственным предшественником синтеза циклического аденозинмонофосфата — вторичного посредника передачи в клетку гормонального сигнала. · Также известна роль АТФ в качестве медиатора в синапсах. У прокариот существует несколько типов богатых энергией химических соединений. Самую большую группу составляют соединения с высокоэнергетической фосфатной связью: ацилфосфаты, фосфорные эфиры енолов (фосфоенолпируват), нуклеотидди- и трифосфаты, аденозинфосфосульфат. Другая распространенная группа — соединения с высокоэнергетической тиоэфирной связью — ацилтиоэфиры. Задача про фосфаты в крови. Ответ: Фосфаты в сыворотке крови являются буфером для поддержания кислотно-щелочного баланса. Большая часть фосфора в сыворотке крови находится в фосфатах. Его концентрация зависит от реабсорбции фосфатов в почечных канальцах, а также от процессов резорбции и синтеза костной ткани. Уровень фосфора регулируется паратгормоном, витамином D и кальцитонином. Дефицит фосфора в организме может быть следствием нарушения кислотно-щелочного баланса, неполноценной диеты, гиперкальциемии, синдрома мальадсорбции и другие факторов, нарушающих работу почек. Гиперфосфатемия возникает из-за избыточного поступления микроэлемента с пищей, гипокальциемии, а также вследствие поражения почек.
Билет 31 Билет 32 Про плотность мочи. Ответ: норма плотности - 1,018 - 1,025 г/л. Гипостенурия – низкая плотность мочи (ни в одной из порций плотность мочи не превышает 1,012–1,013 г/мл) указывает на нарушение концентрационной способности почек, причиной может быть: - хроническая почечная недостаточность; - сердечная недостаточность; - несахарный диабет. Гиперстенурия - относительная плотность мочи больше чем 1,026 г/мл. Причины: - острый гломерулонефрит - сахарного диабета
Билет 33
Остаточный азот 0,8 г/л. Ответ: Норма остаточного азота - 12,5 – 25,0 ммоль/л или - 20 – 40 мг/100мл = 0,2-0,4 г/л. (билет 4) Повышение остаточного азота в крови - азотемия. Азотемия в зависимости от вызывающих ее причин подразделяется на ретенционную и продукционную. Ретенционная азотемия развивается в результате недостаточного выделения с мочой азотсодержащих продуктов при нормальном поступлении их в кровяное русло. Ретенционная может быть почечной (нарушение работы почек, уменьшение выделения азота с мочой) и внепочечная (снижение АД, недостаток кровоснабжения из почечной артерии). Продукционная азотемия развивается при избыточном поступлении азотсодержащих продуктов в кровь, как следствие усиленного распада тканевых белков при обширных воспалениях, ранениях, ожогах, кахексии и др. Нередко наблюдаются азотемии смешанного типа.
Билет 37 1. Витамины группы В, их коферментная роль, участие в биохимических процессах. Потребность.
2. Гормоны гипоталамуса, их биологическая роль. Гормоны гипоталамуса регулируют секрецию гипофизарных гормонов за счет либеринов и статинов (угнетают высвобождение). Семь стимуляторов (либеринов): кортиколиберин, тиреолиберин, люлилиберин, фоллилиберин, соматолиберин, пролактолиберин, меланолиберин; и три ингибитора (статина): соматостатин, пролактостатин и меланостатин. 3. Этапы аэробного распада глюкозы, энергетика этого процесса. Аэробный распад глюкозы - ферментативный процесс превращения глюкокозы в присутствии кислорода с образованием углекислого газа и этанола. Неокислительная стадия: 11) Глюкоза = глюкозо-6-фосфат (гексокиназа/глюкокиназа в пчени) -1АТФ (АТФ до АДФ); 12) Гл-6-ф = (обратимая)= фруктозо-6-фосфат (глюкозо-6-фосфат изомераза); 13) Фр-6-ф = фр-1,6-дифосфат (фосфофруктокиназа - определяет скорость гликолиза) -АТФ (АТФ до АДФ); 14) Фр-6-диф =(обратимая)= глицеральдегидфосфат (ГАФ) + диоксиацетонфосфат (альдолаза); 15) Диоксиацетонф-т =(обратимая)= ГАФ Окислительная стадия: 16) 2ГАФ =(обратимая)= 2 1,3-бисфосфоглицерат (ГАФ-дегидрогеназа) (присоединяется 2Ф, 2НАД до 2НАДН2); 17) 2 1,3-бисфосфогл-т =(обратимая)= 2 3-фосфогл-т (фосфоглицераткиназа) +2АТФ - субстратное фосфорилирование (2АДФ до 2АТФ); 18) 2 3-фосфогл-т =(обратимая)= 2 2-фосфогл-т (фосфогл-тмутаза); 19) 2 2-фосфогл-т = 2 фосфоенолпируват (енолаза) (прямо -2Н2О, обратно +2Н2О); 20) 2 фосфоенолпир-т = 2 пируват (пируваткиназа) +2АТФ - субстр. фосфорил. (2АДФ до 2АТФ); 21) 2 пируват = 2 ацетальдегид (пируватдекарбоксилаза) - кофермент ТДФ (минус СО2); 22) 2 ацетальдегид =(обратимая)= 2 этанол (алкогольдегидрогеназа) (2НАДН2 до 2НАД+); Итого АТФ = 1. 4. Про мочевину… Ответ: Норма: В крови: Мужчина - 3,2 - 7,3 ммоль/л Женщина - 2,6 - 6,7 ммоль/л В моче (высчитывается клиренс): Взрослые - 428–714 ммоль/сут. Повышенное содержание мочевины может быть связано с сахарным диабетом, онкологическими заболеваниями, тиреотоксикозом. Причины понижения уровня мочевины в крови: - печеночная недостаточность, некоторые заболевания печени - акромегалия (гормональное заболевание, характеризующееся повышенной выработкой соматотропного гормона), - голодание, низкобелковая диета, - нарушение кишечного всасывания - нефротический синдром (повышенное выделение белка с мочой, гиперлипидемия, снижение уровня белка в крови), - повышенная выработка антидиуретического гормона (АДГ) и, как следствие, патологическая гиперволемия, - беременность
Билет 38 Химический состав мочи: Натрий, калий, магний, кальций общий, фосфор неорганический, азот аммиака, хлорид, мочевина, мочевая кислота, креатинин, идикан. Свойства мочи: Количество выделяемой мочи (диурез) дл 2л. Увеличение объема - полиурия - выше 2л (в норме при употребление большого количества жидкости и пищевых веществ, повышающих диурез; при патологии - заболевания почек, сахарный диабет и др. патологические сотояния); уменьшение - олигурия (при недостаточном потреблении жидкости, лихорадочных состояних, рвоте, поносе, токсикозах, остром нефрите ит.д.; прекращение выделения мочи - анурия (при мочекаменных болезнях, отравлениях свинцом, ртутью, мышьяком, при сильных нервных потрясениях); длительная анурия ведет к уремии. Преобладание ночного диуреза над дневным - никтурия. Цвет. В норме колеблется от соломенно-желтого до насыщенного желтого. Зависит от пигментов: урохрома, уробилина, уроэритрина, урозеина и др. При патологии цвет может быть красным (при гематурии и гемоглобинурии, после приема антипирина, амидопирина, сантонина и др.), зеленым (при введении в органим метиленового синего, при поцессах гниения белков в кишечнике), коричневым (высокая концентрация уробилина и билирубина в моче) и т.д. Прозрачность. В норме моча прозрачна. Мутность выывают соли, клеточные элементы, бактерии, слизь и жир. Плотность. В моче содержатся разные вещества. Изостенурия - выделение почками мочи с относительно одинаковой плотностью, равной плотности первичной мочи, или ультрафильтрата (при тяжелой почечной недостаточности). Низкая плотность мочи указывае на нарушение концентрационной функции почек (хронический нефрит, несахарный диабет, олигурия). Высокая плотность - полиурия, сахарный диабет (обусловлена высоким содержанием глюкозы). Реакция мочи (рН). При употреблении преимущественно мясной пищи моча имеет более кислую реакцию, при овощной диете - щелочная. При патологии: резко кислая моча при лихорадочных состояниях, сахарном диабете, голодании ит.д.; щелочная - при циститах и пиелитах, после сильной рвоты, приеме некоторых лекарственных средств, употреблени щелочныхминеральных вод и т.д. Билет 39 Билет 40 Глюкоза в крови 3 ммоль/л. Ответ: норма – 3,3-5,5 ммоль/л. Гипогликемия. Причины: - обезвоживание - передозировка инсулином и иными сахароснижающими препаратами - чрезмерная физическая нагрузка - недоедание
Билет 41 Билет 42 Билет 43 Билет 44 1. Катаболизм основных пищевых веществ - углеводов, жиров, белков. Понятие о специфических путях катаболизма и общих путях катаболизма.
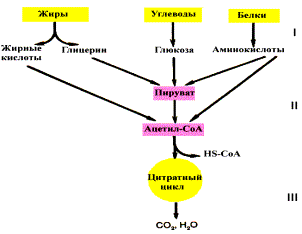
Если процесс катаболизма рассматривать с общей точки зрения, то можно выделить три основные его части: 1. Расщепление в пищеварительном тракте. Это гидролитические реакции, превращающие сложные пищевые вещества в относительно небольшое число простых метаболитов: глюкоза, аминокислоты, глицерин, жирные кислоты. 2. Специфические пути катаболизма. Простые метаболиты подвергаются специфическим реакциям расщепления, в результате которых образуется либо пировиноградная кислота, либо ацетил — КоА. Причем ацетил — КоА может образоваться из пирувата в результате окислительного декарбоксилирования. Могут также образоваться другие соединения, непосредственно включающиеся в цитратный цикл. 3. Цитратный цикл и дыхательная цепь завершают расщепление пищевых веществ до конечных продуктов — СО2 и Н2О. Следовательно, начиная со стадии образования пирувата происходит унификация путей катаболизма. Из большого числа исходных соединений образуется всего два — пируват и ацетил — СоА. Процесс, начинающийся от пирувата, называется общим путем катаболизма и в свою очередь включает: 1. окислительное декарбоксилирование пирувата 2. цитратный цикл. Именно в общем пути катаболизма образуется основная масса субстратов для реакций дегидрирования. Совместно с дыхательной цепью и окислительным фосфорилированием общий путь катаболизма является основным источником энергии в форме АТР. Холестерин 6,1 ммоль/л Ответ (как билет 28): норма - 2,8-5,2 ммоль/л. Наблюдается гиперхолистеринэмия. Причины: - ожирение (индекс массы тела более 30); - злоупотребление продуктами, содержащими трансжиры, холестерин и жиры животного происхождения; - малоподвижный образ жизни; - курение и алкоголь; - болезни печени; - сахарный диабет; - повышенное артериальное давление.
Билет 45
1. Классификация и номенклатура ферментов (привести примеры). По типу катализируемой реакции. Оксидоредуктазы - ок-но-вос-ые реакции. (окисление перикиси до воды и кислорода при участии каталазы); Трансферазы - межмолекулярный перенос различных атомов, групп атомов и радикалов (глицерин + атф = глицерофостфат + адф - фосфоглицерокиназа); Гидролазы - расщепление внутримолекулярных связей органических веществ при участии молекулы воды (гидролиз) (крахмал под действием амилазы до глюкозы); Лиазы - разрыв С-С, С-О, С-N и других связей, а также обратимые реакции отщепления различных групп от субстратов не гидролитическим путем. Эти реакции сопровождаются образованием = связи или присоед-м групп к месту = связи. (малат + НАДН+ = оксалоац. + НАДН2 при уч-и малатдегидрогеназы); Изомеразы - изомеризация или внутримолекулярный перенос групп (в данном случае ферменты называются мутазы) (глюкозо-6-фосфат до глюкозо-1-фосфат под действием фосфоглицеромутазы); Лигазы (синтетазы) - синтез органических веществ из двух исходных молекул с использованием энергии распада АТФ (ацетил-КоА + СО2 + АТФ = малонил-КоА + Н4Р2О7). Свободная соляная кислота Свободной соляной кислотой называется соляная кислота, находящаяся в желудочном соке в виде отдельных ионов H+ и Cl-. Для определения свободной кислотности к 5 мл желудочного сока добавляют одну каплю диметиламидоазобензола. Отметив уровень раствора в мерной пробирке, производят титрование желудочного сока до появления оранжево-жёлтого цвета. Количество мл едкого натра, потраченного на титрование, умноженного на 20, будет равно свободной кислотности. Связанная соляная кислота Связанной соляной кислотой называется соляная кислота, находящаяся в желудочном соке в химически связанном с белками и в недиссоциированном виде. Для определения связанной соляной кислоты используют индикатор ализарин. Процедура титрования аналогична описанным выше и проводится до появления фиолетового окрашивания.
Билет 47 Билет 48 Билет 49 Билет 50 Билет 1
Вторичные энзимопатии. Измерение активности ферментов с целью диагностики болезней. Вторичные энзимопатии являются следствием тех или иных патологических процессов, сопровождающихся нарушением активности ферментов. Все инфекционные болезни (вирусные, бактериальные) протекают с растройством ферментных систем, что связано с выделением экзо- и эндотоксинов, блокирующих ряд ферментов. Другой причиной является гипо- и гиперфункция эндокринных желез. Также причиной может быть резкое изменение условий среды, в которой работает фермент (ацидоз или алкалоз).
Энзимодиагностика: используется достаточно ограниченный набор ферментов для небольшого числа болезней. Уровень липазы, амилазы, трипсина и химотрипсина резко увеличен при диабете, злокачественных поражениях поджелудочной железы, болезнях печени и др. При инфаркте миокарда - резкое повышение в сыворотке крови аминотрансфераз, креатинкиназы и лактатдегидрогеназы.
|
||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 125; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.122.4 (0.238 с.) |