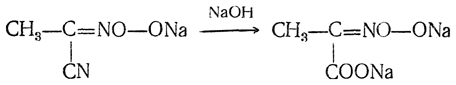Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нитросоединения. Номенклатура
Нитросоединениями называют вещества, содержащие в молекуле одновалентный остаток азотной кислоты, или нитрогруппу, — NO2. В настоящее время нитрогруппе приписывают строение
не отражающее, однако, экспериментально доказанной симметричности этой группы. Равноценность обоих атомов кислорода нитрогруппы лучше отражает формула согласно которой электронная плотность равномерно распределена между обоими кислородными атомами. Можно предположить, что нитрогруппа образуется из нитрозогруппы таким образом: атом азота нитрозогруппы несет свободную пару электронов и при взаимодействии с атомом кислорода, обладающим тремя парами валентных электронов, он отдает эту свободную пару на образование ковалентной связи с кислородом, получающим теперь полный октет электронов. Однако атом азота на создание такой валентной связи затратил не один электрон из своей внешней оболочки, как это происходит при возникновении обычной ковалентной связи, а два и таким образом, очевидно, приобрел один положительный элементарный заряд; атом же кислорода не только не отдал ни одного электрона для образования связывающего его с азотом дублета, но получил при этом один электрон свободной пары азота, т. е. приобрел один элементарный отрицательный заряд. Таким образом, новая связь между кислородом и азотом оказывается одновременно и ионной и ковалентной, т. е. это — типичная семиполярная связь (ср. стр. 105):
В сложных эфирах азотистой кислоты R—О—NO содержится изомерный нитрогруппе одновалентный остаток —О—N=О, т. е. нитросоединения изомерны эфирам азотистой кислоты. Номенклатура Названия нитросоединений производятся от названий соответствующих углеводородов добавлением приставки нитро, например: нитрометан CH3NO2, нитроэтан CH3CH2NO2, α-нитропропан CH3CH2CHNO2, β-нитропропан
и т. д. По женевской номенклатуре, названия нитросоединений строятся так же, но положение нитрогруппы обозначается не греческой буквой, а цифрой: 1-нитропропан, 2-нитропропан. В зависимости от характера алкила, с которым связана нитрогруппа, различают первичные, вторичные и третичные нитросоединения. Способы получения 1. Нитрование парафиновыхуглеводородов Нитросоединения могут быть получены действием азотной кислоты на парафиновые углеводороды (М. И. Коновалов). Нитрование парафиновых углеводородов в газовой фазе при температурах 150—475° С совершается довольно гладко, и в настоящее время осуществляется в промышленности.
Процессы газофазного нитрования парафинов при высоких температурах вероятнее всего идут (А. И. Титов) с участием свободных радикалов:
В качестве побочных продуктов возможно также образование эфиров азотистой кислоты:
2. Действие солей азотистой кислоты Наиболее обычным способом синтеза нитросоединений парафинового ряда является действие солей азотистой кислоты на галоидные алкилы (В. Мейер, 1872) или сложные эфиры серной кислоты:
Для получения нитросоединений из галоидных алкилов обыкновенно применяется нитрит серебра. Так как азотистой кислоте и ее солям обычно придается строение с трехвалентным атомом азота, то при указанных реакциях естественно было бы ожидать образования эфиров азотистой кислоты R—O—N=O. Они отчасти и получаются; образование же нитросоединений обыкновенно объясняют тем, что наряду с реакцией обмена здесь идет сначала реакция присоединения галоидного алкила, а затем отщепления галоидной соли:
Нитросоединения благодаря значительно более высокой температуре ихкипения могут быть отделены от образующихся одновременно с ними эфиров азотистой кислоты. 3. Действие нитритов на α-галоидзамещенные карбоновые кислоты. Первичные и вторичные нитросоединения могут быть получены действием нитрита натрия или калия в водном растворе на галоидзамещенные карбоновые кислоты с атомом галоида в α-положении. При этом сначала образуются нитрокарбоновые кислоты, которые при кипячении с водой разлагаются, давая нитропарафины, например:
4. Конденсация нитрилов с алкилнитратами Первичные нитросоединения можно получать из нитрилов, имеющих метиленовую группу рядом с нитрильной группой, конденсацией с эфирами азотной кислоты под действием этилата натрия (Вислиценус, 1902). При этом образуются изонитросоединения.
которые сначала гидролизуются избытком щелочи
а затем при подкислении превращаются в нитропарафины:
5. Окисление аминов Третичные нитросоединения могут быть получены из аминов, у которых аминогруппа стоит при третичном углеродном атоме, окислением надсерной кислотой (Бамбергер, 1903):
|
||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 95; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.104.120 (0.006 с.) |