Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Г ликолитическая оксиредукция
Процесс циклического восстановления и окис-
ления НАД в реакциях анаэробного гликолиза полу-
чил название гликолитическая оксиредукция.
В анаэробных условиях образуемый в шестой, ГАФ-дегидрогеназной реакции, НАДН используется
в последней реакции для восстановления пирувата до лактата. Образуемый таким образом НАД опять возвращается в шестую реакцию. В аэробных условиях НАДН отдает свои атомы водорода на челночные систе-
мы (см ниже)для их передачи в дыхательную цепь митохондрий.
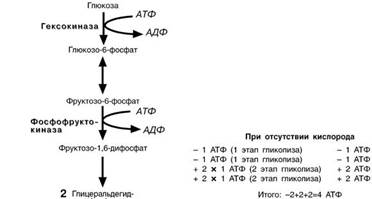
Э НЕРГЕТИЧЕСКИЙ ЭФФЕКТ ОКИСЛЕНИЯ ГЛЮКОЗЫ
На подготовительном этапе
на активацию глюкозы затра-
чивается 2молекулы АТФ,ка-ждая из которых оказывается на триозе – глицеральдегид-
фосфате и диоксиацетонфос-фате. В следующий второй этап входит только глицераль-
дегидфосфат, но его уже две молекулы, каждая из которых окисляется до пирувата с об-
Разованием 2-х молекул АТФ
в реакциях субстратного фос-
форилирования. Таким обра-
зом, суммируя, получаем, что
на пути от глюкозы до пирувата
в чистом виде образуется 2
молекулы АТФ.
Однако надо иметь в виду
и глицеральдегидфосфат-
дегидрогеназную реакцию, из которой выходит НАДН. Если условия анаэробные, то он
используется в лактатдегидро-геназной реакции – окисляется для образования лактата и в
получении АТФ не участвует.
Если же имеется кислород
– НАДН направляется в мито-хондрию, на процессы окисли-
тельного фосфорилирования, и
там его окисление приносит дивиденды в форме АТФ.
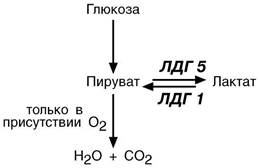
Э ФФЕКТ П АСТЕРА
Эффект Пастера – это снижение потребления глюкозы и прекращение продукции молочной кислоты клеткой в присутствии кислорода.
Луи Пастер, занимавшийся вопросами виноделия, наблюдал подобный фено-мен при производстве вина. Забегая вперед, отметим, что спиртовое броже-ние весьма похоже на гликолиз, только вместо молочной кислоты из пирува-та образуется спирт.
Биохимический механизм эффекта Пастера заключается в конкуренции между
пируватдегидрогеназой,превращающей пируват в ацетил-S-КоА,и лактатдегид-
рогеназой,превращающей пируват в лактат.При отсутствии кислорода внутрими-тохондриальные процессы дыхания не идут, цикл трикарбоновых кислот тормозится
и накапливающийся ацетил-S-КоА ингибирует ПВК-дегидрогеназу. В этой ситуации
пировиноградной кислоте не остается ничего иного как превращаться в молочную. При наличии кислорода ингибирование ПВК-дегидрогеназы прекращается и она, об- ладая большим сродством к пирувату, выигрывает конкуренцию.
Важно то, что пировиноградная кислота является для клетки токсичным
веществом, и клетке необходимо избавиться от нее каким угодно образом. Так как через мембраны она не проходит, то обезвреживание достигается превращением пирувата 1) в лактат; 2) в ацетил- S -КоА; 3) в аланин (см "Ала-нинаминотрансфераза"), 4) в оксалоацетат.
Иллюстрацией к сказанному служит от-личие изоферментов лактатдегидроге-наз (ЛДГ) друг от друга. Сердечный
изофермент ЛДГ-1 обладает высоким сродством к молочной кислоте и "стре- мится" поднять концентрацию пирува-та с целью его включения в ЦТК и полу-чения энергии для деятельности мио- карда. Большое количество митохонд- рий и поступление сюда лактата из других органов обеспечивает работу сердца при аэробных условиях. При не-хватке кислорода свойства ЛДГ-1 не из- менятся, он по-прежнему будет сдвигать реакцию в сторону продукции пиро- виноградной кислоты. Изофермент скелетной мышцы ЛДГ -5 обладает высо-ким сродством к пирувату, при отсутствии кислорода в клетке быстро и эффективно превращает его в лактат, легко проникающий сквозь мембраны. Таким образом, в анаэробных условиях сильнее будет страдать сердечная мышца, что, собственно говоря, и наблюдается в медицинской практике.
Ч ЕЛНОЧНЫЕ СИС-ТЕМЫ
Челночные системы –
механизм доставки обра- зованных в гликолизе ио- нов Н+ (в составе НАДН) из цитозоля в митохонд-рию. Так как сама молекула
НАДН через мембрану не проходит, природа поза- ботилась о том, чтобы
создать системы, прини-
мающие этот водород в цитоплазме и отдающие его в матриксе митохонд-рий.
Определены две основные челночные системы – глицеролфосфатная и малат-
аспартатная.
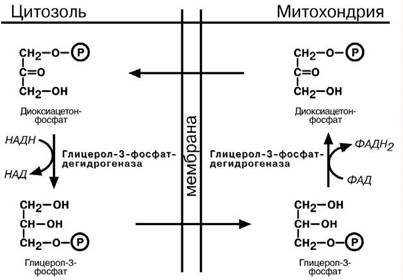
Глицеролфосфатный челнок активен в печени и в быстрых мышечных волок-нах. Его ключевыми ферментами являются изоферменты глицерол-3-фосфат- дегидрогеназы, цитоплазматический и митохондриальный. Они отличаются своими
коферментами: у цитоплазматической формы – НАД, у митохондриальной – ФАД. Метаболиты гликолиза – диоксиацетонфосфат и НАДН образуют глицерол-3- фосфат, поступающий в матрикс митохондрий, где он окисляется с образованием
ФАДН 2. Далее ФАДН2 направляется в дыхательную цепь и используется для полу-чения энергии.
Малат-аспартатный челнок более сложен:постоянно идущие в цитоплазме ре-
акции трансаминирования аспартата поставляют оксалоацетат, который под дейст-вием цитозольного пула малатдегидрогеназы восстанавливается до яблочной ки- слоты. Последняя антипортом с α-кетоглутаратом проникает в митохондрии и, явля-
ясь метаболитом ЦТК, окисляется в оксалоацетат с образованием НАДН. Так как
мембрана митохондрий непроницаема для оксалоацетата, то он аминируется до ас-
парагиновой кислоты, которая в обмен на глутамат выходит в цитозоль.
ГЛЮКОНЕОГЕНЕЗ
Глюконеогенез – это синтез глюкозы из неуглеводных компонентов: лактата, пирувата. глицерола, метаболитов цикла Кребса, аминокислот. Все аминокислоты, кроме кетогенных лейцина и лизина, способны участвовать в синтезе глюкозы. Неко-
торые из них – глюкогенные – полностью включаются в молекулу глюкозы, некото-рые – смешанные – частично.
В организме всегда существует потребность в глюкозе:
• для эритроцитов глюкоза является единственным источником энергии,
• нервная ткань потребляет 120 г глюкозы в сутки, притом эта величина не за-висит от интенсивности ее работы. Только в экстремальных ситуациях (дли- тельное голодание) она способна получать энергию из неуглеводных источ-
ников,
• глюкоза играет весомую роль для поддержания необходимых концентраций
метаболитов цикла трикарбоновых кислот (в первую очередь оксалоацета-
та).
Таким образом, при определенных ситуациях – при низком содержании углево-
дов в пище, голодании, длительной физической работе – организм должен иметь
возможность получить глюкозу. Это достигается процессом глюконеогенеза. Кроме получения глюкозы, глюконеогенез обеспечивает и уборку "шлаков" – лак- тата, образованного при мышечной работе и в эритроцитах, и глицерола, являюще-
гося продуктом липолиза в жировой ткани.
Глюконеогенез лишь отчасти повторяет реакции окисления глюкозы. Как указы-
валось ранее, в гликолизе существуют три необратимые стадии: пируваткиназная
(десятая), фосфофруктокиназная (третья) и гексокиназная (первая). На этих стадиях существуют энергетические барьеры, которые обходятся с помощью специальных реакций.
|
||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 117; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.219.95.244 (0.021 с.) |