
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Vp -диаграмма реального газа. Изотермы Ван-дер-Ваальса
линия 1 k – нижняя пограничная кривая (НПК), разделяет жидкую фазу вещества слева и двухфазное состояние (жидкость-пар) справа, в каждой точке НПК – начало кипения жидкости; линия 2k – верхняя пограничная кривая (ВПК), разделяет двухфазное состояние и паровую (газовую) фазу. С ростом p удельные объемы v Рис.8.2 (плотности r) жидкости и газа сближаются; точка k – критическая точка, в которой исчезает различие между жидкой и газовой фазами, параметры в этой точке (рк, Тк, vк) назы- ваются критическими. Уравнение Ван-дер-Ваальса – уравнение третьей степени относи- тельно v имеет при различных p и T либо один, либо три разных или равных по величине вещественных корня. В соответствии с этим качественно различимы изотермы Ван-дер-Ваальса. · При T > Tк уравнение имеет один вещественный корень и два мнимых, изотермы имеют вид гипербол. · При T = Tк критическая точка к является точкой перегиба изотермы Tк = const; все три корня вещественные, равные друг другу. · При T < Tк уравнение имеет три разных по величине вещественных корня, на изотермах появляются волнообразные участки с минимумом (точка е) и максимумом (точка d). На этих участках состояние вещества ограниченно устойчивое (метастабильное), характерное только для тщательно очищенных веществ. Реальные изотермы в этой области являются прямыми, параллельными оси v, совпадающими с изобарой, например прямая ас (изобара-изотерма). В уравнении Ван-дер-Ваальса коэффициенты а, b и индивидуальная газовая постоянная R определяются по критическим параметрам:
Коэффициент сжимаемости в критической точке
Таблица 8.1 Критические параметры веществ
Подстановка выражений a, b, R в уравнение Ван-дер-Ваальса да-ет уравнение в безразмерном виде:
где p; j; t – соответственно приведенные давление, удельный объем, температура; p = p/pк; j = v/vк; t = T/Tк. Водяной пар: понятие о водяном паре; процессы производства водяного пара; функции состояния жидкости и пара, их графическое описание в s-T и s-h координатах, термодинамические процессы с водяным паром.
точка а – жидкость при 0 ° C; ab – процесс нагревания жидкости при p=const до температуры кипения (сопровождается испарением – парообразованием с поверхности); точка b – начало кипения; bc – изобарно-изотермический процесс па-рообразования с потреблением теплоты при кипении (паро- Рис. 8.3 образование во всем объеме). В каждой точке динамическое равновесие – парообразование компенсируется конденсацией (конденсация – процесс превращения пара в жидкость с выделением теплоты). Состояние пара – влажный насыщенный пар (ВНП) при давлении насыщения p s и температуре насыщения Ts. ВНП – механическая смесь образовавшегося сухого насыщенного пара (СНП) с жидкой фазой. x – степень сухости – отношение массы СНП к массе ВНП; 0 (1-x) – степень влажности – отношение массы жидкой фазы к массе ВНП; r, Дж/кг - скрытая теплота парообразования – количество теплоты, необходимое для полного превращения 1 кг кипящей жидкости в СНП. точка c – СНП; cd – изобарный перегрев пара (степень перегрева– разность температур перегретого пара (ПП) и СНП при p=const), т.е. ( Обозначения параметров и функций жидкости и пара: жидкость при 0°C: жидкость в начале кипения: ВНП: СНП: ПП: При увеличении Линия To=const – жидкость при 0°C. Линия x=0 –нижняя пограничная кривая (НПК), соответствует состоянию жидкости в начале кипения. Линия x=1 – верхняя пограничная кривая (ВПК) – СНП. На пересечении линий To=const и x=0 (НПК) находится тройная точка (А) воды, обозначающая трехфазное состояние (твердое – лед, жидкое, парообразное).
Параметры точки А: p=610 Па; t=0°C; v=0,001м3/кг. На пересечении линий НПК и ВПК находится точка k – критическая точка, в которой исчезает различие между жидкой и газовой фазами. В точке k теплота парообразования r =0. Параметры в точке k: pк=22,06 МПа; Tk=374,1 °C; vк=0,00306 м3/кг.
|
|||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 113; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.116.159 (0.006 с.) |
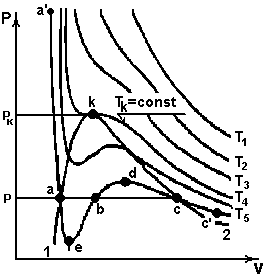 На vp-диаграмме (рис.8.2.):
На vp-диаграмме (рис.8.2.):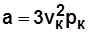 ;
;  ;
; 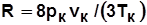 . (8.3)
. (8.3) .
. , (8.4)
, (8.4) На vp-диаграмме (рис.4.3):
На vp-диаграмме (рис.4.3): x
x 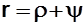 , где r - внутренняя теплота парообразования (изменение внутренней потенциальной энергии); y - внешняя теплота парообразования (работа расширения ВНП), y ~ пл. bobccobo (см. рис 8.3);
, где r - внутренняя теплота парообразования (изменение внутренней потенциальной энергии); y - внешняя теплота парообразования (работа расширения ВНП), y ~ пл. bobccobo (см. рис 8.3); ); cd ¢ - изотермический перегрев пара (степень перегрева (
); cd ¢ - изотермический перегрев пара (степень перегрева (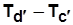 ).
). ,
, 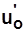 ,
, 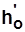 ,
, 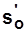 .
. ,
,  ,
, 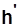 ,
, 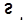 .
.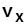 ,
,  ,
,  ,
,  .
. ,
,  ,
,  ,
, 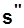 .
. ,
,  ,
,  ,
,  .
. возрастают
возрастают 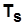 и незначительно
и незначительно  и уменьшаются
и уменьшаются 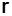 и
и 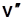 .
.


