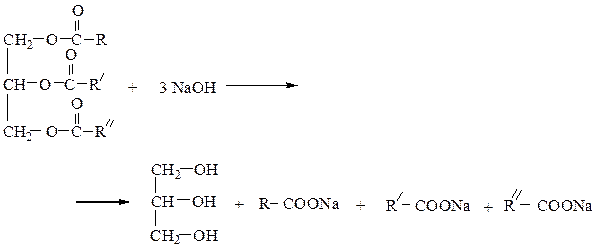Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 6.1.5 Реакции ангидридов карбоновых кислот
Реактивы, материалы, приборы: уксусный ангидрид, этанол, изоамиловый спирт, 1%-й раствор гидроксида натрия, пробирки, спиртовки.
а) Взаимодействие уксусного ангидрида с водой. В пробирку помещают 2 см3 воды и 1 см3 уксусного ангидрида. Смесь взбалтывают, наблюдают ее расслоение с выделением уксусного ангидрида в нижнем слое. При осторожном нагревании в процессе встряхивания происходит гидролиз уксусного ангидрида и смесь становится однородной. (CH 3 CO)2 O + H 2 O ¾ ® 2 CH 3 COOH б) Взаимодействие уксусного ангидрида с гидроксидом натрия. В пробирку наливают 0,5 см3 уксусного ангидрида и 1 см3 1%-го раствора гидроксида натрия. При встряхивании образуется однородный раствор. (CH 3 CO)2 O + 2 NaOH ¾ ® 2 CH 3 COONa в) Ацилирование этанола уксусным ангидридом. В пробирке смешивают 2 см3 этилового спирта и 1 см3 уксусного ангидрида. Реакционную смесь нагревают несколько минут в водяной бане с температурой 65-75 ºС. Затем добавляют 1-2 см3 воды и нейтрализуют реакционную смесь гидрокарбонатом натрия. Появляется запах и на поверхности образуется слой этилацетата. (CH3CO)2O + CH3CH2OH ¾ ® CH3COOCH2CH3 + CH3COOH Напишите схему межмолекулярной дегидратации масляной кислоты и реакции образовавшегося вещества с гидроксидом калия, пропанолом-2 и метиламином.
Наблюдение:
Выводы:
Опыт 6.1.6 Гидроксамовая проба на сложные эфиры
Реактивы, материалы, приборы: изоамилацетат, бутилацетат, насыщенный раствор солянокислого гидроксиламина в метаноле, спиртовой насыщенный раствор гидроксида калия, 1 н раствор соляной кислоты, 0,1 н раствор хлорида железа (III), пробирки, капельницы, спиртовки.
В пробирке нагревают 2 капли сложного эфира (см. опыт 4.5.3) с 2 каплями насыщенного раствора солянокислого гидроксиламинав метаноле и оставляют стоять 1 мин. Затем добавляют 1 каплю спиртового насыщенного раствора гидроксида калия и осторожно нагревают до начала кипения. После охлаждения смесь подкисляют 3 каплями соляной кислоты и добавляют 1 каплю раствора хлорида железа(III). В зависимости от природы сложного эфира возникает розовая, красная или фиолетовая окраска. Аналогичная реакция характерна и для галогенангидридов и ангидридов кислот.
Наблюдение:
Выводы:
Опыт 6.1.7 Получение амида бензойной кислоты
Реактивы, материалы, приборы: хлористый бензоил, 25%-й водный раствор аммиака, пробирки.
Бензамид получается в виде белого кристаллического осадка при взаимодействии хлорангидрида бензойной кислоты с аммиаком.
C 6 H 5 COCl + NH 3 ¾ ® C 6 H 5 CONH 2 Напишите уравнение реакции хлорангидрида пропионовой кислоты с аммиаком, метиламином и диметиламином. Назовите полученные продукты реакций.
Наблюдение:
Выводы:
Опыт 6.1.8 Свойства олеиновой кислоты
Реактивы, материалы, приборы: олеиновая кислота, медь (проволока), азотная кислота концентрированная, бромная вода, 5%-й раствор перманганата калия, 10%-й раствор карбоната натрия, пробирки, капельницы, мерные пробирки, корковые пробки.
а) Изомеризация олеиновой кислоты в элаидиновую кислоту. В пробирку наливают 1 см3 олеиновой кислоты, добавляют несколько кусочков медной проволоки и 1,5 см3 концентрированной азотной кислоты, закрывают корковой пробкой и встряхивают. Оставляют стоять на 30-40 мин при периодическом встряхивании. К концу опыта вся масса затвердевает.
[ NO + NO 2 ] цис- СН3 (СН2)7 СН=СН (СН2)7 СООН ¾¾¾¾¾ ® ¾¾ ® транс -СН3(СН2)7 СН=СН (СН2)7 СООН
б) Взаимодействие олеиновой кислоты с бромом. К 2 см3 бромной воды добавляют 3-4 капли олеиновой кислоты, смесь энергично встряхивают. Наблюдают обесцвечивание раствора. Br 2 СН3(СН2)7СН=СН(СН2)7СООН ¾ ® СН3(СН2)7–СН–СН–(СН2)7СООН │ │ Br Br
в) Окисление олеиновой кислоты водным раствором перманганата калия. В пробирку помещают 1 см3 5%-го раствора перманганата калия, 1 см3 10%-го раствора карбоната натрия и 0,5 см3 олеиновой кислоты. Смесь энергично перемешивают. Отмечают обесцвечивание реакционной смеси.
К MnO 4 СН3(СН2)7СН=СН(СН2)7СООН ¾ ® СН3(СН2)7–СН–СН–(СН2)7СООН │ │ OH OH Что образуется при окислении олеиновой кислоты концентрированным раствором перманганата калия при нагревании в присутствии H2SO4?
Наблюдение:
Выводы:
ЖИРЫ И МАСЛА Опыт 6.2.1 Омыление жира
Реактивы, материалы, приборы: животный жир, 40%-й раствор гидроксида натрия, насыщенный раствор хлорида натрия, фарфоровые чашки, стеклянные палочки, мерные пробирки, штативы.
Напишите уравнение реакции гидролиза тристеарата глицерина в кислой среде и с помощью раствора гидроксида натрия.
РАБОТУ ПРОВОДЯТ ЗА ЗАЩИТНЫМ ЭКРАНОМ ИЛИ В ОЧКАХ! В фарфоровую чашку помещают 2-3 г животного жира, добавляют 7 см3 40%-го раствора гидроксида натрия и смесь кипятят при слабом нагревании при помешивании стеклянной палочкой. По мере выкипания добавляют воду. Через 15 мин прибавляют 7 см3 насыщенного раствора хлорида натрия, массу охлаждают, выпавшее мыло отфильтровывают. Мыльную воду и мыло используют для дальнейших реакций.
Наблюдение:
Выводы:
|
||||||
|
Последнее изменение этой страницы: 2021-04-12; просмотров: 1001; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.2.184 (0.01 с.) |