Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гиповолемический (постгеморрагический) шок.
Кардиогенный шок. 3. Сосудистый шок (шок, связанный с пониженной резистентностью сосудов). Разновидностью гиповолемического шока являются травматический и ожоговыи шок. К сосудистым видам шока относятся септический и анафилактический шок.В свою очередь, каждый из этих видов шока имеет свою детальную клиническую классификацию. Необходимо отметить, что все виды шока объединяются одним общим признаком — тяжелыми нарушениями кровообращения и, как следствие этого, нарушениями гомеостаза. Причины, вызывающие шок различны, так же как и механизмы реализации их патологического воздействия на организм. Следовательно, и лечение больных должно быть патогенетически обоснованным и зависит от вида шока. В зависимости от этиологического фактора и патофизиологических сдвигов в организме шок разделяют на геморрагический, травматический, кардиогенный, септический, анафилактический, ожоговый и т.д. Все виды шока объединяет одно общее явление - снижение сердечного выброса в основе которого лежит снижение венозного возврата (в ряде случаев и при кардиогенном шоке), обусловленное снижением ОЦК. В связи с этим все виды шока можно представить как остро развивающееся состояние гиповолемии (исключение разновидности кардиогенного) степень выраженности которой, наряду с другими факторами, будет определять глубину шока и его прогноз.
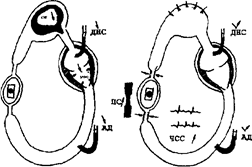
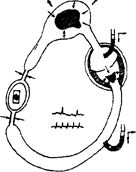
1. ГИПОВОЛЕМИЧЕСКИИ (ПОСТГЕМОРРАГИЧЕСКИЙ) ШОК. Пусковым механизмом в его развитии является синдром малого выброса, формирующийся в ответ на снижение венозного возврата (см рис 1). Данный вид шока развивается, как правило, не столько в связи с уменьшением ОЦК, сколько в результате интенсивности кровопотери. При кровопотере до 10% от ОЦК (это примерно до 500 мл крови) организм за счет моторики венозного русла (в нем в норме содержится до 70% объема крови, в артериях —15%,
Дефицит объёма Симпатоадренергическая Гиповолемический противорегуляция шок
Рис. 1. Патогенез гиповолемического шока (по X. П Шустер и соавт., 1981).
в капиллярах — 12% и в камерах сердца — 3%) довольно успешно справляется с данной ситуацией, давление наполнения (ДН) правых отделов сердца остается в пределах нормы, ЦВД держится на должном уровне, ударный объем (УО) не страдает. При потере более 10% от ОЦК, приток крови с периферии в малый круг начинает уменьшаться, ДН правых отделов сердца падает, ЦВД становится ниже нормы, вследствие этого снижается УО. Данный пато-логический сдвиг компенсируется тахикардией (уменьшение ОЦК на 10% и более резко стимулирует функцию надпочечников, а КА через воздействие на β-рецепторы сердца вызывают увеличение ЧСС) в результате чего МОС возрастает. При истощении компенсаторных механизмов (это проявляется уменьшением венозного возврата на 25—30%) УО уменьшается ниже критической величины и развивается СИНДРОМ МАЛОГО ВЫБРОСА. Он частично купируется компепсаторной тахикардией и вазоконстрикцией. (В основе вазоконстрикции, также как и в увеличении ЧСС, лежит массивный выброс катехоламинов непосредственно после кровопотери их уровень в крови возрастает в 50—100 раз). Поскольку периферический спазм неравномерен, кровоток перераспределяется за счет резкого сокращения перфузии всех органов и систем, организму некоторое время удается поддержать кровоснабжение сердца и головного мозга на приемлемом для жизни уровне. Данный феномен называется ЦЕНТРАЛИЗАЦИЕЙ КРОВООБРАЩЕНИЯ. Само по себе это явление можно расценивать как биологически целесообразную реакцию, необходимую организму для проведения компенсаторных изменении с целью нормализации состояния внутренней среды за счет перераспределения объемов водных секторов. Однако, если организм самостоятельно не в силах справиться с кровопотерей, то вазоконстрикция на фоне затянувшегося синдрома малого выброса приводит к глубокой гипоксии тканей с неизбежным развитием АЦИДОЗА (при гипоксии, вызванной значительной кровопотерей, потребности организма в кислороде покрываются приблизительно на 50%).
При шоковом состоянии происходят значительные нарушения водно- электролитного равновесия. Под влиянием ацидоза развивается постепенная потеря тонуса прекапиллярного сфинктера, на фоне сохранившегося тонуса посткапиллярной части капиллярона. Прекапиллярный сфинктер перестает реагировать даже на высокие концентрации эндогенных КА. Повышение гидростатического давления в сочетании с повышенной проницаемостью сосудистой стенки способствует переходу воды и электролитов в интерстиций. Повышается вязкость крови, возникает ее стаз, а в последующем и сладж, что в свою очередь вызывает возникновение коагулопатии.
При гиповолемических состояниях и эндотоксическом шоке (особенно вызванном грамотрицательнои флорой), а также при ишемии органов брюшной полости, геморрагическом и некротическом панкреатите из разрушенных лейкоцитов и поврежденных тканей выделяются протеолитические ферменты и попадают в плазму крови. Под их влиянием пептиды имеющие своим источником Q2-глобулиновую фракцию сыворотки крови (такие как ангиотензин, брадикинин) активируются и начинают оказывать угнетающее действие на миокард. Сумма этих активных пептидов называется фактор MDF (myocardial depressant factor). Во всех вышеуказанных случаях выделение и накопление MDF можно предупредить использованием ингибиторов протеолитической активности — трасилолом (контрикалом), больших доз глюкокортикоидов. В условиях нормальной оксигенации абсолютное большинство энергии (98%) вырабатывается в цикле Кребса (цикл трикарбоновых кислот). При гипоксии данный процесс нарушается и выработка энергии начинает сопровождаться накоплением большого количества лактата, недоокисленных аминокислот и жирных кислот, что, в свою очередь, вызывает развитие метаболического ацидоза. Гипоксия в сочетании с ацидозом вызывает выход ионов калия из клетки и вход в нее воды и ионов натрия, что еще более нарушает её биоэнергетику. Заключение. В основе гиповолемического шока лежит острая массивная кровопотеря. В результате уменьшения ОЦК падает УОС, снижается давление наполнения правых отделов сердца, уменьшается ЦВД и АД. В ответ на экстремальное воздействие организм отвечает массивным выбросом в кровоток КА, они, в свою очередь, через стимуляцию бета-рецепторов сердца вызывают увеличение ЧСС, а через воздействие на альфа-рецепторы, заложенные в стенках кровеносных сосудов, вызывают их констрикцию. В то же время, адреналин расширяет сосуды сердца и головного мозга, что в сочетании с увеличенной ЧСС обеспе-чивает приемлемый для жизни уровень кровоснабжения этих двух жизненно важных органов. Формируется ЦЕНТРАЛИЗАЦИЯ КРОВООБРАЩЕНИЯ. Если данное состояние держится более нескольких часов, в системе микроциркуляции развивается МЕТАБОЛИ-ЧЕСКИЙ АЦИДОЗ. Шоковое состояние сопровождается нарушением нормальной энергетики, дизэлектремией, появлением в плазме крови фактора MDF, возможно возникновение коагулопатии. 2. ТРАВМАТИЧЕСКИЙ ШОК. Ведущим в патогенезе травматического шока является мощная болевая импульсация, идущая с места травмы в ЦНС. В ответ на это организм отвечает гиперкатехоламинемией, клинически проявляющейся развитием I фазы шока — эректильной, однако, ввиду кратковременности данной фазы, клиницисты наблюдают её редко; в последующем у больного развивается II фаза — торпидная, в основе которой лежит энергетическое голодание в результате истощения запасов эндогенной энергии, уменьшение УО, замедление капиллярного кровотока, возрастание вязкости крови и последующая её секвестрация. Так как травматический шок редко бывает без большой внутренней или наружной кровопотери, то это, в свою очередь, усугубляет течение травматического шока и, в конечном итоге, дальнейшее его развитие идет по пути, характерному для гиповолемической модели (см. выше).
3. ОЖОГОВЫЙ ШОК. В основе его развития, также как и травматического шока, лежит сверхсильное воздействие болевой импульсации на ЦНС, что клинически проявляется последовательным появлением эректильной (более выражена, чем при травматическом шоке) и торпидной фаз. Особенностью данного патологического состояния, в сравнительном аспекте с другими разновидностями шока, является то, что в результате нарушения целостности кожных покровов, происходит интенсивная плазморея, способная в течение первых часов снизить ОЦК на 20-40%, в результате чего развивается выраженная гиповолемия в сочетании с вторичной эритремией и естественным для данного состояния нарушением микроциркуляции. Дефицит ОЦК может увеличиться и за счет кровопотери с ожоговой поверхности. В конечном итоге развитие ожогового шока идет по пути, характерному для гиповолемической модели (см. выше). 4. СЕПТИЧЕСКИЙ ШОК. В его основе лежит воздействие эндотоксинов на систему микроциркуляции, в частности, происходит раскрытие артериовенозных анастомозов. Так, если в нормальных условиях через A-V шунт проходит около 5% органного кровотока, то при септическом шоке эта величина неуклонно возрастает, что способствует формированию кислородного дефицита в системе капилляров. Усиленный сброс артериальной крови через A-V шунт вызывает формирование весьма нехарактерного признака для шоковых состоянии: кожные покровы становятся теплыми, иногда даже горячими на ощупь. Кроме этого, бактериальные токсины нарушают усвоение кислорода непосредственно в клетках. В ответ организм реагирует повышением МОС посредством повышения УО и ЧСС с одновременным снижением ПСС. Этот этап шока обозначается как ГИПЕРДИНАМИЧЕСКАЯ ФАЗА (Э.К. Айламазян, 1995). Кроме воздействия на гемодинамику, бактериальные токсины оказывают непосредственный токсический эффект на внутренние органы (сердце, легкие, мозг, печень и т. д.) и вносят в развитие заболевания аллергический компонент, проявляющийся присоединением к развитию заболевания ряда признаков, характерных для течения анафилактического шока. На пике развития септического шока основные показатели центральной гемодинамики будут следующие: АД, УО, ЦВД, ДН в пределах верхней границы нормы или незначительно увеличены, умеренная тахикардия, сниженное ПСС. По мере нарасгания интоксикации УО приходит к нормальным величинам, а затем начинает прогрессивно уменьшаться, что способствует переходу шока в ГИПОДИНАМИЧЕСКУЮ ФАЗУ (Э. К. Айламазян, 1995). Данный вариант патологии наиболее часто встречается в акушерско-гинекологической практике у молодых женщин и протекает крайне бурно — летальный исход может наступить буквально через несколько часов.
5. АНАФИЛАКТИЧЕСКИЙИ ШОК. В его основе лежит массивный выброс в кровоток гистамина, серотонина и прочих биологически активных веществ на фоне повторного попадания в организм аллергена. Данные вещества оказывают паралитическое влияние на прекапиллярный сфинктер в системе микроциркуляции, в результате периферическое сосудистое сопротивление резко уменьшается и имеющийся объем крови становится слишком малым по отношению к сосудистому руслу. Иначе этот процесс условно можно оценить как децентрализацию кровообращения, т. е фактически возникает внезапная гиповолемия без потери ОЦК. Под влиянием биологически активных веществ быстро повышается проницаемость клеточных мембран, в результате этого возникают интерстициальные отеки, прежде всего, в головном мозге и легких, а переход жидкой части крови в интерстиций способствует её сгущению и еще большему уменьшению ОЦК. Все это происходит на фоне практически мгновенно развивающегося полного или частичного ларинго- и бронхиолоспазма, что клинически проявляется возникновением признаков ОДН. Появляются спастические сокращения кишечника, мочевого пузыря и матки с соответствующей клинической картиной. Защитная симпатоадреналовая реакция, характерная для многих других видов шока, здесь не проявляется, т. к. сама реакция на симпатическое раздражение нарушена. КЛИНИКА ШОКОВЫХ СОСТОЯНИЙ Клинические признаки шокового состояния
Синдромный диагноз «шок» ставится у больного при наличии острого нарушения функции кровообращения, которое проявляется следующими симптомами: • холодная, влажная, бледно-цианотичная или мраморная кожа, • резко замедленный кровоток ногтевого ложа, • затемненное сознание, • диспноэ, олигурия, тахикардия, уменьшение артериального и пульсового давления. В тех случаях, когда у больного имеются бесспорные признаки кровопотери, но еще отсутствует гипотония, нужно решить вопрос, развился шок или нет. В данной ситуации удобно пользоваться патогенетической классификацией Г. А. Рябова (1979). Исходя из патогенеза, автор предлагает выделять три стадии в развитии гиповолемического (геморрагического) шока (см. табл. 1): 1. Компенсированный обратимый шок (синдром малого выброса). 2. Декомпенсированный обратимый шок. 3. Необратимый шок.
Острая кровопотеря в объеме до 500 мл у взрослого человека протекает практически бессимптомно и не требует проведения интенсивной терапии. Таблица 1. Патогенетическая классификация, основные клинические симптомы и компенсаторные механизмы гиповолемического шока (по Г. А. Рябову, 1979).
При шоке ПЕРВОЙ СТАДИИ организм хорошо компенсирует острую кровопотерю физиологическими изменениями деятельности ССС. Сознание полностью адекватное, иногда отмечается некоторое возбуждение. При осмотре обращают на себя внимание незначительная бледность кожных покровов и наличие запустевших, нитевидных вен на руках. Верхние и нижние конечности на ощупь прохладные. Пульс слабого наполнения, умеренная тахикардия. АД, несмотря на снижение сердечного выброса, остается в пределах нормы, а иногда даже отмечается его увеличение. ЦВД на уровне нижней границы нормы или еще ниже, умеренная олигурия. Незначительные признаки субкомпенсированного ацидоза. С патогенетической точки зрения, первую стадию шока можно расценивать как начало формирования централизации кровообращения. Для шока ВТОРОЙ СТАДИИ ведущим клиническим симптомом является снижение системного давления. В основе этого явления лежит истощение возможностей организма при помощи спазма периферических сосудов компенсировать малый сердечный выброс. В результате нарушения кровоснабжения сердца падает его сократительная способность. Это в еще большей степени нарушает органную перфузию и усиливает ацидоз. В системе микроциркуляции развивается стаз. Клинически вторая стадия проявляется спутанностью сознания, компенсаторными тахикардией (ЧСС 120-140) и одышкой, низким пульсовым АД, венозной гипотонией, низким или отрицательным ЦВД. Компенсаторная одышка появляется в ответ на метаболический ацидоз и как ответная реакция на формирующиеся шоковые легкие. Прогностически плохими предвестниками в данной стадии шока является появление у больного акроцианоза на фоне общей бледности в сочетании с гипотонией и олигоанурией. Шок ТРЕТЬЕЙ СТАДИИ начинает формироваться, если некомпенсированная гипотония держится у больного 12 и более часов. С точки зрения патогенеза, принципиальным отличием третьей фазы шока от второй является переход стаза в системе микроциркуляции в сладж-синдром. Это сопровождается, помимо начала первой фазы ДВС-синдрома, феноменом некроза и огторжения слизистой оболочки кишечника. В основе данного явления лежит переполнение сосудов кишечника кровью, выходом плазмы в интерстиций и последующим отторжением. Клинически состояние больного характеризуется как крайне тяжелое. Сознание отсутствует. Отмечаются резкая бледность кожных покровов, холодный пот, низкая температура тела, олигоанурия. Пульс на периферии определяется с большим трудом или вообще отсутствует. ЧСС более 140, АД менее 60 мм рт.ст. или совсем не определяется. Критерии контроля шока В качестве экспресс-диагностики шока можно использовать определение «шокового индекса Альговера» (ШИ) — это отношение частоты сердечных сокращений за 1 мин. к величине систолического давления. Нормальная величина ШИ = 60/120 = 0,5 Примечание. 60 — ЧСС в I мин. 120 — нормальная величина систолического АД в мм рт.ст.
В диагностике шока на первоначальном этапе используют общедоступные клинические тесты, на втором — лабораторные и специальные методы исследования. В конечном итоге контроль направлен на выяснение механизмов возникновения шока, определения его глубины и эффективности проводимых мер. Для адекватного лечения необходимо осуществлять постоянный контроль за состоя-нием сознания, температурой и цветом кожных покровов, ЦВД, АД, МОС, УО, ОЦК, ЧСС и их ритмом, кислотно-щелочным и водно-электролитным состоянием, вязкостью крови и гематокритом, почасовым диурезом и плотностью мочи, свертывающей системой крови, функцией легких, основными биохимическими параметрами, определением температурного градиента между кожными покровами и прямой кишкой и т.д.
|
||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 221; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.174.95 (0.021 с.) |
|||||||||||||||||||||||||||||||||||||||||||||