Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Переваривание и всасывание липидов.Стр 1 из 8Следующая ⇒
Переваривание и всасывание липидов. Лишь 40-50% пищевых липидов расщепляется полностью, от 3% до 10% пищевых липидов всасываются в неизмененном виде. Желчь синтезируется в печени, концентрируется в желчном пузыре и после приёма жирной пищи выделяется в просвет двенадцатиперстной кишки (500-1500 мл/сут). Жёлчь это вязкая жёлто-зелёная жидкость, имеет рН=7,3-8.0, содержит Н2О – 87-97%, органические вещества (желчные кислоты, жирные кислоты, желчные пигменты, холестерин, фосфолипиды) и минеральные компоненты (натрий, хлор, НСО3- ион слабой двухосновной угольной кислоты и калий). Нарушение соотношение компонентов желчи приводит к образованию камней.
Переваривание фосфолипидов. К фосфолипидам относятся глицерофосфолипиды – производные фосфатидной кислоты, и сфингофосфолипиды. Основными компонентами фосфолипидов являются кефалин, лецитин, фосфатидилсерин и сама фосфатидная кислота. Метаболизм фосфолипидов тесно связан со многими процессами в организме: образование и разрушение мембранных структур клеток, формирование липротеинов, мицелл желчи, образование в легочных альвеолах поверхностных пленок (сульфоктанта) препятствующих слипание альвеол. Фосфолипиды – за счет наличия в структуре остатка фосфорной кислоты обладают амфифильностью, за счет чего образуют бислойную структуру мембран, в которую погружены белки. Амфифильность – это сочетание гидрофобных и гидрофильных свойств молекулы за счет наличия различных участков. Так в молекуле фосфолипида остатки жирных кислот проявляют гидрофобные свойства, а остаток фосфорной кислоты с аминоспиртом – гидрофильные. В молекуле сфинголипидов и сфингофосфолипидов в место молекулы глицерина используется другой многоатомный спирт – сфингозин (N-ацилсфингозин). В организме сфинголипиды выполняют пластическую функцию в структуре клеточных мембран. Больше содержится сфинголипидов и сфингофосфолипидов в нервной ткани.
Нарушение обмена фосфолипидов – причина развития многих заболеваний (липидоз печени, респираторный дистресс-синдром). Обмен холестерина. Источники холестерина: Синтез холестерина в печени Процесс биосинтеза ХС сложный и многоступенчатый, происходит в цитоплазме клеток печени из ацетил-КоА Ацетилкофермента А. В нём участвуют более 100 ферментов, включает 35 уравнений химических реакций. Синтезированные в кишечнике ХМ и в печени ЛПОНП попадают в кровеносное русло и переносят ТГ (триглицериды) в жировые клетки и другие ткани. После отделения ТГ в жировых клетках, ХМ вновь поступают в печень, а ЛПОНП превращаются в ЛПНП, обогащенные ХС. ЛПНП сохраняются в кровеносном русле в течение 2,5 суток и служат транспортерами ХС в различные клетки периферических тканей. Поступление ХС в клетки осуществляется при помощи рецепторов ЛПНП, количество и функции которых находятся под генетическим контролем. Клеточные рецепторы группируются в специальных участках клеточной мембраны, погруженных виде кратера в цитоплазму. После взаимодействия рецептора с ЛПНП участок мембраны, содержащий рецепторы, втягивается внутрь клетки и образует окаймленную везикулу. В цитоплазме ЛПНП отделяются от рецептора и проникают в лизосомы, а рецепторы возвращаются на клеточную мембрану. Освобождение ХС из ЛПНП осуществляется под действием нескольких ферментов. Обратная доставка ХС в клетки печени и тонкого кишечника осуществляется ЛПВП также с использованием механизма рецепторного эндоцитоза. Использование холестерина в тканях Холестерин необходим для всех клеток и тканей. 1. В печени примерно половина синтезирующегося холестерина превращается в жёлчные кислоты при участии ключевого фермента 7-α-гидроксилазы. 2. Холестерин используется для построения клеточных мембран, где он составляет примерно треть всех липидов мембран и определяет физико-химические свойства липидной фазы мембран. 3. В надпочечниках, половых железах холестерин используется на синтез стероидных гормонов 4. В коже из производного холестерина происходит образование витамина Д3(холекальциферола). Выведение холестерина из организма Избыток холестерина удаляется из тканей при участии ЛПВП, которые адсорбируют холестерин из клеток и переносят его в печень. Основная часть холестерина выводится из организма через кишечник в виде жёлчных кислот, продуктов их обмена и образующихся из холестерина под действием микрофлоры холестанола и копростанола. Выведение холестерина из организма в небольших количествах происходит со слущивающимся эпителием, с мочой в виде соединений стероидных гормонов с глюкуроновой кислотой.
Ацетоновые тела.
При состояниях, сопровождающихся снижением глюкозы крови, клетки органов и тканей испытывают энергетический голод. Например, в постадсорбционном периоде (когда между приемами пищи длительный интервал) идет мобилизация энергетических ресурсов организма в том числе мобилизация триглицеридов жировой ткани. Так как окисление жирных кислот процесс "трудоемкий", а нервная ткань вообще неспособна окислять жирные кислоты, то печень облегчает использование этих кислот тканями, заранее окисляя их до уксусной кислоты и переводя последнюю в транспортную форму – кетоновые тела. Ацетоновые тела (кетоновые тела) — группа органических соединений, включающая β-оксимасляную кислоту, ацетоуксусную кислоту и ацетон, между которыми существует тесная взаимосвязь: при окислении β-оксимасляной кислоты ее вторичная спиртовая группа переходит в кетоновую и образуется ацетоуксусная кислота; эта реакция обратима. В процессе карбоксилирования ацетоуксусная кислота распадается на ацетон и CO2. Оксимасляная и ацетоуксусная кислоты как промежуточные продукты жирового обмена образуются преимущественно в печени в результате β-окисления высших жирных кислот с четным количеством углеродных атомов. Значительные количества ацетоуксусной кислоты образуются не только при окислении β-оксимасляной кислоты, но и путем конденсации двух молекул уксусной кислоты, отщепляющейся в процессе β-окисления высших жирных кислот или образующейся из пировиноградной кислоты. Ацетоуксусная кислота образуется также в процессе промежуточного обмена аминокислот фенилаланина, тирозина, лейцина, оксипролина и отчасти изолейцина. Ацетоновые тела окисляются до CO2 и H2O не в печени, а в других органах и тканях (легкие, почки, мышцы и др.). Окисление ацетоуксусной кислоты до CO2 и H2O осуществляется в цикле трикарбоновых кислот. Повышение образования ацетоновых тел в печени обычно наблюдается при понижении содержания в ней гликогена и связано с избыточным поступлением в печень из жировых депо жира и последующим его окислением. Недостаточное окисление ацетоновых тел зависит от нарушения цикла трикарбоновых кислот. Содержание ацетоновых тел в крови в норме не превышает 2—4 мг% (миллиграмм процент) (выраженных в виде ацетона) или 8 мг% (выраженных в виде β-оксимасляной кислоты).
Ацетоуксусная и β-оксимасляная кислоты являются нормальными промежуточными продуктами окислительного обмена жирных кислот. В патологических условиях (например, при сахарном диабете, голодании, при недостатке углеводов в пище) кетоновые тела накапливаются в организме и содержатся в повышенных количествах в тканях, органах, крови, моче, обусловливая ацетонемию и ацетонурию. При избыточном содержании ацетона в крови он выделяется не только почками, но и легкими. Накопление в организме ацетоновых тел в результате повышенного их образования, недостаточного окисления и ресинтеза в жирные кислоты приводит к развитию ацидоза и к отравлению, проявляющемуся резким угнетением деятельности ЦНС и развитием коматозного состояния.
Патология липидного обмена Нарушения липидного обмена могут возникнуть в результате нарушений: 1) всасывания жира в кишечнике; 2) перехода жира из крови в ткань; 3) депонирования жира: 4) промежуточного жирового обмена. Нарушение всасывания жира Для всасывания пищевого жира из кишечника необходимо его эмульгирование, расщепление на глицерин и жирные кислоты и образование комплексных соединений с желчными кислотами. Поэтому прекращение выделения желчи в двенадцатиперстную кишку или уменьшение ее секреции немедленно отражаются на переваривании жиров. Закупорка желчного протока, воспаление желчного пузыря (холецистит) и некоторые заболевания печени, связанные с нарушением процесса секреции желчи, приводят к тому, что неэмульгированные жиры проходят через пищеварительный канал, подвергаясь лишь в незначительной степени гидролизу. То же происходит при уменьшении или полном прекращении секреции ферментов поджелудочной железы, при понижении функции кишечного эпителия и при значительно усиленной перистальтике тонкого кишечника, когда жир не успевает всосаться. Такого рода расстройства всасывания жира наблюдаются при энтеритах, гиповитаминозах А и В, вследствие нарушения образования ферментов, участвующих в ресинтезе триглицеридов в кишечном эпителии. Выделение жира происходит в основном через кишечник и в меньшей степени осуществляется сальными и потовыми железами. В моче обнаруживаются лишь следы жира. При нарушениях всасывания жира кал содержит много нерасщепленного жира и высших жирных кислот и имеет характерный серовато-белый цвет - стеаторея. Выделение жира с мочой - липурия - может возникнуть после приема с пищей очень больших количеств жира, при переломах трубчатых костей, сопровождающихся размозжением костного мозга, травме обширных участков жировой ткани, при липоидном нефрозе. Избыточное выделение жира сальными железами - себорея - имеет место при некоторых заболеваниях кожи - угри, экзема, авитаминозы и др.
Жиры и липоиды легко синтезируются в организме из промежуточных продуктов углеводного обмена, но полное исключение из пищи жиров недопустимо. С жирами в организм вводятся жизненно необходимые жирорастворимые витамины (A, D, Е, К) и поэтому при недостаточном введении жиров с пищей у человека могут развиваться гиповитаминозы. Кроме того, в состав природных жиров всегда входят в небольшом количестве незаменимые ненасыщенные высшие жирные кислоты (например, линолевая-С18Н32О2 и линоленовая - С18Н30О2), которые не могут синтезироваться в организме из других жирных кислот. Полное отсутствие ненасыщенных высших жирных кислот в пище человека также может быть причиной более или менее серьезных расстройств обмена. Регуляция обмена липидов. Обмен липидов так же, как и других веществ, регулируется центральной нервной системой. Центр регуляции липидного обмена находится в промежуточном мозге. Регуляция осуществляется, с одной стороны, через симпатическую и парасимпатическую систему, с другой - через железы внутренней секреции. Большое значение в обмене жиров имеют процесс отложения запасного жира в жировой ткани и его мобилизация. Симпатическая нервная система способствует мобилизации жира. При ее возбуждении, обусловленном мышечным напряжением, отрицательными эмоциями, возможна убыль жира в жировой ткани. Наоборот, слабая возбудимость симпатической нервной системы способствует понижению расщепления жира и приводит к ожирению. К железам внутренней секреции, через которые нервная система влияет на жировой обмен, относят гипофиз, щитовидную, поджелудочную, половые железы и др. Переход углеводов в жиры осуществляется непосредственно в жировой ткани. Этот сложный процесс регулируется гормоном поджелудочной железы инсулином. Превращению углеводов в жиры способствует гормон передней доли гипофиза пролактин. Тиамин также активизирует процесс образования жира из углеводов. Мобилизация жира и его энергетическое использование стимулируются гормоном щитовидной железы тироксином - он активизирует окислительные процессы, в результате чего усиленно расщепляется сахар, печень теряет гликоген и получает из жировых депо жир. Соматотропный гормон гипофиза ускоряет как выход жирных кислот из жировой ткани, так и их сгорание. Выделяемая при этом энергия обеспечивает синтез белка, что ведет к усиленному росту организма. Следовательно, гормон роста способствует экономному расходу белков и интенсивному использованию вместо них жиров. Гипофункция гипофиза приводит к значительному отложению жиров (гипофизарное ожирение), а гиперфункция - к истощению (гипофизарная кахексия). На белковый, углеводный и жировой обмен наряду с центральной нервной системой влияют почти все железы внутренней секреции. Резко разграничивать регуляторную деятельность каждой железы на тот или иной обмен веществ очень трудно, поэтому их рассматривают всегда в комплексе Обмен веществ имеет ряд общих реакций, связывающих между собой обмен белков, углеводов и жиров в единый биологический процесс. Так, например, углеводный обмен нельзя рассматривать изолированно от обмена белков и жиров. В ходе обменных процессов в организме существует взаимосвязь и переплетение различных видов обмена. Белки и даже жиры могут быть источниками образования гликогена, а за счет углеводов может осуществляться образование жиров, что происходит при откорме животных. Кроме того, за счет углеводов путем трансаминирования могут быть также синтезированы многие заменимые аминокислоты. Причем возможен и обратный процесс, то есть большинство аминокислот может служить источником для образования пировиноградной кислоты - главного посредника в обмене белков и углеводов. Взаимосвязь промежуточного обмена углеводов и жиров ярко выражена при сахарном диабете. При этом уменьшение использования углеводов и нарушение их промежуточного обмена способствуют нарушению обмена жиров, что приводит к накоплению ацетоновых тел. И наконец, роль белков в обмене липидов определяется тем, что они выполняют каталитические функции в реакциях их расщепления и синтеза.
Энергетический обмен. Энергетическии обмен (катаболизм, диссимиляция) — это процессы расщепления веществ с высвобождением энергии. Высвобожденная энергия преобразуется в энергию АТФ. Наиболее важными процессами энергетического обмена являются дыхание и брожение. БРОЖЕНИЕ
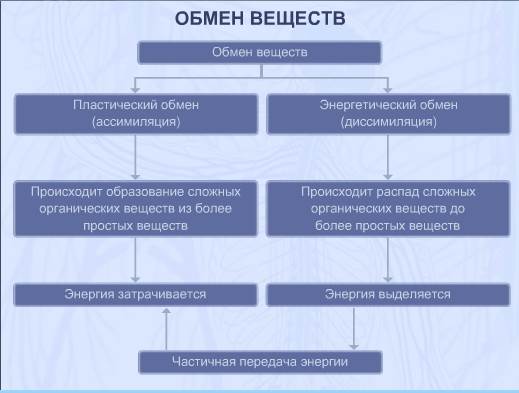
Метаболизм Обмен веществ, или метаболизм (в принципе, эти два понятия не вполне идентичны, но в учебной литературе, они рассматриваются в качестве синонимов), - это совокупность протекающих в организме химических превращений, обеспечивающих их рост, развитие, адаптацию к изменениям окружающей среды и воспроизведение. В ходе метаболизма происходит также постоянный контакт с окружающей средой и обмен с ней веществом. В процессе обмена веществ внутри организма происходит расщепление и синтез молекул, входящих в состав клеток, образование, разрушение и обновление клеточных структур и межклеточного вещества.
Метаболизм выполняет три специализированные функции: Энергетическая – снабжение клетки химической энергией, Пластическая – синтез макромолекул как строительных блоков, Специфическая – синтез и распад биомолекул, необходимых для выполнения специфических клеточных функций. Метаболизм включает два неразрывных процесса анаболизм и катаболизм.
Анаболизм Анаболизм – это биосинтез белков, полисахаридов, липидов, нуклеиновых кислот и других макромолекул из малых молекул-предшественников. Поскольку он сопровождается усложнением структуры, то требует затрат энергии. Источником такой энергии является энергия АТФ.
Катаболизм Катаболизм – расщепление и окисление сложных органических молекул до более простых конечных продуктов. Оно сопровождается высвобождением энергии, заключенной в сложной структуре веществ. Большая часть высвобожденной энергии рассеивается в виде тепла. Меньшая часть этой энергии сразу используется для синтеза АТФ. Весь катаболизм условно подразделяется на 4 этапа: I этап Гидролитический в котором из полимеров образуются мономеры. Происходит в кишечнике (переваривание пищи) или в лизосомах при расщеплении уже ненужных молекул. При этом освобождается около 1% энергии, заключенной в молекуле. Она рассеивается в виде тепла. II этап Промежуточный. Превращение мономеров в пировиноградную кислоту и ацетил-КоА). Локализация второго этапа – цитозоль и митохондрии. I I I этап Цикл Кребса. Локализация - митохондрии IV этап Тканевое дыхание и окислительное фосфорилирование. Локализация - митохондрии
·
Ассимиляция (биология) — совокупность процессов синтеза в живом организме Диссимиляция разрушение сложных органических веществ до более простых
Цикл трикарбоновых кислот. За открытие этого цикла Ганс Кребс получил Нобелевскую премию. Цикл Кребса это — ключевой этап дыхания всех клеток, является процессом окисления ацетилкоэнзима А –универсального продукта катаболизма углеводов, липидов и белков. ЦТК протекает в митохондриях с участием 8 ферментов, которые локализованы в матриксе в свободном состоянии или на внутренней поверхности внутренней мембраны. Основной функцией ЦТК является образование восстановленных кофермен-тов НАДН, которые поставляют протоны в дыхательную цепь. Кроме того, субстраты ЦТК могут использоваться для глюконеогенеза, переаминирования, синтеза гема, жирных кислот. Таким образом, ЦТК интегрирует все виды обмена веществ. Т.О.Цикл Кребса — перекрёстная точка метаболических путей. Им заканчивается катаболизм (распад), им начинается анаболизм (синтез);
По сути Цикл Кребса описывает этапы превращения лимонной кислоты. Этапы ЦТК ацетил-коэнзима А вступает в реакцию со щавелевоуксусной кислотой, что приводит к образованию лимонной кислоты. Лимонная кислота превращается в изолимонную. Изолимонная кислота дегидрируется с образованием альфа-кетоглутаровой и углекислого газа. Альфа-кетоглутаровая кислота дегидрируется с образованием сукцинил-коэнзима А и углекислого газа. Сукцинил-коэнзим А превращается в янтарную кислоту. Янтарная кислота дегидрируется с образованием фумаровой. Фумаровая кислота гидратируется с образованием яблочной. Яблочная кислота дегидрируется с образованием щавелевоуксусной. При этом цикл замыкается. В первую реакцию следующего цикла вступает новая молекула ацетил-коэнзима А.
Макроэргические соединения. Макроэргические соединения (греч. makros большой + ergon работа, действие;) — группа природных веществ, молекулы которых содержат богатые энергией, или макроэргические, связи; присутствуют во всех живых клетках и участвуют в накоплении и превращении энергии. Разрыв макроэргических связей в молекулах М.с. сопровождается выделением энергии, используемой для биосинтеза и транспорта веществ, мышечного сокращения, пищеварения и других процессов жизнедеятельности организма. Переваривание и всасывание липидов. Лишь 40-50% пищевых липидов расщепляется полностью, от 3% до 10% пищевых липидов всасываются в неизмененном виде. Желчь синтезируется в печени, концентрируется в желчном пузыре и после приёма жирной пищи выделяется в просвет двенадцатиперстной кишки (500-1500 мл/сут). Жёлчь это вязкая жёлто-зелёная жидкость, имеет рН=7,3-8.0, содержит Н2О – 87-97%, органические вещества (желчные кислоты, жирные кислоты, желчные пигменты, холестерин, фосфолипиды) и минеральные компоненты (натрий, хлор, НСО3- ион слабой двухосновной угольной кислоты и калий). Нарушение соотношение компонентов желчи приводит к образованию камней.
|
|||||||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 74; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.189.177 (0.08 с.) |