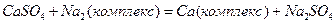Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основные компоненты физико-химического состава природных вод
Химические компоненты природных вод делят на 6 групп: - главные ионы; - растворенные газы; - растворенные органические вещества; - микроэлементы; - биогенные вещества; - токсичные элементы. Иногда выделяют еще одну группу – взвешенные вещества. Главные ионы. В значительных количествах в природных водах присутствуют ионы: Na+, K+, Ca2+, Mg2+, HCO3– (CO32– ), SO42–, Cl–, которые и называют главными ионами. Содержание их в пресных водоемах изменяется в широких пределах. Экспериментально установлено, что в открытом океане независимо от абсолютной концентрации соотношения между главными ионами основного солевого состава остаются примерно постоянными. Предложено подразделять все природные воды по преобладающему аниону на три класса: - гидрокарбонатные (карбонатные); - сульфатные; - хлоридные. Каждый класс по преобладающему катиону подразделяется на три группы: - кальциевую; - магниевую; - натриевую. Гидрокарбонатный и карбонатный ионы являются важнейшей составной частью ионного состава пресных и маломинерализованных природных вод суши. Появляются эти ионы в воде в результате растворения солей угольной кислоты – карбонатов кальция и магния. Соли СаСО3 и MgCO3 трудно растворимы в воде и могут перейти в раствор только в присутствии углекислого газа СаСО3 + СО2 + Н2О = Са(НСО3)2 Ионы НСО3–, СО32–, Са2+, Н+ и Н2СО3 находятся между собой в растворе в определенных количественных отношениях, определяющихся константой диссоциации угольной кислоты по первой и второй ступени (К1 = 3 . 10– 7 , К2 = 4 . 10– 11). Эти ионы и угольная кислота образуют карбонатную систему химического равновесия, т.е. изменение содержания одного из них влечет за собой изменение содержания другого, что имеет большое значение для поддержания реакции среды в природных водах. Хлорид – ионы обычно занимают первое место среди анионов в воде океанов, морей, сильно минерализованных озер, меньше их в воде рек. Источники хлорид-ионов в воде – продукты выветривания магматических пород, в которых хлор присутствует в рассеянном состоянии, колоссальные залежи хлористых солей осадочных пород, вулканические выбросы. Широкому распространению хлоридов в природных водах суши в значительной мере способствует деятельность человека, т.к. большое промышленное и физиолобиологическое значение NaCl способствует рассеянию его по земной поверхности. Ионы Cl– не усваиваются растениями и бактериями и выделяются в свободном состоянии организмами животных, поэтому круговорот их в земной коре несложен. Повышенное содержание хлоридов ухудшает вкусовые качества воды, делает ее малопригодной для питьевого водоснабжения и ограничивает применение для других целей. Концентрация хлоридов и ее колебания могут служить одним из критериев загрязненности водоема хозяйственно-бытовыми стоками.
Сульфат – ионы также важнейшие анионы природной воды и вместе с хлорид-ионами составляют главную часть анионного состава воды морей и сильно минерализованных озер. Содержание сульфат-ионов в природных водах лимитируется присутствием в воде катионов Са2+, которые образуют с сульфат-ионами малорастворимое соединение CaSO4. Основными источниками растворенных в воде сульфатов являются различные осадочные породы, в состав которых входит гипс СаSO4. 2H2O. Источниками сульфат-ионов в природной воде служат и процессы окисления самородной серы, протекающие по уравнению 2S + 3 O2 + 2 H2O = 2 H2SO4, а также окисление широко распространенных в земной коре сульфидных соединений. На содержание сульфат-ионов в природных водах оказывают влияние процессы распада и окисления органических веществ растительного и животного происхождения, содержащих серу. Вблизи населенных пунктов присутствие сульфат-ионов в воде часто оказывается результатом загрязнения ее бытовыми и промышленными сточными водами. Сульфат-ионы являются устойчивыми. При отсутствии кислорода сульфаты могут быть восстановлены обычно под действием сульфатредуцирующих бактерий, обнаруженных в морях и в водах нефтеносных месторождений, до сероводорода. Получающийся в процессе восстановления сульфатов сероводород в дальнейшем при соприкосновении с воздухом вновь окисляется вначале до серы 2 H2S + O2 = 2 H2O + 2 S, а затем до сульфатов. Повышенное содержание сульфатов в воде ухудшает ее органолептические свойства. Сульфаты могут придавать воде слабительные свойства, поэтому их содержание строго регламентируется.
При значительном содержании в воде хлоридов и сульфатов они являются причиной ее агрессивности по отношению к бетону. Так, сульфат-ионы могут взаимодействовать с известью цемента с образованием гипса, что вызывает увеличение объема и образование трещин в бетоне. Присутствие в воде значительного количества хлоридов приводит к выщелачиванию и разрушению бетонного камня вследствие образования растворимых хлоридов кальция и магния. Ионы щелочных металлов. Из ионов щелочных металлов в природных водах в наибольших количествах находятся ионы Na+, в значительно меньших – ионы К+. Подобно хлорид–ионам, ионы Na+ являются характерными ионами сильноминерализованных вод. Важнейшим источником катионов натрия в природных водах являются его залежи в виде хлористых солей, находящиеся среди различных осадочных пород морского, а в засушливых районах и континентального происхождения.
Другим источником ионов щелочных металлов в природной воде являются продукты выветривания горных пород. Калий содержится, главным образом, в кислых изверженных породах (ортоклаз, мусковит), а натрий входит в состав различных алюмосиликатов. Кроме того, в ряде случаев происходит обменная адсорбция ионов Са2+ и Na+ в породах, в результате чего в растворе взамен ионов Са2+ появляется эквивалентное количество ионов Na+ по схеме: Ионы магния и кальция. Если в сильноминерализованных водах доминирует катион натрия, то в маломинерализованных водах обычно доминирует катион кальция, гораздо реже – магния.
Основным источником катионов Са2+ в природных водах являются известняки, которые растворяются угольной кислотой, находящейся в воде, с образованием гидрокарбонатов Другим источником катионов Са2+ в природных водах является гипс, весьма распространенный в осадочных породах. Катионы магния поступают в воду преимущественно при растворении доломитов (MgCO3.CaCO3), мергелей или продуктов выветривания коренных пород. Присутствие катионов кальция и магния обусловливает жесткость воды. Растворенные газы. Из растворенных в воде газов наибольшее значение имеют кислород и оксид углерода (IV) (углекислый газ), а также азот, сероводород, метан и др. Растворимость газа в воде зависит от его природы, парциального давления и температуры. Для данной температуры растворимость может быть определена по закону Генри: С = К×Р, где С – растворимость газа, мг/дм3; К – коэффициент пропорциональности, равный растворимости газа при данной температуре и давлении 1 атм; Р – парциальное давление газа, атм. Концентрация любого газа в воде стремится перейти в равновесие с парциальным давлением этого газа над водой, поэтому непрерывно происходят обратимые процессы сорбции и десорбции. Кислород находится в природной воде в виде растворенных молекул. Его присутствие является обязательным условием для существования большинства организмов, населяющих водоемы. Вода обогащается кислородом за счет растворения кислорода атмосферы и за счет его выделения водной растительностью в процессе фотосинтеза. Дождевые и снеговые воды обычно пересыщены кислородом, поэтому их поступление в водоем увеличивает его аэрацию. Уменьшение содержания растворенного кислорода в воде происходит вследствие его выделения в атмосферу и из-за потребления на окисление органических веществ при дыхании организмов, брожении, минерализации органических остатков. Наличие растворенного кислорода является одной из причин коррозионной агрессивности воды по отношению к металлам. Концентрация кислорода определяет величину окислительно-восстановительного потенциала и в значительной мере направление и скорость процессов химического и биохимического окисления. Кислородный режим оказывает сильное влияние на жизнь водоема.
Содержание кислорода в воде обычно выражают в мг/дм3, в природных водах его содержание колеблется в пределах от 0 до 14 мг/дм3. Углекислый газ. Углекислый газ находится в воде главным образом в виде растворенных молекул СО2. Однако часть их, около 1%, вступает во взаимодействие с водой, образуя угольную кислоту СО2 + Н2О = Н2СО3 Обычно же не разделяют СО2 и Н2СО3 и под углекислым газом подразумевают их сумму. Источником углекислого газа в природных водах являются, прежде всего, процессы окисления органического вещества, происходящие как непосредственно в воде, так и в почвах и илах, с которыми соприкасается вода. Сюда относятся дыхание водных организмов и различные виды брожения распадающихся органических остатков. Обогащают воду углекислым газом и геохимические процессы в осадочных породах. Поглощение СО2 из атмосферы наблюдается почти исключительно в морях и очень редко в водах суши. Из процессов, направленных на уменьшение СО2 в природных водах, важнейшими являются удаление в атмосферу из-за перенасыщенности воды этим газом; расходование его на переход карбонатных пород в раствор; потребление водной растительностью при фотосинтезе. Содержание углекислого газа в природных водах колеблется в очень широких пределах: от нескольких десятков долей до нескольких сотен мг/дм3. Наименьшее его количество наблюдается в морях, наибольшее – в подземных водах. Обычно весной и летом содержание диоксида углерода в водоеме понижается, а в осенне-зимний период увеличивается, достигая максимума в конце зимы. Повышенные концентрации СО2 угнетающе действуют на животные организмы. В реках и озерах из-за постоянного выделения в атмосферу, а также значительного потребления при фотосинтезе содержание СО2 редко превышает 20-30 мг/дм3. При высоких концентрациях углекислого газа воды становятся агрессивными по отношению к металлам и бетону, т.к. при этом образуются растворимые гидрокарбонаты, нарушающие структуру этих материалов.
Прочие газы. Появление в природных водах сероводорода и метана указывает на наличие гнилостных процессов, протекающих в водоемах при ограниченном доступе воздуха. В природных условиях как сероводород, так и метан чаще встречаются в подземных водах. Однако наличие этих газов, в особенности Н2S, в реках и озерах может быть следствием сброса неочищенных сточных вод. Растворенные органические вещества. Эта группа веществ включает различные органические соединения: органические кислоты, спирты, альдегиды и кетоны, сложные эфиры, белки, углеводы, амины, свободные аминокислоты и т.д. По происхождению растворенные органические вещества можно разделить на автохтонные – продукты метаболизма и биохимического распада остатков организмов – и аллохтонные, которые поступают в водную среду с поверхностными стоками с площади водосбора с ливневыми и талыми водами, с атмосферными осадками и сточными водами. При разложении отмерших растений и их гумификации образуется сложная смесь высокомолекулярных органических соединений – гумусовые вещества, прежде всего гуминовые кислоты и фульвокислоты. Поверхностный сток с заболоченной площади водосбора приносит в природную воду большое количество этих веществ. Окраска природных вод связана, как правило, с наличием в водоеме гумусовых веществ. Содержание гумусовых веществ в речных водах около 5 – 10 мг/дм3, в озерных до 150 мг/дм3. Загрязнение природных вод происходит и ядохимикатами, применяемыми в сельском хозяйстве. К числу постоянных источников органического вещества следует отнести также бытовые и промышленные сточные воды, попадающие в подземные воды и реки. Состав этих веществ весьма различен. К ним относятся поверхностно-активные вещества (ПАВ), фенолы, нефтепродукты и др. Ввиду сложности определения индивидуальных органических веществ, их многообразия и малых природных концентраций для их количественной характеристики используют косвенные показатели: общее содержание Сорг; Nорг; Рорг, перманганатную или дихроматную окисляемость воды (ХПК), биохимическое потребление кислорода (БПК). Микроэлементы. В природных водах установлено наличие более 70 химических элементов. Веществ, совершенно не растворимых в воде, нет и каждый элемент, встречающийся в земной коре, содержится и в природных водах. К микроэлементам, по А.П. Виноградову, относятся те элементы, содержание которых в воде меньше 10–3 %. В группу микроэлементов входят все металлы, кроме главных ионов и железа, а также некоторые анионы. Тяжелые металлы (медь, кобальт, никель, марганец, цинк и др.) находятся в природных водах в небольших количествах, что объясняется небольшим содержанием их в почвах и грунтах.
Среднее содержание ионов брома в пресных водах колеблется в пределах 0,001 – 0,2 мг/дм3. Содержание ионов иода значительно меньше – до 0,003 мг/дм3, в морских водах оно повышается до 0,05 мг/дм3. Содержание фтора в воде озер, рек и артезианских скважин колеблется в пределах 0,04 – 0,3 мг/дм3. Содержание бора в пресных водах примерно 0,01 мг/дм3, в морских водах – 1,5 – 4,4 мг/дм3. Биогенные вещества. К биогенным принадлежат вещества, в той или иной мере связанные своим происхождением с жизнедеятельностью водных организмов. Присутствие этих веществ в воде, в свою очередь, определяет возможность существования водных организмов. Выделение этой группы является несколько условным, т.к. в жизненных процессах принимают участие и другие ионы, в частности ионы Са2+, Mg2+, К+. Биогенные вещества находятся в воде в виде ионов, а также в виде коллоидов. Соединения азота. Из неорганических соединений азота в природной воде встречаются катионы аммония (NH4+), нитритные (NO2–) и нитратные (NO3–) анионы. Сходство их генезиса и возможность взаимного перехода одного в другой дают основание объединить их в одну группу.
Основным источником появления в природной воде NH4+, а затем NO3– и NO2– являются различные сложные органические вещества животного и растительного происхождения, содержащие в своем составе белок. Некоторые микроорганизмы способны под действием протеолитических ферментов расщеплять молекулы белка на пептидные цепочки и отдельные аминокислоты:
Образовавшиеся аминокислоты далее разлагаются при участии бактерий и ферментов с выделением аммиака. Разложение (дезаминирование) аминокислот может осуществляться при участии воды (гидролитическое дезаминирование) R CHNH2COOH + H2O ® R CHOH – COOH + NH3; кислорода (окислительное дезаминирование) R CHNH2COOH + O2 ® R–СО–COOH + NH3 и водорода (восстановительное дезаминирование) R CHNH2COOH + H2 ® R CH2COOH + NH3. Процесс разложения продуктов гидролиза белковых соединений микроорганизмами с выделением аммиака называется аммонификацией. Вместе с тем катионы аммония могут появляться и другим путем – из неорганических соединений. Замечено присутствие NH4+ в болотистых водах, богатых гумусовыми веществами, которые, по-видимому, способны восстанавливать нитраты до NH4+. Нитраты и нитриты могут быть восстановлены до NH4+ и другими веществами, например, сероводородом и железом (II). Кроме того, NH4+ часто попадает в водоемы в составе промышленных сточных вод, например, азотно-туковых, содовых, коксо-газовых и других заводов. Наличие аммиака в воде всегда вызывает подозрение в загрязнении воды сточными водами. В природной воде аммиак довольно неустойчив и под влиянием нитрифицирующих бактерий окисляется сначала до азотистой кислоты, а затем до азотной кислоты (реакции нитрификации) 2 NH3 + О2 = 2 НNО2 + 2 Н2О (NH4)2СО3 + 3 О2 = 2 НNО2 + СО2 + 3 Н2О 2 НNО2 + О2 = 2 НNО3 Другим важнейшим источником непосредственного обогащения природных вод нитратами являются получающиеся при атмосферных электрических разрядах оксиды азота, которые после поглощения атмосферными водами попадают на земную поверхность. Нитратные ионы встречаются в поверхностных природных водах в количествах несколько больших, чем нитритные. В то же время в подземных водах содержание нитритов обычно значительно выше, особенно в верхних водоносных горизонтах. При исследовании поверхностных вод по соотношению содержания в них аммиака, нитритов и нитратов можно судить о времени загрязнения воды. Так, наличие в воде аммиака и отсутствие нитритов указывает на свежее загрязнение воды. Отсутствие аммиака в воде при наличии нитритов и особенно нитратов свидетельствует, что загрязнение воды произошло давно, и прошел процесс самоочищения. Соединения фосфора. Минеральный фосфор в природных водах в растворенном состоянии находится главным образом в виде гидрофосфат-иона НРО42–, в меньшей мере дигидрофосфат- иона Н2РО4–, еще меньше фосфат – иона РО43–. Содержание тех или иных ионов ортофосфорной кислоты определяется реакцией среды. Органический растворенный фосфор является составной частью сложных органических соединений. Фосфор может находиться в природной воде и во взвешенных частицах как минерального, так и органического происхождения. Соединения фосфора, хотя и присутствуют в природных водах в ничтожных количествах, имеют исключительно важное значение для развития растительной жизни, являясь зачастую одним из факторов, лимитирующих и определяющих развитие растительных организмов и, следовательно, продуктивность водоемов. Именно увеличение содержания фосфора в пресных водоемах обычно становится причиной их эвтрофирования. Соединения железа очень часто встречаются в природных водах вследствие перехода их в раствор из различных горных пород, в которых железо широко распространено. Переход железа в раствор может происходить под действием окислителей или кислот. В болотистых водах железо часто находится в виде сложных гумусовых комплексов. Форма, в которой железо находится в природных водах, может быть весьма разнообразной. Преобладающее в подземных водах закисное железо присутствует в воде водоемов в виде растворимых солей гидрокарбоната железа (II) Fe(HCO3)2 и карбоната FeCO3, которые устойчивы только при содержании больших количеств СО2 и отсутствии кислорода. В противном случае происходит гидролиз, и железо переходит в малорастворимый гидроксид железа (II) Fe(HCO3)2 + 2 Н2О = Fe(OН)2 + 2 Н2СО3, который далее легко окисляется в гидроксид железа (III) 4 Fe(ОH)2 + О2 + 2 Н2О = 4 Fe(ОH)3. Процесс окисления во многих случаях протекает при участии микроорганизмов, которые используют выделяющуюся при этом энергию в процессе жизнедеятельности. Fe(ОH)3 очень мало растворим, но может присутствовать в растворе в коллоидном состоянии, которое, по-видимому, является основной формой существования железа в поверхностных водах. Воды, содержащие железо в значительных количествах, обычно имеют кислую реакцию среды. Это характерно для железистых вод, если происхождение железа связано с растворением сульфата железа (III). Fe2(SO4)3 + 6 H2O = 2 Fe(OH)3 + 3 H2SO4 Соединения железа (III) чаще встречаются в поверхностных водах (сотые, реже десятые доли мг/дм3), соединения железа (II) –преимущественно в подземных водах в несколько больших количествах (до 1 мг/дм3). Соединения кремния. Повсеместное распространение кремния в природе обеспечивает его непрерывное поступление в природные воды в виде выщелачиваемой водой кремневой кислоты и ее щелочных солей, содержащих ионы HSiO3– и SiO32–, а часть кремния находится в коллоидном состоянии, в частицах состава SiO2´ Н2О, а также в виде поликремневой кислоты состава х SiO2 ´уН2О. Кроме того, в водах присутствуют и органические соединения кремния. Наибольшие количества кремния встречаются в подземных водах, наименьшие – в поверхностных слоях открытых водоемов, где растения потребляют кремний. Обычно содержание кремния в открытых водоемах колеблется от десятых долей мг/дм3 в морях до 10 мг/дм3 в водах суши. Токсичные вещества. К этой группе веществ относят тяжелые металлы (ртуть, кадмий, свинец и др.), нефтепродукты, хлорорганические и другие пестициды, фенолы, синтетические поверхностно-активные вещества (СПАВ) и т.д. Взвешенные вещества. Содержание взвешенных веществ в воде называется мутностью и выражается в г/м3 или мг/дм3. Мутность речной воды зависит от скорости течения и расхода воды. Основная причина наличия взвешенных частиц – эрозия русла и склонов. В некоторых водоемах источником взвешенных веществ органического происхождения является планктон, развитие которого наблюдается преимущественно в летние месяцы. Производственные сточные воды нередко содержат значительные количества взвешенных частиц. Допустимое увеличение концентрации их в природных водах жестко нормируется.
1.3. Классификация природных вод по степени минерализации
Химический состав природных вод очень разнообразен и изменчив. Существует несколько классификаций воды (по происхождению, по целевому назначению и др.), но одной из важнейших является классификация по степени минерализации, т.е. по сумме растворенных в воде минеральных солей. Согласно ГОСТ 17403 – 72 природные воды по степени минерализации подразделяются следующим образом: пресные воды – от 0 до 1,0 г/кг; солоноватые воды – от 1,0 до 25 г/кг; соленые воды – от 25 до 50 г/кг; рассолы – более 50 г/кг. Предел пресных вод по степени минерализации до 1,0 г/кг основан на восприятии человеком вкуса солености свыше этой величины. Граница между солоноватыми и солеными водами установлена Н.М. Книповичем на том основании, что при минерализации 24,685 г/кг температура замерзания и температура наибольшей плотности морской воды совпадают и меняются многие свойства воды, влияющие на гидрологический режим. Граница 50 г/кг между солеными водами и рассолами принята потому, что соленость выше этой величины в морях не наблюдается, а характерна она только для соленых озер и высокоминерализованных подземных вод. Для пресных вод плотность воды близка к единице, поэтому минерализацию речных вод часто измеряют в мг/дм3. Речные воды по величине минерализации подразделяются следующим образом: воды малой минерализации – до 200 мг/дм3; воды средней минерализации – от 200 до 500 мг/ дм3; воды повышенной минерализации – от 500 до 1000 мг/дм3; воды высокой минерализации – более 1000 мг/дм3. Воды большинства рек земного шара имеют малую и среднюю минерализацию. Озерные воды по степени минерализации подразделяются на три группы: пресные – до 1 г/кг; солоноватые – от 1 до 25 г/кг; соленые – более 25 г/кг. Классификация вод по их минерализации систематизирует воды в общих чертах и не учитывает содержание отдельных ионов и газов. В соответствии с гигиеническими требованиями к качеству питьевой воды минерализация не должна превышать 1000 мг/дм3. По согласованию с органами санэпиднадзора, допускается использовать воду артезианских скважин с минерализацией до 1500 мг/дм3.
Сточные воды
Сточными водами называются воды, поступающие от населенных пунктов, промышленных или сельскохозяйственных предприятий и иных объектов, подлежащие очистке от различных примесей. В зависимости от происхождения и качественных характеристик примесей сточные воды можно разделить на четыре основные категории: – промышленные; – сельскохозяйственные; –хозяйственно-бытовые (коммунальные, фекальные); – атмосферные (или дождевые, ливневые). К хозяйственно-бытовым сточным водам относятся стоки душевых, бань, прачечных, столовых, туалетов и др. Содержание в них азота составляет в среднем 25-30 мг/дм3, а фосфора - 6-8 мг/дм3.Они содержат различные примеси, из которых примерно 58 % органических и 42 % минеральных веществ. Принято считать, что в сточные воды в сутки поступает на одного человека в граммах: аммонийного азота – 7– 8; хлоридов – 8–9; калия – 3; фосфатов – 1,5–1,8; органических веществ – 5–7. Из органических веществ в сточных водах присутствуют мочевина (до 40%), мыла (до 23,5%), жиры, крахмал и т.д. Одним из самых загрязненных составляющих бытового стока является моча. В ее составе обнаружено 229 химических соединений, в том числе 103 азотсодержащих вещества, 30 электролитов, 22 витамина, 38 гормонов, 10 энзимов, а также углеводы, липиды, органические кислоты. Атмосферные сточные воды образуются в результате выпадения дождей или при таянии снега при смывании образующимися потоками воды загрязняющих веществ с селитебных территорий, в том числе городских улиц, промышленных площадок и т.д. Промышленными сточными водами называются жидкие отходы, которые образуются при добыче органического и неорганического сырья и его переработке в промышленную продукцию, а также в процессе изготовления из него товаров широкого потребления. В зависимости от конечного получаемого продукта и применяемой технологии они содержат разнообразные минеральные и органические вещества. Промышленные сточные воды подразделяются на условно чистые и грязные. Условно чистыми водами являются воды, получающиеся в процессах охлаждения, конденсации и т.д. Эти воды охлаждаются в городских прудах или градирнях, очищаются от механических примесей и масел, а затем возвращаются в производство при небольшой добавке свежей воды. Сельскохозяйственные сточные воды подразделяются на сточные воды от животноводческих комплексов и поверхностные стоки с полей. Первый тип сточных вод характеризуется большим количеством органических загрязнителей – до 10 г/дм3, высоким содержанием азота – до 1,5 г/дм3, содержание фосфора 0,06 - 0,10 г/дм3. Поверхностные сточные воды, поступающие в водные объекты, содержат вещества, используемые в качестве удобрений и средств защиты растений от вредителей (соединения азота, фосфора, калия, пестициды). Концентрация биогенов и пестицидов в них зависит от количества вносимых химикатов, а также от правильности их складирования, хранения и применения. Грязные сточные воды подлежат очистке. Они могут подвергаться механической, физико-химической, биологической очистке, при этом могут быть использованы как деструктивные, так и регенеративные методы. Процесс очистки может происходить как на предприятии, так и на городских биологических очистных сооружениях, причем в последнем случае на предприятии должны уменьшить содержание всех загрязняющих веществ до концентраций, не вызывающих нарушений работы активного ила в аэротенках. Сточные воды, направляемые на биологическую очистку, характеризуются величиной БПК и ХПК. БПК – это биохимическое потребление кислорода, или количество кислорода, использованного при биохимических процессах окисления органических веществ (исключая процессы нитрификации) за определенный промежуток времени (2; 5; 8; 10; 20 суток). ХПК – это химическое потребление кислорода, т.е. количество кислорода, эквивалентное количеству расходуемого окислителя, необходимого для окисления всех восстановителей, содержащихся в воде. В качестве окислителя используют дихромат калия в среде концентрированной серной кислоты. Если ХПК существенно превышает БПК, это свидетельствует о высоком содержании биохимически неокисляющихся веществ. Эвтрофикация водоемов
Эвтрофирование – повышение биологической продуктивности водных объектов в результате накопления в воде биогенных элементов под действием антропогенных и естественных факторов. Эвтрофирование представляет собой естественный процесс эволюции водоема. С момента «рождения» водоем в естественных условиях проходит несколько стадий в своем развитии: на ранних стадиях от ультраолиготрофного до олиготрофного, далее становится мезотрофным и в конце концов водоем превращается в эвтрофный и гиперэвтрофный – происходит «старение» и гибель водоема с образованием болота. Если в естественных условиях эвтрофирование какого-либо озера протекает за 1000 лет и более, то в результате антропогенного воздействия это может произойти в сто и даже тысячу раз быстрее. Антропогенная эвтрофикация связана с поступлением в водоемы значительного количества биогенных веществ, прежде всего азота и фосфора. Если отношение содержания общего азота к содержанию общего фосфора меньше 10, то первичная продукция фитопланктона лимитируется азотом, при N: P > 17 – фосфором, при N: P = 10-17 – азотом и фосфором одновременно. Для водоемов умеренной зоны решающую роль играет фосфор. В настоящее время критическими концентрациями азота и фосфора (включая общий фосфор, ортофосфаты, общий азот и растворенный неорганический азот аммоний, нитриты и нитраты) во время интенсивного перемешивания вод, при котором создаются потенциальные условия для цветения водорослей, считаются следующие: для фосфора 0,01 мг/дм3, для азота 0,3 мг/дм3. Биогенные компоненты поступают в природные экосистемы как водным, так и воздушным путем. Основными загрязнителями водоемов биогенными веществами служат азотные и фосфорные удобрения, отходы животноводства, фосфорсодержащие пестициды. К эвтрофированию может привести строительство водохранилищ без надлежащей очистки ложа, строительство плотин, образование застойных зон, тепловое загрязнение воды, сброс сточных вод, особенно коммунально-бытовых, содержащих детергенты, в том числе и прошедших биологическую очистку, Основные критерии для характеристики эвтрофирования водоемов – это: · уменьшение концентрации растворенного кислорода в водной толще; · увеличение содержания взвешенных частиц, особенно органического происхождения; · увеличение концентрации фосфора в донных отложениях; · уменьшение проникновения света (возрастание мутности воды); · увеличение концентрации газов, образующихся при разложении органических остатков при недостатке кислорода – аммиака, метана, сероводорода; · показатель кислотности воды при 100% насыщении кислородом (рН100%); · последовательная смена популяций водорослей с преобладанием сине-зеленых и зеленых водорослей; · значительное увеличение биомассы фитопланктона; · обнаружение альгитоксинов. В качестве прямого индикатора трофического состояния водоема обычно используется концентрация хлорофилла «а», который является основным фотосинтетическим пигментом. Значение его концентрации в пробе воды является репрезентативным индикатором биомассы водорослей, точной мерой эвтрофирования водоемов. Поэтому определение хлорофилла «а» регулярно используется при измерении «откликов» водоемов на биогенную нагрузку с целью их восстановления. Вследствие массового размножения сине-зеленых водорослей, вызывающих «цветение» воды, ухудшаются условия жизни гидробионтов и качество воды, прежде всего, ее органолептические свойства. Сине-зеленые водоросли в результате своей жизнедеятельности производят при определенных условиях сильнейшие токсины, которые представляют опасность для живых организмов и человека. Они не имеют ни цвета, ни запаха, не разрушаются при кипячении. Альгитоксины по своей токсичности не имеют себе равных. Они могут вызывать цирроз печени, дерматиты у людей, отравление и гибель животных. Фактором риска при использовании воды эвтрофированных водоемов является создание в них благоприятных условий для развития промежуточных форм возбудителей и переносчиков паразитарных болезней.
Самоочищение водоемов
Поступающие в водоем загрязнения вызывают в нем нарушение естественного равновесия. Способность водоема противостоять этому нарушению, освобождаться от вносимых загрязнений и составляет сущность процесса самоочищения. Самоочищение водных систем обусловлено многими природными, а иногда и техногенными факторами. К числу таких факторов относятся различные гидрологические, гидрохимические и гидробиологические процессы. Условно можно выделить три типа самоочищения: физическое, химическое, биологическое. Среди физических процессов первостепенное значение имеет разбавление (перемешивание). Хорошее перемешивание и снижение концентрации взвешенных частиц обеспечивается интенсивным течением рек. Способствует самоочищению водоемов отстаивание загрязненных вод и оседание на дно нерастворимых осадков, сорбция загрязняющих веществ взвешенными частицами и донными отложениями. Для летучих веществ важным процессом является испарение. Среди химическим факторов самоочищения водоемов главную роль играет окисление органических и неорганических веществ. Окисление происходит в воде при участии растворенного в ней кислорода, поэтому чем выше его содержание, тем быстрее и лучше протекает процесс минерализации органических остатков и самоочищения водоема. При сильном загрязнении водоема запасы растворенного кислорода быстро расходуются, а накопление его за счет физических процессов газообмена с атмосферой протекает медленно, отчего самоочищение замедляется. Самоочищение воды может происходить и вследствие некоторых других реакций, при которых образуются трудно растворимые, летучие или нетоксичные вещества, например, гидролиза пестицидов, реакции нейтрализации и др. Содержащиеся в природной воде карбонаты и гидрокарбонаты кальция и магния нейтрализуют кислоты, а растворенная в воде угольная кислота нейтрализует щелочи. Под влиянием ультрафиолетового излучения солнца в поверхностных слоях водоема происходит фоторазложение некоторых химических веществ, например ДДТ, и обеззараживание воды – гибель патогенных бактерий. Бактерицидное действие ультрафиолетовых лучей объясняется их влиянием на протоплазму и ферменты микробных клеток, что вызывает их гибель. Ультрафиолетовые лучи оказывают губительное воздействие на вегетативные формы бактерий, споры грибов, цисты простейших, вирусы. Каждый водоем – это сложная живая система, где обитают бактерии, водоросли, высшие водные растения, различные беспозвоночные животные
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 166; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.21.103.209 (0.088 с.) |