
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Термодинамический процесс и равновесное состояниеСтр 1 из 6Следующая ⇒
Лекция №1 Введение Одной из основных проблем современного производства, является надёжное обеспечение топливо энергетическими ресурсами. В связи с повышением количества потребителей энергетических ресурсов и возрастания их стоимости, всё более актуальны становятся проблемы повышения эффективности использования топлива, снижения потребления топлива и загрязнения окружающей среды. Главным путем решение эффективности и всестороннее применение энергосберегающих технологий. Учёные биологи утверждают,что от тепловой “смерти” биосферы, человечество отделяет один порядок величин. Если будем использовать в 10 раз больше энергии, чем сейчас, то биосфера погибнет. Проблема заключается в так называемом парниковом эффекте, содержащийся в атмосфере Диоксид углерода пропускает солнечные лучи, но препятствует охлаждению земли путём излучению теплоты в космос. В связи с этим, необходимо снижать в энергетике долю углеродосодержащих топлив. Между тем около 90% всей используемой человечеством энергии приходится на ископаемые, органические топлива(нефть, природный газ, уголь). Кроме выброса углекислого газа в атмосферу, топливо энергетические выбросы производят загрязнение атмосферы: тепловое загрязнение (выбросы нагретой воды и газов),выбросы залы и сажи. Всё это, с увеличением масштабов производства создаёт большие проблемы для человечества. Экологические факторы также заставляют увеличить степень использования топлива. Процент использования топлива в промышленности не превышает <35-40%. 60-65% - загрязняет окружающую среду. КПД бензинного 30-40% КПД дизельного 35-50% Очевидно, что гораздо эффективнее изобретать новый более эффективный вид топлива, чем строить предприятия изготавливающих бензинное и дизельное топливо. Тем более, что запасов нефти осталось на 50 лет. Теплотехника – это наука и отрасль техники, изучающая методы получения, преобразования и использования теплоты,а так изучает устройство и принцип работы связанных с этим аппаратов и устройство. Знание теплотехники необходимо для оптимизации использования топлива и выявления возможности использования вторичных энергетических ресурсов. Существует 2 принципиально различных направления использования теплоты:
1)энергетических (ДВС) 2)Технологическое (при энергетическом использовании теплота преобразуется в механическую работу или другие виды энергии с помощью тепловых машин. При технологическом использовании теплота необходимо для изменения физических свойств различных материалов: плавление металла, изменение структуры и протекания большинства химических процессов в химической промышленности.) Тепловая машина – это устройство, в котором тепловая энергия (теплота сгорания топлива) Преобразуется в механическую работу (перемещение и вращение). Виды тепловых машин: 1)Поршневые двигатели 2)Роторные двигатели 3)Газотурбинные двигатели 4)Реактивные двигатели. По способу подвода теплоты 1) Термодинамика а) физическая термодинамика – дает представления об общих законах преобразования энергии. б) химическая термодинамика – изучает процессы обмена теплотой с изменением химического состава. в) техническая термодинамика – изучает процесс взаимного превращения теплоты и работы, свойств различных тел, особенности протекания термодинамических процессов и циклов. 2) Теория теплообмена а) Виды теплообмена б) Способы теплопередачи – позволяет выполнить расчёт теплообменного аппарата и тепловой изоляции. в) Промышленная теплотехника – изучает использование теплоты в различных отраслях, исследует различные виды топлива (в том числе альтернативные),особенности процесса горения, принцип действия и устройство теплоэнергетических установок,систем теплоснабжения, паровых и газовых турбин, ДВС.
Лекция № 2 Предмет Термодинамики Термодинамика – это наука о взаимном превращении теплоты и других видов энергии. Термодинамика возникла в начале XIX века, и состоит из слов therme – тепло, dynamis – сила. И называлась как наука связанная с теплотой. Термодинамика основана на 3-х законах(началах): 0 закон – закон теплового равновесия междутелами – согласно этому закону, изолированная термодинамическая схема стремится к состоянию теплового равновесия, и после его достижения не может самопроизвольно выйти из данного состояние.
1 закон – закон сохранения энергии применительно к термодинамическим процессом – согласно этому закону, невозможен процесс возникновения или исчезновения энергии, которая может только преобразовываться одного вида в другой. 2 закон – определяет направление протекания реальных термодинамических процессов – не возможен процесс имеющий, единственным своим результатом превращение теплоты в работу. Термодинамический метод исследования основан на законах термодинамики и представляет их логическое и математическое развитие. Объектом исследования в термодинамике – является термодинамическая система, или рабочее тело тепловой машины. Термодинамика основана дедуктивно, частные выводы получены из общих законов. Термодинамика наука феноменологическая, она рассматривает вещество как сплошную среду и использует для его исследования макропараметры, давление, температуру, объем. Определяемые путём прямого измерения (с помощью физических приборов). Кроме данного подхода, существует ещё статический подход. В этом случае, вещество рассматривается как совокупность огромного количества микрочастиц и о состоянии вещества, судят и о характере движения примером служит молекулярно-кинетическая теория.
В термодинамике давление измеряется с помощью манометра. Достоинства Термодинамического метода исследования: 1) Результат исследования не зависит от наших знаний структуры вещества. 2) Более простой математический аппарат. Достоинства статического подхода: 1) Более высокая наглядность. Техническая термодинамика с помощью термодинамического метода исследования, устанавливает закономерности взаимного преобразования теплоты и работы, для чего изучает свойства газов и устанавливает взаимосвязь между тепловыми, механическими и химическими процессами протекающими в тепловых двигателях и холодильных установках. Одна из основных задач термодинамики – это отыскание рациональных способов преобразования теплоты в работу, или работу в теплоту(в холодильных машинах). Термодинамическая система Термодинамическая система (ТДС) – это совокупность макроскопических тел являющихся объектом изучения и как правило обменивающихся энергией как друг с другом, так и с окружающей средой. Макроскопические тела – это тела имеющие массу, соизмеримую с массой окружающих их тел, являющихся объектом их изучения. Тело не входящее в состав окружающей системы называется внешней средой(окружающей средой). Изолированная ТДС – не обменивается с внешней средой теплотой. Замкнутая ТДС – не обменивается с внешней средой работой. Закрытая ТДС – не обменивается с внешней средой веществом, т.е. её состав остаётся неизменным. На пример в теоретическом двигателе отсутствует потеря рабочего тела. Открытая ТДС – обменивается с внешней средой не только энергией, но и веществом. Открытая система очень сложна в расчетах и рассматриваться не будет. Лекция №3 Лекция №4 Уравнение состояния. Если система предоставлена сама себе, то через некоторое время (время релаксации) в системе установится равновесие, при этом значение параметров в различных точках системы выравниваются между собой и будут однозначно связанны определённым соотношением, которое называется уравнением состояния данной системы.
Уравнение состояния ТДС связывающие между собой давление, объём и температуру называется уравнением состояния ТДС. f(PVT) f- зависит от свойств данной системы. Любой из параметров данной функции можно определить зная два других: P=f(TV) V=f(TP) T=f(PV) Вопрос получения уравнений состояния достаточно сложен и полностью не решен даже для газов. Уравнение состояния получено методами статической физики в рамках МКТ а также империческим (опытным) экспериментальным путём для газов близких по свойствам к идеальным. Идеальным газом называется газ в котором: 1. Отсутствуют силы взаимодействия между молекулами. 2. Пренебрегают объёмом молекул. 3. Столкновения молекул между собой и со стенками системы являются абсолютно упругими. В реальных газах: 1. молекулы занимают некоторый объём. 2. междуними действуют силы притяжения и отталкивания. Учёт этих факторов значительно усложняет термодинамический расчёт, однако, свойства реального газа во многих практических условиях достаточно близки к свойствам идеального газа. Лекция №8 Теплоёмкость Теплоёмкость – это количество теплоты, которое требуется подвести или отнять от тела для изменения его температуры на один градус, обозначается С, измеряется в [
Отсюда можно определить количество теплоты Q, которое требуется подвести к телу, для изменения его температуры на необходимое количество градусов.
Значение теплоёмкости индивидуально для каждого вещества, определено экспериментальным путём и приводится в справочниках. Теплоёмкость зависит от: 1) Характера процесса при котором подводится или отводится теплота · CV – теплоёмкость определяемая при растущем объёме. · Cp – теплоёмкость определяемая при растущем давлении. 2) Температуры тела: в практических инженерных расчётах данная зависимость приходится учитывать. Количество подведенной теплоты в процессе рассчитывается по формуле:
В предварительных расчётах среднее значение теплоёмкости в данном температурном диапазоне, то есть она принимается постоянной.
В зависимости от способа задания количества вещества используют теплоёмкости: · Удельная теплоёмкость (C
· Объёмная теплоёмкость (C’ · Молярная теплоёмкость ( Рассмотрим процессы подведения теплоты, происходящие при: 1. В изохорном процессе вся подводимая теплота идёт только на увеличение внутренней энергии (температуры).
2. В процессе с постоянным давлением часть теплоты пошла на увеличение внутренней энергии (температуры), а часть теплоты пошла на совершение работы равной: (работа изменения объёма)
Таким образом, в изобарном процессе с подвижным поршнем, потребовалось большее количество теплоты для изменения температуры на один градус, на величину энергии соответствующую совершенной работе. Связь между изохорной и изобарной теплоёмкостями устанавливает уравнение Маера:
Из данного уравнения хорошо виден смысл газовой постоянной R. Физический смысл газовой постоянной заключается в том, что она численно равна работе совершаемой газом при нагревании его на один градус при росте давлении.
Политропный процесс – это термодинамический процесс, который объединяет в себе изопроцессы, а так же промежуточные процессы. При политропном процессе остаётся постоянная теплоёмкость. Уравнение политропы имеет вид:
Где n – показатель политропного процесса.
Примеры политропных процессов: 1. Изобарный 2. Изохорный 3. Изотермический 4. Адиабатный
Лекция №9 Второй закон термодинамики Лекция №10 Круговые процессы или термодинамические циклы. Условие работы тепловых машин.
Тепловая машина – это устройство преобразующие тепловую энергию в механическую работу при циклическом процессе теплообмена между термодинамической системой (рабочим телом тепловой машины) и источником теплоты. Рабочим телом является газ, по средством которого осуществляется преобразование теплоты в работу. Для того чтобы от тепловой машины получить полезную работу необходимо выполнить следующие условия: 1. Необходимо иметь рабочее тело 2. Необходимо наличие двух источников теплоты: нагреватель и охладитель. Для того чтобы рабочее тело совершив ряд процессов вернулось в исходное состояние. Должен совершится термодинамический цикл. Термодинамический цикл – совокупность термодинамических процессов, после совершения которых система возвращается в исходное положение.
При подводе теплоты Q1 от нагревателя с температурой Т1 совершается процесс 1-а-2, в ходе которого система совершает положительную работу L, численно равную площади под линией процесса. В процессе 2-в-1 от рабочего тела отводится теплота в количестве Q2 к охладителю с температурой Т2. В процессе сжатия затрачивается работа L2 (отрицательная работа системы) так как она совершается внешними силами. Работа системы равна сумме работ во всех циклах. Уравнение первого закона термодинамики для процессов 1-а-2 и 2-в-1 соответственно будут иметь вид:
Чтобы получить полезную работу цикла работа затраченная на сжатие должна быть меньше работы совершаемой системой при расширении. Необходимо одновременно со сжатием охлаждать рабочее тело отнимая у него теплоту Q2. Если при сжатии не охлаждать рабочее тело, то полезная работа будет равна нулю. Степень совершенства тепловой машины оценивается коэффициентом полезного действия.
Коэффициент полезного действия тепловой машины всегда меньше единицы так как часть теплоты в количестве Q2 отводится в окружающую среду. Полное превращение теплоты в работу, по средствам тепловой машины не возможно. Цикл тепловой машины. Цикл холодильной машины. Цикл тепловой машины направлен по часовой стрелке. Работа расширения всегда больше работы сжатия.
На участке 1-2 создаётся разряжение в следствии чего температура рабочего тела уменьшается, и становится ниже температуры охлаждаемого тела. На участке 2-1 рабочее тело сжимается в результате чего его внутренняя энергия повышается. В следствии совершения внешними силами работы L над рабочим телом, происходит отвод теплоты Q2 от охлаждаемого тела и передача теплоты Q1 к тепловому резервуару (окружающей среде), причём Q1 больше чем Q2. Степень совершенства тепловой машины оценивается коэффициентом:
Цикл Карно Цикл Карно – это идеальный термодинамический цикл, тепловая машина работающая по этому циклу обладает максимальным КПД. Цикл Карно состоит из двух адиабатных и двух изотермических процессов. Изотермические и адиабатные процессы являются самыми выгодными для получения работы из определённого количества теплоты, в изотермическом процессе вся теплота, подводимая к рабочему телу превращается в работу, а адиабатный процесс протекает без потерь теплоты так как отсутствует теплообмен с окружающей средой и работа совершается за счёт уменьшения внутренней энергии. Кроме того одним из важных свойств цикла Карно является его обратимость
Лекция №11 Энтропия Обмен энергией может происходить в форме работы и в форме теплоты. Работа совершается системой в случае изменения объёма или перемещения всей системы.
Работа может быть изображена на графике площадью под линией процесса. Работа зависит от значения давления и объёма. В случае передачи энергии в форме теплоты значение энергии в некоторых случаях возможно получить по известной формуле однако, измеряя значение температуры не всегда можно определить количество переданной теплоты (при подводе теплоты к кипящей воде её температура не меняется). В 1852 году Клаузис предложил параметр, который изменялся только в случае подвода или отвода теплоты (энтропия) Энтропия – функция состояния термодинамической системы дифференциал которой равен количеству подведённой теплоты отнесённому к температуре процессу
dQ – элементарное количество теплоты подведённое к системе при постоянной температуре Т. Данная формула является математической записью второго закона термодинамики для обратимых процессов. Вывод из второго закона термодинамики: энтропия системы при совершении необратимых процессов возрастает. Энтропия может быть измерена и определена только только расчётным путём – также как потенциальная энергия тела. Количество подводимой теплоты к системе из данной формулы можно записать в виде интеграла: Как следует из формул:
dQ=TdS
Существует следующая зависимость: dS>0 dQ>0 dS<0 dQ<0 Тепловая диаграмма T-S. Тепловая диаграмма T-S – это графическая зависимость между температурой и энтропией, она имеет широкое применение при исследовании и расчёте термодинамических процессов и циклов, значительно упрощает и повышает наглядность термодинамических исследований.
Изобарный и изохорный процесс в T-S координатах
Расчёт КПД цикла Карно с помощью тепловой диаграммы

Лекция №12 Цикл Дизеля Цикл дизеля имеет преимущество перед циклом Отто при использовании в ДВС.В цикле дизеля, можно увеличить степень сжатия (т.к. воздух не самовоспламеняется) В цикле Дизеля ɛ=16-22 Подача топлива в цикле Дизеля методом распыления сжатым воздухом(от компрессора в момент прихода поршня в ВМТ) и продолжается в процессе расширения(движение поршня в НМТ)
AC – Адиабатное сжатие ТС=3000 С ZB – адиабатное сжатие ηотто = 30-40% ηдизеля =35-45% Если степень сжатия более 20 единиц, то возрастает расход работы на преодоление сил трения. Оптимальной является степень сжатия при которой сумма КПД будет максимальной. Цикл дизеля состоит из 2-х адиабат: сжатия и расширения, изохоры и изобары. Характеристика цикла 1) 2) 3) Цикл дизеля используется на стационарных двигателях.
Лекция №14: Цикл Тринклера 1)Цикл с комбинированным отводом теплоты 2)Цикл современного дизельного двигателя Стремление упростить конструкцию, снизить нагрузки действующие на детали двигателя, привело к разработке со смешанным подводом теплоты. Теплота подводится после процесса сжатия, сначала при V=const, затем при P=const. Цикл состоит из: 1)2 адиабат 2)2 изохор 3)1 изобара
АС – адиабатное сжатие в точке С происходит впрыск топлива протекает быстрая фаза сгорания в точке Z продолжается впрыск топлива,в результате чего продолженая по изобаре Z-Z1 CZ1 - изохорный подвод теплоты ZZ1- изобарный подвод теплоты Z1B- адиабатное расширение BA – изобарный отвод теплоты
Характеристиками данного цикла являются 1) 2) 3) Отсюда видно,что на увеличение КПД влияетповышение степени сжатия и степени повышения давления λ и увеличения k (показатель адиабаты для воздуха).А с увеличением ϴ расширения КПД уменьшается. Лекция №15: Сгорание топлива Процесс сгорания топлива проходит в камере сгорания ДВС после совершения процесса сжатия. Топливо воспламеняется либо, от электрической искры (от свечи зажигания) в бензиновых двигателях работающих по циклу Отто (цикл быстрого сгорания), либо топливо самовоспламеняется в момент впрыска его топливной форсункой в раскалённый воздух камеры сгорания (цикл Дизеля и Тринклера). Нормальный процесс сгорания протекает с дозвуковой скоростью,жесткость работы двигателя при этом, и нагрузка на детали КШМ, цилиндропоршневой группы, и другие детали двигателя находится в допускаемых пределах, в том числе и по температурному режиму. При детонационном сгорании процесс сгорания протекает со сверхзвуковой скоростью, что приводит к значительным перегрузкам. Приводит в первую очередь к прогоранию поршня, поломке колец и т.о. Медленное сгорание имеет место при обеднённой бензо-воздушной смеси, либо при использовании в качестве топлива СПДТ. (смесь пропаново-бутановая топливная) Сгорание топлива – это быстропротекающая химическая реакция окисления углеводородом топлива, кислородом содержащимся в воздухе. В процессе сгорания межмолекулярные связи топлива разрываются. При сгорании 1 кг топлива выделяются следующее количество теплоты: Hб = 44 МДж/кг – теплотворная способность бензина Hд = 42 МДж/кг – теплотворная способность дизельного топлива Hгаз = 34 МДж/кг – теплотворная способность газа Конечная реакция сгорания углеводорода и водорода: 2Н2 + О2 = 2Н2О С + О2 = С2О Теоретическое количество топлива необходимое для сгорания 1 кг бензина равна 14,5 кг воздуха. Коэффициент избытка воздуха – это отношение действительного количества воздуха, поступающего в двигатель, теоретического необходимого для сгорания.
В процессе работы двигателя, работающего в различных режимах изменяются. При повышении нагрузки на двигатель смесь обогащается
Лекция №16 Теплопередача. Теполопередача (теплообмен) – наука о самопроизвольных процессах передачи теплоты в пространстве с неоднородным температурным полем. При проектировании различных теплосиловых установок: тепловых двигателей, холодильных машин, компрессоров и так далее, необходимо обязательно учитывать процессы переноса теплоты. Выбор процесса (способа для защиты конструкции от перегрева) часто становится определяющим при разработке компоновки и общей конструкции теплосилового устройства. Для того, чтобы конструкция работала надёжно необходимо предусмотреть некоторые меры, которые ограничели бы максимальную температуру различных деталей и узлов установки. В противном случае установка может разрушится так как конструкционные материалы при нагревании теряют прочность, а также могут нарушиться зазоры в сопряжениях трущихся пар, что значительно усилит износ, либо приведёт к заклиниванию деталей. Виды переноса теплоты: · Теплопроводность · Конверсия · Излучение На практике редко встречается один вид переноса теплоты, то есть имеет место сложный процесс переноса теплоты. Теплопроводность – процесс передачи теплоты на молекулярном уровне. Имеет место в твёрдых телах, незначительно присутствует в жидкостях и газах, полностью отсутствует в вакууме. Излучение – процесс передачи теплоты в пространство через оптически прозрачные среды (в том числе через вакуум), связанно с распространением электромагнитных волн или индукцией фатонов, излучаемых любым телом имеющим температуру выше температуры абсолютного нуля. Конвенция – процесс передачи теплоты, связанный с перемещением в пространстве макротел (масс вещества) в жидкостях и газах. При этом уже не отдельные молекулы, а значительные (макроскопические) объёмы горячей жидкости или газа перемещаются в зону с более низкой температурой (за счёт действия сил Архимеда) тела имеющие меньшую плотность (массу единицы объёма) поднимаются вверх. В технике часто рассматривают два вида сложных процессов передачи теплоты: · Теплоотдача · Теплопередача
Данный способ передачи теплоты имеет место в теплообменных аппаратах. Лекция №1 Введение Одной из основных проблем современного производства, является надёжное обеспечение топливо энергетическими ресурсами. В связи с повышением количества потребителей энергетических ресурсов и возрастания их стоимости, всё более актуальны становятся проблемы повышения эффективности использования топлива, снижения потребления топлива и загрязнения окружающей среды. Главным путем решение эффективности и всестороннее применение энергосберегающих технологий. Учёные биологи утверждают,что от тепловой “смерти” биосферы, человечество отделяет один порядок величин. Если будем использовать в 10 раз больше энергии, чем сейчас, то биосфера погибнет. Проблема заключается в так называемом парниковом эффекте, содержащийся в атмосфере Диоксид углерода пропускает солнечные лучи, но препятствует охлаждению земли путём излучению теплоты в космос. В связи с этим, необходимо снижать в энергетике долю углеродосодержащих топлив. Между тем около 90% всей используемой человечеством энергии приходится на ископаемые, органические топлива(нефть, природный газ, уголь). Кроме выброса углекислого газа в атмосферу, топливо энергетические выбросы производят загрязнение атмосферы: тепловое загрязнение (выбросы нагретой воды и газов),выбросы залы и сажи. Всё это, с увеличением масштабов производства создаёт большие проблемы для человечества. Экологические факторы также заставляют увеличить степень использования топлива. Процент использования топлива в промышленности не превышает <35-40%. 60-65% - загрязняет окружающую среду. КПД бензинного 30-40% КПД дизельного 35-50% Очевидно, что гораздо эффективнее изобретать новый более эффективный вид топлива, чем строить предприятия изготавливающих бензинное и дизельное топливо. Тем более, что запасов нефти осталось на 50 лет. Теплотехника – это наука и отрасль техники, изучающая методы получения, преобразования и использования теплоты,а так изучает устройство и принцип работы связанных с этим аппаратов и устройство. Знание теплотехники необходимо для оптимизации использования топлива и выявления возможности использования вторичных энергетических ресурсов. Существует 2 принципиально различных направления использования теплоты: 1)энергетических (ДВС) 2)Технологическое (при энергетическом использовании теплота преобразуется в механическую работу или другие виды энергии с помощью тепловых машин. При технологическом использовании теплота необходимо для изменения физических свойств различных материалов: плавление металла, изменение структуры и протекания большинства химических процессов в химической промышленности.) Тепловая машина – это устройство, в котором тепловая энергия (теплота сгорания топлива) Преобразуется в механическую работу (перемещение и вращение). Виды тепловых машин: 1)Поршневые двигатели 2)Роторные двигатели 3)Газотурбинные двигатели 4)Реактивные двигатели. По способу подвода теплоты 1) Термодинамика а) физическая термодинамика – дает представления об общих законах преобразования энергии. б) химическая термодинамика – изучает процессы обмена теплотой с изменением химического состава. в) техническая термодинамика – изучает процесс взаимного превращения теплоты и работы, свойств различных тел, особенности протекания термодинамических процессов и циклов. 2) Теория теплообмена а) Виды теплообмена б) Способы теплопередачи – позволяет выполнить расчёт теплообменного аппарата и тепловой изоляции. в) Промышленная теплотехника – изучает использование теплоты в различных отраслях, исследует различные виды топлива (в том числе альтернативные),особенности процесса горения, принцип действия и устройство теплоэнергетических установок,систем теплоснабжения, паровых и газовых турбин, ДВС.
Лекция № 2 Предмет Термодинамики Термодинамика – это наука о взаимном превращении теплоты и других видов энергии. Термодинамика возникла в начале XIX века, и состоит из слов therme – тепло, dynamis – сила. И называлась как наука связанная с теплотой. Термодинамика основана на 3-х законах(началах): 0 закон – закон теплового равновесия междутелами – согласно этому закону, изол
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 47; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.135.224 (0.212 с.) |

 ]
] 
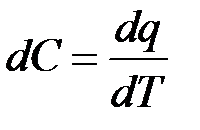
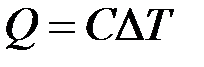


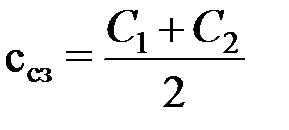

 ,C
,C  ) – показывает какое количество тепла необходимо подвести к одному килограмму вещества для изменения его температуры на один градус.
) – показывает какое количество тепла необходимо подвести к одному килограмму вещества для изменения его температуры на один градус. ,C’
,C’  ) – показывает какое количество тепла необходимо подвести к одному метру кубическому вещества для изменения его температуры на один градус.
) – показывает какое количество тепла необходимо подвести к одному метру кубическому вещества для изменения его температуры на один градус. C
C  C
C 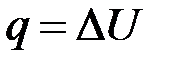
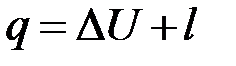
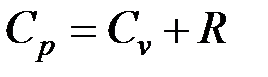
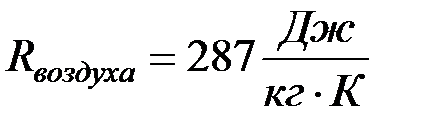



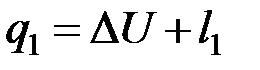
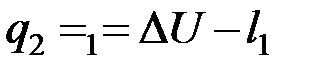
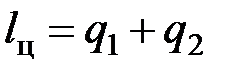

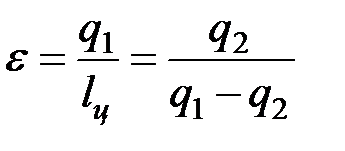
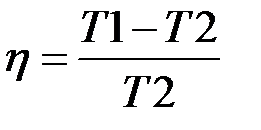
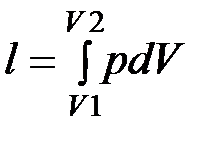

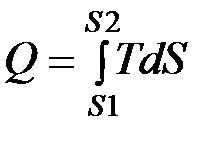

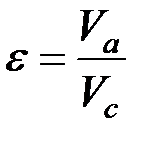 - степень сжатия
- степень сжатия – степень предварительного расширения
– степень предварительного расширения


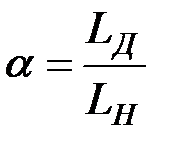
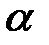 = 0,8…0,95. При движении в установившемся режиме с номинальной скоростью смесь обеднённая
= 0,8…0,95. При движении в установившемся режиме с номинальной скоростью смесь обеднённая 


