Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Колбе с кислородом взамен ст. ГФ XI, вып. 1
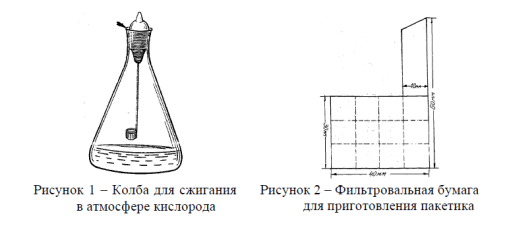
Метод сжигания в колбе с кислородом применяется для определения содержания брома, йода, селена, серы, фосфора, фтора и хлора в лекарственных средствах. Принцип метода состоит в разрушении органических веществ сжиганием в атмосфере кислорода, растворении образующихся продуктов сгорания в поглощающей жидкости и последующем определении элементов, находящихся в растворе в виде ионов.
Около 0,05 г (точная навеска) тонкоизмельченного образца испытуемого вещества или другое количество, указанное в фармакопейной статье, помещают в центр не содержащей галогенидов фильтровальной бумаги размером 30 × 40 мм, с выступающей узкой полоской шириной 10 мм и длиной 30 мм, заворачивают в виде пакетика, оставляя узкую полоску (рис. 2). При исследовании жидкости навеску помещают в капилляр, заплавленный парафином, или в капсулу (полиэтиленовую, из нитропленки или метилцеллюлозы). При исследовании жидких образцов объемом не более 200 мкл возможно использование капсул из поликарбоната. Для жидкостей возможно применение двойного бумажного пакетика. При исследовании мазеобразных веществ применяют капсулу (вместимостью не более 200 мкл) из нитропленки или пакетик из вощеной жиронепроницаемой бумаги. Капсулу или пакетик заворачивают в фильтровальную бумагу, как указано выше. Если при проведении определения требуется, чтобы фильтровальная бумага была пропитана лития карбонатом, следует увлажнить центр бумаги насыщенным раствором лития карбоната и высушить ее перед применением при 100 – 105 ºС. При исследовании твердых и мазеобразных веществ, сгорающих со вспышкой, к навеске прибавляют 3 – 5 мг парафина. Подготовленную пробу в пакетике из фильтровальной бумаги помещают в держатель (корзиночка или спираль). В колбу для сжигания наливают воду или другую поглощающую жидкость, указанную в фармакопейной статье, увлажняют горло колбы водой и пропускают в течение 3 – 5 мин ток кислорода через трубку, конец которой находится выше уровня жидкости. Затем осторожно поджигают узкий конец свободной полоски фильтровальной бумаги и немедленно плотно закрывают колбу пробкой, смоченной водой. Во время сжигания следует придерживать пробку рукой.
По окончании сжигания содержимое колбы встряхивают и оставляют на 30 – 60 мин при периодическом перемешивании. Стенки колбы, платиновую проволоку с корзиночкой и пробку промывают водой, промывные воды присоединяют к основному раствору и проводят определение элемента методом, указанным в фармакопейной статье. Параллельно проводят контрольный опыт. Примечание. При проведении работы необходимо надеть защитные очки, колбу поместить в предохранительный чехол, установить защитный экран. Колба для сжигания должна быть тщательно вымыта и свободна от следов органических веществ и растворителей. Определение хлора и брома Точную навеску вещества, указанную в фармакопейной статье, сжигают, как описано выше, используя в качестве поглощающей жидкости 20 мл водорода пероксида раствора 6 %. Стенки колбы и держатель образца обмывают 40 мл воды, прибавляют 5 капель бромфенолового синего раствора спиртового 0,1 % и нейтрализуют по каплям натрия гидроксида раствором 0,1 М до перехода желтой окраски в синюю. Затем прибавляют 1 мл азотной кислоты раствора 0,3 %, 5 капель раствора дифенилкарбазона и титруют ртути(II) нитрата раствором 0,005 М до перехода желтой окраски в светло-фиолетовую. 1 мл ртути(II) нитрата раствора 0,005 М соответствует 0,7091 мг хлора или 1,598 мг брома. Определение йода Точную навеску вещества, указанную в фармакопейной статье, сжигают, как описано выше, поглощая продукты сжигания 10 мл натрия гидроксида раствора 0,2 М. Шлиф и держатель обмывают 25 мл калия ацетата раствора 10 % в уксусной кислоте ледяной, к которому предварительно прибавляют 15 капель брома, затем пробку с держателем и стенки колбы тщательно промывают 40 мл воды, прибавляют по каплям муравьиную кислоту безводную 85 % до обесцвечивания раствора, 20 мл серной кислоты раствора 0,025 М, 0,5 г калия йодида и выдерживают в темном месте в течение 5 мин. Выделившийся йод титруют натрия тиосульфата раствором 0,1 М (индикатор – крахмал).
1 мл натрия тиосульфата раствора 0,1 М соответствует 12,69 мг йода. Определение фтора Определение проводят в соответствии с ОФС «Определение фтора». Определение серы Точную навеску вещества, указанную в фармакопейной статье, сжигают, как описано выше, используя в качестве поглощающей жидкости 15 мл водорода пероксида раствора 6 %. Держатель образца и стенки колбы обмывают 20 мл воды и упаривают содержимое колбы до 4 – 5 мл. К охлажденному раствору прибавляют 2 мл уксусной кислоты разведенной 30 %, 20 мл спирта 96 %, по 2 капли водного метиленового синего раствора 0,02 % и торина раствора 0,2 % и титруют бария нитрата раствором 0,01 М до перехода желто-зеленой окраски в розовую. 1 мл бария нитрата раствора 0,01 М соответствует 0,3207 мг серы. Примечания.
Установка титра. К 10 мл титрованного серной кислоты раствора 0,01 М прибавляют 40 мл воды, прибавляют по 2 капли метиленового синего раствора водного 0,02 % и торина раствора 0,2 % и медленно титруют приготовленным раствором бария нитрата до перехода желтой окраски в розовую. 1 мл серной кислоты раствора 0,01 М соответствует 2,614 мг бария нитрата.
Раствор хранят в защищенном от света месте в течение 7 дней. Определение фосфора Точную навеску вещества, указанную в фармакопейной статье, сжигают, как описано выше, используя в качестве поглощающей жидкости 10 мл серной кислоты раствора 0,05 М. Определение фосфора проводят в соответствии с ОФС «Спектрофотометрическое определение фосфора».
12. Проблемы, связанные со стабильностью во время хранения лекарственных средств (физические, химические и микробиологические). Привести примеры изменения состава и свойств препаратов при неправильном хранении (не менее 5 примеров) 1. Проблемы, связанные со стабильностью лекарственных средств во время хранения. Стабильность -- одна из важнейших характеристик лекарственного средства. Предприятие медицинской промышленности должно гарантировать содержание терапевтической дозы JIB в ЛФ в течение определенного срока. Это отражают в ФС или ФСП. Вопросам стабильности ЛС начали уделять внимание уже в те годы, когда налаживалось их первое промышленное производство, Однако подход к этой проблеме был чисто эмпирический. Повышение стабильности может быть достигнуто на основе исследования механизма химических процессов, происходящих при хранении ЛС, и создания способов ингибирования этих процессов. Процессы, происходящие при хранении ЛС, могут привести к изменению их химического состава или физических свойств (образованию осадка, изменению окраски или агрегатного состояния). Эти процессы приводят к постепенной потере фармакологической активности или к образованию примесей, изменяющих направленность фармакологического действия. Из физических факторов наибольшее влияние на стабильность лекарств оказывают температура, свет и влажность. Особенно велика роль температурного режима на стабильность ЛВ. Известно, что с повышением температуры резко возрастает скорость химических реакций. Снижение температуры оказывает различное воздействие на ЛС. Так, ампулированные растворы, содержащие 0,1% адреналина гидрохлорида, 25-40% глюкозы, 25% магния сульфата, 10% кальция хлорида, 5% эфедрина гидрохлорида, сохраняют свои качества при понижении температуры даже до -43°С. В то же время бактерийные и некоторые другие ЛС разлагаются при температуре ниже 0°С, а растворы некоторых антибиотиков (канамицина сульфата, эритромицина и др.) разрушаются в течение нескольких дней при температуре от б до 20°С. Свет также по-разному влияет на ЛВ. Обычно воздействие света ускоряет разложение. Сухие кристаллические вещества более устойчивы к свету, чем растворы. Гигроскопичные вещества после растворения в кристаллизационной воде повышают светочувствительность. Воздействие света усиливается в присутствии катализаторов, которые активизируют химические процессы. Фотокаталитические процессы происходят в кристаллических веществах только в поверхностном слое. При хранении на свету некоторых ЛС, особенно относящихся к фенолам, аминам, сульфаниламидам, происходит изменение окраски, формы кристаллов. Другие на свету сохраняются лучше, чем в темноте. ЛС, содержащие соли железа (И), стабильны и повышают устойчивость к свету других ЛВ...
1 Физические процессы 1.1 Температура К физико-химическим процессам, происходящие при неправильном хранении лекарственных средств и лекарственных форм, относятся: поглощение и потеря воды; изменение фазового состояния, например плавление, испарение или сублимация, расслаивание, укрупнение частиц дисперсной фазы и др. Так, при хранении легколетучих веществ (раствор аммиака, бромкамфора, йод, йодоформ, эфирные масла) может изменяться содержание лекарственных веществ в лекарственной форме. Из физических факторов наибольшее влияние на стабильность лекарств оказывают температура, свет и влажность. Особенно велика роль температурного режима на стабильность лекарственных веществ. Известно, что с повышением температуры резко возрастает скорость химических реакций. Даже если принять температурный коэффициент равным 2, то скорость реакции при нагревании реагирующих веществ от 20 до 100°С возрастает в 256 раз. Из этого вытекает необходимость установления оптимальных температурных условий для тех или иных лекарственных препаратов. Вместе с тем зависимость между температурой и скоростью химической реакции лежит в основе методов ускоренного хранения лекарств, используемых для изучения их стабильности. Снижение температуры оказывает различное воздействие на лекарственные вещества. Так, ампулированные растворы, содержащие 0,1% адреналина гидрохлорида, 25 - 40% глюкозы, 25% магния сульфата, 10% кальция хлорида, 5% эфедрина гидрохлорида, 2% новокаина, сохраняют свои качества при понижении температуры даже до -43°С. В то же время бактерийные и некоторые другие препараты разлагаются при температуре ниже 0°, а растворы некоторых антибиотиков (колимицина сульфата, эритромицина и др.) разрушаются в течение нескольких дней при температуре от 6 до 20°С.
1.2 Свет Свет также по-разному влияет на лекарственные вещества. Обычно воздействие света ускоряет разложение. Сухие кристаллические вещества более устойчивы к свету, чем растворы. Гигроскопичные вещества после плавления в кристаллизационной воде повышают светочувствительность. Воздействие света усиливается в присутствии катализаторов, которые активизируют химические процессы. Фотокаталитические процессы происходят в кристаллических веществах только в поверхностном слое. При хранении на свету некоторых средств, особенно относящихся к фенолам, аминам, сульфаниламидам, происходит изменение окраски, формы кристаллов. Другие же кристаллы на свету сохраняются лучше, чем в темноте (10% спиртовой раствор йода). Препараты, содержащие соли железа (II), стабильны и повышают устойчивость к свету других лекарственных веществ. 1.3 Влажность Влажность воздуха - один из факторов, активно снижающих стабильность лекарств. Пониженная влажность воздуха, обычно сопровождающаяся повышением температуры, уменьшает содержание кристаллизационной воды в лекарственных веществах. Это приводит к повышению концентрации препаратов, а также к изменениям физических свойств (формы кристаллов, растворимости и т.д.). Повышенная влажность воздуха влияет на физические свойства гигроскопичных лекарственных веществ, ускоряет такие химические процессы, как гидролиз. В результате могут измениться внешний вид, окраска, концентрация лекарственного вещества. Вследствие этих процессов образуются продукты разложения и снижается фармакологическая активность. 2. Химические процессы Химические процессы, происходящие при хранении лекарств, сложны и многообразны. Они протекают в виде реакций гидролиза окисления-восстановления, рацемизации, образования высокомолекулярных соединений и тесно связаны с влиянием физических факторов (температуры, света, влажности). Знание механизма и скорости протекания этих процессов дает возможность устранять или замедлять ход химических реакций, а следовательно, повышать стабильность лекарств. Гидролиз, реакции окисления-восстановления, декарбоксилирования, фотохимическая деструкция, изомеризация - таков далеко не полный перечень химических процессов, которые могут происходить при хранении лекарственных веществ.
2.1 Гидролиз Гидролиз - это химический процесс, наиболее часто происходящий при хранении лекарственных веществ, производных сложных эфиров, амидов, лактонов, лактамов, имидов, уретанов, уреидов и других классов химических соединений. Некоторые лекарственные вещества гидролизуются даже в кристаллическом виде, особенно при повышенной температуре и влажности воздуха. Значительно активизируется процесс гидролиза в присутствии следов солей металлов (меди, цинка, железа и др.). Наиболее существенное влияние на скорость гидролиза лекарственных веществ в растворах оказывают растворители и рН среды. Обычно растворителем служит вода, для приготовления растворов лекарственных веществ практически нерастворимых в воде используют растительные масла. Растворителями могут также быть пропиленгликоль, диметилсульфоксид, полиэтиленоксид-400, этилолеат, бензилбензоат. Константа скорости гидролиза при использовании этих растворителей, например пропиленгликоля в сочетании с водой, заметно снижается. Ингибируют процесс гликолиза, действуя растворами соляной кислоты, буферными растворами или растворами щелочей. Выбор стабилизатора зависит от химических свойств лекарственного вещества. Константа скорости гидролиза зависит от рН раствора. Можно установить интервал значений рН среды, при котором константа скорости реакции имеет минимальную величину. Константа скорости зависит также от ионной силы раствора, диэлектрической постоянной. Поэтому в качестве стабилизатора используют хлорид натрия и другие соли. Выбор оптимальных интервалов значений рН среды и других параметров, влияющих на константу скорости реакции, имеет очень большое значение для увеличения срока годности многих растворов лекарственных веществ, особенно применяемых для инъекций. В лекарственных формах роль катализаторов могут выполнять как ионы водорода, так и гидроксид-ионы, т.е. рН среды оказывает не только стабилизирующее, но и каталитическое воздействие. Для каждого лекарства оптимальные условия хранения устанавливают экспериментально. На процесс гидролиза ингибирующее воздействие оказывает добавление поверхностно-активных веществ (ПАВ). Особенно эффективны анионактивное ПАВ - лаурилсульфат натрия и катионактивное ПАВ - цетилтриметиламмоний бромид. Они в 10-20 раз повышают гидролитическую устойчивость ряда сложных эфиров. Наиболее часто встречающимся, типом гидролиза является гидролиз солей. Гидролиз солей, образованных слабым основанием и сильной кислотой, происходит, например, в растворах солей алкалоидов и синтетических азотистых оснований. Нагревание раствора во время стерилизации и разведение увеличивают степень гидролиза. Усиление гидролиза происходит при подщелачивании раствора силикатами щелочных металлов, входящих в состав стекла. Это возможно в растворах соей стрихнина, папаверина и других веществ даже при незначительном повышении рН. При значительном увеличении рН раствора наблюдается образование сравнительно сильных свободных оснований, например, прокаина. Если основание хорошо растворимо в воде (например, основание эфедрина), то осадок не выпадает. Иногда свободное основание алкалоида не образует осадка вследствие взаимодействия со щелочью. Например, в случае морфина, апоморфина, адреналина образуются растворимые в щелочной среде феноляты. Гидролиз солей, образованных слабым основанием и сильной кислотой, протекает практически до конца. Органические соединения, имеющие сложноэфирные, амидные, лактонные, гликозидные и некоторые другие связи, легко подвергаются гидролизу в водных растворах с образованием двух и более веществ. Аналогично сложным эфирам гидролизуются амиды кислот, например, никотинамид. Однако в этом случае гидролиз протекает очень медленно и возможен только при нагревании с раствором гидроксида натрия. Гидролизу подвергаются также полисахариды и сердечные гликозиды. При стабилизации различных органических веществ рекомендуется использовать различные стабилизаторы. Изменение рН среды не является единственным способом стабилизации лекарственных веществ в растворах. В последнее время используются ПАВ (мицеллообразование), ВМС (образование более стойких комплексных соединений) и др. 2.2 Окисление Окисление - процесс, являющийся одной из причин разложения лекарственных веществ. Некоторые из них (производные фенолов) окисляются, находясь в кристаллическом состоянии, процесс окисления заметно активизируется при растворении. Особенно легко окисляются лекарственные вещества, проявляющие активные восстановительные свойства (альдегиды, гидрозиды, производные фенотиазина и др.). Признаки окисления - изменение окраски лекарственного вещества или его раствора, появление ополисценции. Лекарственные средства, разрушающиеся под влиянием света и кислорода, становятся непригодными к применению, а в некоторых случаях опасными для здоровья. Например, обнаружено, что введение в организм адренохрома (окисленного адреналина) может быть причиной появления галлюцинаций. Поэтому раствор адреналина гидрохлорида после вскрытия флакона нужно использовать как можно быстрее. Известно также, что продукты окисления резорцина обладают рвотным действием, а хлороформ под действием кислорода воздуха на свету легко образует токсические продукты (фосген, хлор, хлористый водород). Процесс окисления заметно активизируется при повышенной температуре и влажности, ультрафиолетовом облучении. Процесс окисления катализируют различные примеси. Очень часто процесс окисления предшествует процесс гидролиза (сульфацил-натрия) или, наоборот, гидролитическое расщепление следует за окислительным процессом (аскорбиновая кислота). Лекарственные средства могут взаимодействовать также с углекислым газом воздуха: например, оксид магния превращается в карбонат магния основной. В реакцию с СО2 вступают соли щелочных металлов и слабых органических кислот (натриевые соли сульфаниламидов, производные барбитуровой кислоты), неорганические препараты меди, цинка, железа. Под воздействием света, температуры и при изменении рН среды возможно превращение оптически активного ЛВ в его оптический изомер (реакции рацемизации). Образующиеся оптические изомеры могут обладать сниженным фармакологическим эффектом, не обладать таковым или проявлять токсичность. 2.3 Процессы изомеризации При хранении лекарственных препаратов могут происходить процессы изомеризации. Реакции рацемизации (образования рацематов) является причиной значительного снижения фармакологического действия лекарственных препаратов, обладающих оптической активностью. Оптические изомеры отличаются друг от друга по фармакологической активности иногда в несколько раз. В растворе адреналина постепенно происходит процесс рацемизации -- образования смеси обоих изомеров. Этот процесс сопровождается заметным снижением активности препарата. 3. Биологические процессы Биологические процессы вызывают изменения в лекарствах под влиянием жизнедеятельности микроорганизмов, что приводит к снижению стабильности лекарственных средств и инфицированию человека-Лекарства чаше всего загрязняются сапрофитами, широко распространенными в окружающей среде. Сапрофиты способны разлагать органические вещества: белки, липиды, углеводы. Дрожжевые и нитчатые грибы разрушают алкалоиды, антипирин, гликозиды, глюкозу, различные витамины. Срок годности лекарственных средств может резко снижаться из-за низкого качества упаковки; Например, при хранении растворов для инъекций во флаконах или ампулах из некачественного стекла происходит переход силиката натрия и калия из стекла в раствор. Это приводит к увеличению значения рН среды и образованию так называемых «блесток» (частичек разрушенного стекла). При повышении рН соли алкалоидов и синтетических азотсодержащих оснований разлагаются со снижением или потерей лечебного действия и образованием токсических продуктов. Щелочные растворы катализируют процессы окисления аскорбиновой кислоты, аминазина, эрготала, ПАСКа, викасола, витаминов, антибиотиков, гликозидов. Кроме того, щелочность стекла также способствует развитию микрофлоры. 4. Влияние условий получения и хранения на стабильность лекарственных веществ Физические факторы и химические процессы могут оказывать влияние на стабильность лекарственных веществ, начиная с момента их получения и до приема больным. Стабильность лекарственных веществ во многом зависит от соблюдения условий технологического процесса. При этом важная роль принадлежит степени чистоты исходных продуктов синтеза, растворителей, техническому состоянию аппаратуры, соблюдению требований регламента производства по очистке промежуточных продуктов синтеза, а также качеству исходных веществ, используемых для получения лекарственных форм. Эти факторы могут вызвать побочные химические реакции, привести к образованию веществ, нарушающих нужную степень чистоты и стабильность конечного продукта. Очень важно, чтобы полученное лекарственное вещество строго соответствовало требованиям НТД по всем параметрам. Стабильность зависит не только от химических, но и от физических свойств лекарственного вещества. Например, в зависимости от условий кристаллизации могут изменяться размер кристаллов, поверхностна) энергия, степень роста кристаллов, оформление их граней и т. д. Физические свойства кристаллов, в свою очередь, оказывают влияние на гигроскопичность, химическую активность, а, следовательно, и на стабильность лекарственного препарата. Форма и размер кристаллов находятся в зависимости от природы, степени чистоты растворителя, температурных условии и продолжительности процесса кристаллизация, наличия сопутствующих веществ. Эти факторы (особенно природа растворителя) влияют, например, на процесс образования полиморфных форм лекарственных веществ. Известно, что полиморфные формы отличаются по своей стабильности. При хранении может происходить процесс превращения одной полиморфной формы в другую, более стабильную. В то же время нестабильные полиморфные формы (в частности сульфаниламидов, барбитуратов, стероидных гормонов) отличаются более высокой как химической, так и фармакологической активностью. Это вызывает необходимость разработки методов стабилизации более активных полиморфных форм. Для некоторых групп лекарственных препаратов, в частности биологически активных веществ (гормоны, витамины, гликозиды, антибиотики), оказалось невозможным повысить стабильность. Малые дозы, в которых применяют эти препараты, в сочетании с непродолжительным сроком годности создают определенные трудности как в их производстве, так и в хранении и применении. Выход из положения был найден в том, что в процессе производства в лекарственные формы вносят избыток этих препаратов до ПО--120%. При хранении в течение определенного срока происходит снижение фармакологической активности, обусловленное уменьшением концентрации препарата до 80--90%. Эта технологическая операция носит название избыток для производственных целей. Она привела к необходимости допускать в фармакопеях пределы содержания таких препаратов в лекарственных формах от 90 до 110% и даже от 80 до 120% для некоторых антибиотиков и гормонов. Учитывая влияние физических и химических факторов на стабильность лекарственных веществ, можно сделать вывод, что важная роль принадлежит условиям хранения. В ГФ СССР эти условия оговорены в виде общих указаний. Обычно они отражают влияние какого-то определенного фактора или группы факторов. Для некоторых лекарственных веществ в ГФ СССР указан температурный режим хранения. Так, антибиотики тетрациклинового ряда, а также канамицина моносульфат, оксациллина натриевую соль, феноксиметилпенициллин, стрептомицина сульфат хранят при комнатной температуре, а новобиоцина натриевую соль, никодин -- не выше 20°С, тиофосфамид -- не выше 10°С. В ГФ X оговариваются особые требования к хранению некоторых гормонов, витаминов, биопрепаратов. Так, суспензию цинк-инсулина необходимо хранить во флаконах нейтрального стекла, укупоренных резиновыми пробками с металлической обкаткой, при температуре от +1 до +10°С. Не допускается замораживание препаратов инсулина. Условия хранения лекарственных средств регламентируются «Инструкцией по организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения», утвержденной приказом МЗ СССР № 520 от 15 мая 1981 г. В соответствии с этой инструкцией все лекарственные средства в зависимости от физических и физико-химических свойств, а также от воздействия на них различных факторов внешней среды подразделяют на требующие защиты от света, воздействия влаги, улетучивания, повышенной и пониженной температуры, от газов, содержащихся в окружающей среде. Установлены также условия хранения пахучих, красящих и дезинфицирующих средств. По каждой из этих групп приведен перечень лекарственных средств, требующих соответствующих условий хранения. Защиты от воздействия света требуют нитраты, нитриты, соли оксогалогенсодержащих кислот и другие производные галогенов, нитро- и нитрозосоединения, фенолы, амиды и аминосоединения, производные фенотиазина. кортикостероиды, витамины, антибиотики, эфирные и жирные масла, а также галеновые и органопрепараты. Под воздействием света эти препараты окисляются с образованием различных веществ, отличающихся по фармакологической активности, полностью теряющих ее или даже имеющих токсическое действие на организм. В зависимости от чувствительности к окислителям данную группу лекарственных веществ следует хранить в стеклянной таре оранжевого стекла либо в металлической таре, либо в упаковке из алюминиевой фольги или полимерных материалов, окрашенных в темный цвет. 13. Типы реакций, наиболее часто приводящих к изменению лекарственных средств под влиянием факторов окружающей среды. Привести примеры не менее 5 реакций. Гидролиз — реакция ионного обмена между различными веществами и водой. Значительно активизируется процесс гидролиза в присутствии следов солей металлов (меди, цинка, железа и др.).Наиболее существенное влияние на скорость гидролиза ЛВ в растворах оказывают растворители и рН среды. Ингибируют процесс гидролиза, действуя растворами хлороводородной кислоты, буферными растворами или растворами щелочей. Выбор стабилизатора зависит от химических свойств ЛВ. Константа скорости гидролиза зависит от рН раствора. На процесс гидролиза ЛВ ингибирующее воздействие оказывает добавление поверхностно-активных веществ (ПАВ). Особенно эффективны анионактивное ПАВ — лаурилсульфат натрия, катионактивное ПАВ — цетилтриметимаммоний бромид. Они в 10-20раз повышают гидролитическую устойчивость ряда сложных эфиров. Гидролизу подвергаются соли в составе которых имеется так называемый «слабый ион», т.е. эти вещества должны быть образованы слабым основанием и сильной кислотой (гидролиз протекает по катиону), сильным основанием и слабой кислотой (гидролиз протекает по аниону) или же слабым основанием и слабой кислотой (гидролиз по катиону и аниону). Соли, образованные сильной кислотой и сильным основанием не гидролизуются (NaCl, KNO3, BaSO4, Ca(ClO4)2 и т.д.). Существует несколько вариантов записи уравнений реакции гидролиза солей. В первом случае первоначально указывают продукты диссоциации соли и воды, после чего – полное и сокращенное ионное уравнения гидролиза и, наконец, его же, но в молекулярном виде. Рассмотрим на примере гидролиза сульфита натрия (Na2SO3) – двухосновной соли, образованной слабой кислотой – сернистой (H2SO3) и сильным основанием – гидроксидом натрия (NaOH): Na2SO3 ↔ SO32- + 2Na+ (диссоциация соли); SO32- + 2Na++ H2O ↔ HSO3—+ OH— + 2Na+ (полное ионное уравнение); SO32- + H2O ↔ HSO3—+ OH— (сокращенное ионное уравнение); Na2SO3 + H2O ↔ NaHSO3+ NaOH (молекулярное уравнение). Теоретически возможна вторая ступень гидролиза: NaHSO3↔Na+ + HSO3—(диссоциация соли); Na+ + HSO3— + H2O ↔H2SO3 + OH— + Na+ (полное ионное уравнение); HSO3— + H2O ↔ H2SO3 + OH—(сокращенное ионное уравнение); NaHSO3+ H2O↔H2SO3 +NaOH (молекулярное уравнение). Присутствие гидроксид-ионов свидетельствует о том, что реакция среды водного раствора сульфита натрия будет щелочной, а окраска индикатора лакмуса – синей. Окисление — это встречно-параллельные химические реакции, протекающие с изменением степеней окисления атомов, входящих в состав реагирующих веществ, реализующихся путём перераспределения электронов между атомом-окислителем и атомом-восстановителем. Некоторые из них (производные фенолов) окисляются, находясь в кристаллическом состоянии. Процесс окисления заметно активизируется при растворении. Особенно легко окисляются ЛВ, проявляющие активные восстановительные свойства (альдегиды, гидразиды, производные фенотиазина и др.). Признаки окисления — изменение окраски ЛВ или его раствора, появление опалесценции. Процесс окисления заметно активизируется при повышенной температуре и влажности, ультрафиолетовом облучении. Процесс окисления катализируют различные примеси. Особенно велика роль даже небольших количеств примесей тяжелых металлов, в частности железа (III), меди (II), свинца, никеля и др. Очень часто процессу окисления предшествует процесс гидролиза (сульфацил-натрия) или, наоборот, гидролитическое расщепление следует за окислительным процессом (аскорбиновая кислота). Альдегиды окисляются до карбоновых кислот при действии многих окислителей: азотной кислоты, соединений хрома (VI), щелочного раствора йода, перекиси водорода, оксида серебра, перманаганата калия, гидроксида меди. В общем случае, фенолы не устойчивы к окислению и в зависимости от природы окислителя и условий реакции дают различные соединения. Так, при действии CrO3 или хромовой смеси они превращаются в п-бензохиноны с образованием промежуточного гидрохинона: Рисунок 1. Именно появлением хиноидного строения (хромофорной системы связей) обусловлена окраска фенолов в процессе спонтанного окисления при хранении. Действием пероксида водорода в присутствии железа (вместо соединений хрома) получают пирокатехин: При хранении ЛВ могут происходить процессы изомеризации. Реакции рацемизации (образования рацематов) являются причиной значительного снижения фармакологического действия ЛВ, обладающих оптической активностью. Оптические изомеры отличаются друг от друга по фармакологической активности иногда в несколько раз. Например, левовращающий оптический изомер адреналина в 15-20 раз активнее правовращающего. Поэтому в медицинской практике применяют L-изомер. В растворе адреналина постепенно происходит процесс рацемизации — образования смеси обоих изомеров. Этот процесс сопровождается заметным снижением активности ЛВ. Адреналин биологически высокоактивен (левовращающий изомер в 12—15 раз активнее правовращающего).
|
|||||||||
|
Последнее изменение этой страницы: 2021-01-14; просмотров: 432; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.54.6 (0.073 с.) |