
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
С трудом выпускники определяют тип строения веществ.Стр 1 из 4Следующая ⇒
Часть А В тестах ЕГЭ задания А1 –А5 проверяют знание ПЗ в свете учения о строении атома и строение вещества. Наибольшее число ошибок было совершено при установлении принадлежности d -элементов к побочной подгруппе ПС по их электронной конфигурации. С трудом выпускники определяют тип строения веществ. А5(21%) Атомную кристаллическую решетку имеет 1) Н2 2) SiO2 3) KBr 4) He Молекулярную кристаллическую решетку имеет Йодид цезия 2) графит 3) сера 4) красный фосфор Задания А6 – А13 проверяют знания классификации веществ. Наибольшее число ошибок связано с определением амфотерных оксидов и гидроксидов и их свойств: А10 (55%) Оксид калия взаимодействует c Оксидом кальция Оксидом азота(II) Оксидом цинка Оксидом лития Выпускники забывают, что амфотерные оксиды и гидроксиды цинка, бериллия, алюминия, хрома(III) взаимодействуют как с кислотами, так и со щелочами, либо с кислотными и основными оксидами. Как и в прошлые годы к наиболее сложным для испытуемых вопросам относятся вопросы, посвященные кислородосодержащим органическим веществам: А16 (47%) Верны ли следующие суждения о свойствах спиртов? А. С ростом молекулярной массы усиливаются водородные связи между молекулами спиртов. Б. Атом водорода гидроксильной группы способен замещаться щелочным металлом. Верно только А Верно только Б Верны оба суждения Оба суждения неверны А17 (34%) Твердый жир из жидкого получают реакцией Гидратации Дегидратации Гидрирования Дегидрирования А18 (48%) В схеме превращений ацетальдегид => X => этилат натрия Веществом «X» является Этилен Ацетат натрия Уксусная кислота Этанол А27 (53%) Уксусная кислота не взаимодействует с Карбонатом кальция Аммиаком Этанолом Гидросульфатом натрия Трудными оказались и вопросы, связанные с практическим применением веществ и химических реакций: · Правила работы в лаборатории. Методы исследования объектов, изучаемых в химии. Индикаторы. Качественные реакции (А2 8, 62,4%). · Общие научные принципы химического производства (А29, 58,4%). А28 (32%) Верны ли следующие суждения о правилах обращения с веществами?
А. Перманганат калия нельзя смешивать с горючими и легкоокисляющимися веществами. Б. С солями меди следует обращаться осторожно ввиду их ядовитости. Верно только А Верно только Б Верны оба суждения Оба суждения неверны А29 (37%) Для получения железа алюмотермическим способом используют каждое из двух веществ: 1) FeO, А l2O3 2) Fe3O4, Al 3) Fe2O3, А l2O3 FeS, Al Низкие результаты школьников по отдельным вопросам части А могут быть связаны иногда с их более сложной структурой. Так представляют повышенную трудность для школьников вопросы, содержащие отрицание, вопросы на оценку справедливости двух суждений. При подготовке у ЕГЭ по химии в очередном учебном году следует обратить внимание на эти типы вопросов. Часть В. Примеры наиболее сложных заданий части В: Как и в части А наибольшую сложность в этой части представили вопросы по органической химии. Особенно заметно отставание по заданиям В6 «Реакции, характеризующие основные свойства и способы получения углеводородов», который и оказался самым сложным для участников экзамена (37,8%). В6 (21%) Реакция бромирования пропана протекает По ионному механизму В несколько стадий 3) с образованием как 1-бромпропана, так и 2-бромпропана В соответствии с правилом В.В. Марковникова В присутствии катализатора 6) с преимущественным образованием 2-бромпропана Немногим лучше были выполнены задания В7 (39,1%), посвященные свойствам кислородсодержащих органических соединений: В7 (24%) Для альдегидов характерны реакции Гидролиза Присоединения по карбонильной группе Окисления по связи С-Н Этерификации Замещения в углеводородном радикале Дегидратации Существенно хуже по сравнению с прошлым годом были выполнены и задания В8 (35,3%) – «Азотсодержащие соединения. Амины. Аминокислоты» B8 (27%) Щелочную среду имеют водные растворы: 1) C 6 H 5 - NH 2 2) C 3 H 7 - NH 2 3) CH3-NH-CH3 4) C6H5-NH-C6H5 5) CH2(NH2)-COOH 6) CH2(NH2)-COONa В неорганической химии сложными оказались задания В5, связанные с определением возможности веществ взаимодействовать друг с другом:
В5 (22%) Установите соответствие между названием вещества и реагентами, с которыми оно может вступать во взаимодействие.
Подобные задания часто удобнее решать от противного – с какими веществами реакция невозможна. Если есть хоть одно такое вещество – вариант можно отбросить. Тема «Заряды ионов. Степень окисления. Реакции окислительно-восстановительные. Коррозия металлов» в целом выглядела неплохо, но вот это задание оказалось трудным: В2 (37%) Установите соответствие между реагирующими веществами и азотсодержащим продуктом реакции.
Часть C. С заданиями С-1 школьники справились успешнее всего, хотя и несколько хуже, чем в прошлом году. Принципиальных отличий в заданиях не было. Наиболее сложным уравнением в вариантах первой волны экзамена явилось следующие задания: С1 (55%). Используя метод электронного баланса, составьте уравнение реакции: FeSO 4 + KMnO 4 +…→…+ K 2 SO 4 + K 2 MnO 4 Кислотно-основные реакции. Есть ли в наборе явные кислоты, кислотные оксиды, кислые соли с одной стороны и основания, основные оксиды, основные соли с другой? Если да, запишите уравнения реакций между ними. Другие замечания по заданию С2: школьники не видят возможность взаимодействия амфотерных оксидов и щелочей, не видят окислительные свойства нитрат-иона, восстановительные иодид-иона, путают продукты реакций с азотной кислотой, допускают ошибки в определении коэффициентов, особенно в уравнениях реакций с перманганатом, дихроматом, хлоратом калия. Задания С-3 (цепочка превращений органических веществ) были выполнены практически на уровне прошлого года (–1,7%). Большинство уравнений реакций, включенные в эти цепочки, отвечали базовому курсу органической химии, наиболее типичным свойствам органических веществ. К новым типам реакций, которые встретились в этом году, можно отнести реакции циклизации и разрушения циклов. Примером наиболее сложной цепочки может служить задание: С3 (26%) Приведите уравнения реакций, с помощью которых можно осуществить следующие превращения 1,3-дибромбутан Здесь надо было учесть образование циклопропанового цикла на первой стадии, его разрыва на второй, затем образование ароматического кольца на четвертой стадии. Элементы правильного ответа: 1. CH 2 Br - CH 2 - CHBr - CH 3 + Zn ® 2. 3. 2CH3-CHBr-CH2CH3 + 2Na ® 2CH3CH2-CH(CH3)-CH(CH3)-CH2CH3 +2NaBr 4. CH3CH2-CH(CH3)-CH(CH3)-CH2CH3 5. 5 Решение: 1. Стехиометрическая схема реакции горения амина: 2 RNH 2 → N 2 Определяем количество вещества амина и его молярную массу: n(RNH2)=2n(N2)=2,24/22,4*2=0,05 моль М(RNH 2)=9/0,05=45г/моль 2. Находим молярную массу радикала: М(R)+14+2=45 М(R)=29 г/моль Формула амина С2Н5 NH2 Замечания по С5: не всегда правильно представляют алгоритм решения, забывают о молекулярном строении простых веществ (N 2), теряют водород уходящий в галогенводород при сжигании галогенсодержащих веществ, грубое округление. О росте подготовленности участников ЕГЭ-2009 свидетельствует и то, что подавляющее число их приступает к выполнению части С (96%). Конечно, среди этих работ есть и очень слабые, получившие нулевую оценку или 1-2 балла. Тем не менее, это говорит о более серьезном отношении выпускников к экзамену.
Часть А В тестах ЕГЭ задания А1 –А5 проверяют знание ПЗ в свете учения о строении атома и строение вещества. Наибольшее число ошибок было совершено при установлении принадлежности d -элементов к побочной подгруппе ПС по их электронной конфигурации. С трудом выпускники определяют тип строения веществ. А5(21%) Атомную кристаллическую решетку имеет 1) Н2 2) SiO2 3) KBr 4) He
|
|||||||||||||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 79; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.238.20 (0.014 с.) |
 X 1 ® 2-бромбутан
X 1 ® 2-бромбутан 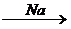 X 2 ®
X 2 ® 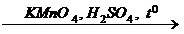 X 3
X 3 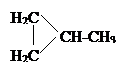 + ZnBr 2;
+ ZnBr 2;
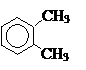 + 4H2;
+ 4H2;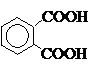 + 12MnSO4 + 6K2SO4 +28H2O;
+ 12MnSO4 + 6K2SO4 +28H2O;


