Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
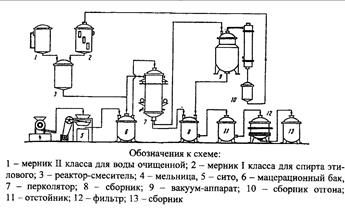
Технологическая схема (для перколяции)
Количественное определение спирта в соответствии с ГФ: 1. по температуре кипения – в готовом препарате. 2. по плотности (ареометр, денсиметр) – в готовом препарате, рекуперате, экстрагенте. 3. спиртомером (концентрация) - в готовом препарате, рекуперате, экстрагенте. 4. методом дистилляции – в готовом препарате. Настойка эвкалипта готовится на 70% спирте в соотношении 1:5 методом перколяции или ускоренной дробной мацерации. Преимущества использования клеточных культур заключаются в следующем: § Решается проблема дефицита исходного сырья, особенно ценных исчезающих видов растений, не поддающихся плантационному культивированию; § Возможно получение фитомассы, полностью свободной от гербицидов, пестицидов, тяжелых металлов и др.; § Имеется возможность получения новых веществ, не синтезируемых соответствующим целевым растением; § Возможно управление биосинтезом целевых продуктов за счет условий культивирования, состава питательной среды и другими способами; § Имеется возможность индустриализации и удешевления производства некоторых БАВ, синтез которых пока не разработан или очень дорог. Ситуационная задача № 41 1. В РПО аптеки поступил рецепт: Rp.: Amyli Zinci oxydi Talci ana 15,0 Aquae purificatae 250 ml Glycerini 50,0 Spiritus aethylici 50 ml Misce. Da. Signa. Втирать в кожу стоп. Каковы профессиональные действия провизора при осуществлении фармацевтической экспертизы поступившего рецепта? Объясните, возможен ли отпуск лекарственной формы по рецепту из ветеринарной поликлиники? Каковы особенности хранения спирта этилового в аптеке? В каких единицах ведет предметно-количественный учет спирта этилового? Каковы профессиональные действия материально-ответственного лица в конце календарного месяца и после инвентаризации при осуществлении предметно-количественного учета одного из ингредиентов прописи? ОТВЕТ. При поступлении рецепта в аптеку провизор проводит фармацевтическую экспертизу рецепта в соответствии с приказом МЗ и ср РФ от 12 февраля 2007г. № 110. -Форма рецептурного бланка;
-соответствующее оформление (дата, взрослый или детский, ф.и.о. больного, возраст, адрес, ф.и.о.врача, наименование лек. ср-ва на латинском языке, подпись и печать врача, годность рецепта, дополнительные печати) -проверка доз; -таксировка. Отпуск данной прописи по рецепту из ветеринарной клиники не возможен, т.к. в соответствии с приказом МЗиСР РФ от 12 февраля 2007г. 110№ «О порядке назначения и выписывания ЛС, ИМН и продуктов лечебного питания» назначение лекарственных средств при амбулаторно-поликлиническом и стационарном лечении в ЛПУ независимо от организационно-правовой формы производится врачом, непосредственно осуществляющем ведение больного, в том числе частнопрактикующим, имеющим лицензию на медицинскую деятельность, выданную в установленном порядке. При оказании скорой и неотложной медицинской помощи лекарственные средства назначаются врачом выездной бригады скорой помощи или врачом отделения неотложной помощи (помощи на дому) амбулаторно-поликлинического учреждения. В ряде случаев лекарственные средства могут быть назначены специалистом со средним медицинским образованием (зубным врачом, фельдшером, акушеркой) в соответствии со статьей 54 Основ законодательства Российской Федерации об охране здоровья граждан (Ведомости Совета народных депутатов и Верховного Совета Российской Федерации). В соответствии с приказом МЗ РФ от12.11.1997г. №330 «О мерах по улучшению учета, хранения, выписывания и использования наркотических средств и психотропных веществ» наркотические средства и психотропные вещества подлежат предметно-количественному учету в специальном журнале регистрации операций, связанных с оборотом наркотических средств и психотропных веществ, пронумерованном, сброшюрованном и заверенном подписью руководителя аптеки и скрепленном печатью аптеки. Не реже одного раза в месяц уполномоченное лицо, на которое возложен контроль за ведением и хранением журнала регистрации, проверяет записи в журнале, сверяет фактическое наличие наркотических средств и психотропных веществ с их книжными остатками, о чем на следующей строке после последней на момент проверки записи в журнале регистрации делает отметку с указанием даты проверки и заверяет ее своей подписью.
В соответствии с приказом МЗ РФ от 14.12.2005г. №785 «О порядке отпуска лекарственных средств», при изготовлении экстемпоральных лекарственных препаратов, содержащих лекарственные средства, подлежащие предметно-количественному учету, в соответствии с рецептами, выписанными врачом, провизор аптечного учреждения (организации) расписывается на рецепте о выдаче, а фармацевт аптечного учреждения (организации) - в получении требуемого количества лекарственных средств. Инвентаризация товарно-материальных ценностей, основных средств, денежных средств проводится в соответствии с приказом МЗ СССР от 17 февраля 1986г. №229. При инвентаризации товарно-материальных ценностей аптеки (отдела аптеки) устанавливаются фактические остатки наркотических средств и психотропных веществ, на что составляется отдельная инвентаризационная опись. В случаях выявления недостачи применяются нормы естественной убыли. (Приказ МЗ РФ от 20.07.2001г.№ 284). Нормы естественной убыли установлены при изготовлении лекарственных средств по рецептам врачей и требованиям ЛПУ. Лекарственные средства, подлежащие предметно-количественному учету (наркотические ср-ва, психотропные в-ва и их прекурсоры, лек. ср-ва списков ПККН, др. лек. ср-ва подлежащие ПКУ): - по индивидуальному изготовлению по рецептам и требованиям ЛПУ 0,95; - отвешивание и отмеривание их в аптечную тару без дополнительных технологических операций 0,4; Этиловый спирт: - индивидуальное изготовление лекарственных средств 1,9; -отвешивание спирта в аптечную тару 0,65. В случае выявления отклонений при снятии фактических остатков от книжных данных руководитель аптеки обязан немедленно поставить об этом письменно в известность орган управления здравоохранением или фармацевтической деятельностью субъекта Российской Федерации, который в 3-х-5-ти дневный срок должен провести служебное расследование.
2. Дайте определение и дисперсологическую характеристику изготовленной лекарственной формы. • Какой закон лежит в основе теоретического обоснования технологии? Назовите метод изготовления. • По каким технологическим показателям и как оценивают качество лекарственной формы? • В состав препарата входят глицерин и спирт этиловый: приведите классификацию неводных растворителей. Укажите особенности промышленного производства растворов на неводных растворителях. • Предложите и охарактеризуйте типы мешалок, используемых в данном производстве. ОТВЕТ. Суспензия - жидкая лекарственная форма, представляющая собой дисперсную систему, в которой твердое вещество взвешено в жидкости. Суспензии состоят из дисперсионной среды (воды, растительных масел, глицерина и т.п.) и дисперсной фазы (частиц твердых лекарственных веществ, практически нерастворимых в данной жидкости). Суспензии готовят двумя способами: дисперсионным (дробного фракционирования) и конденсационным. Отличаются они тем, какие вещества составляют дисперсную фазу (гидрофильные или гидрофобные). Данная суспензия приготовлена методом взмучивания (дисперсионный), т.к. входящие в состав тальк, цинка оксид и крахмал являются гидрофильными ненабухающими.
Необходимость применения этого метода возникает на практике при назначении в составе жидкого лекарства лекарственного вещества, нерастворимого или малорастворимого в данной дисперсионной среде. Если лекарственное вещество гидрофильно и лишено способности к набуханию, т.е. не увеличивается в объеме при контакте с водой или водными растворами и не превращается в упругий студень, то наиболее целесообразным приемом получения достаточно тонкой суспензии является взмучивание. Грубые, недостаточно диспергированные зерна быстро выделяются в осадок, в то время как тонкие частицы на известное время остаются во взвешенном состоянии. Тонкую суспензию сливают с осадка в отпускную склянку, а осадок подвергают повторному растиранию. Подобные операции повторяют до получения достаточно устойчивой суспензии. По исследованиям Б. В. Дерягина, решающее влияние на результаты диспергирования суспендируемого вещества оказывает соотношение между твердой (Т) и жидкой (Ж) фазой в момент измельчения. Наивысшая степень дисперсности достигается при их оптимальном соотношении, называемом правилом Дерягина 0,4—0,6 мл жидкости на 1 г измельчаемой твердой фазы. При таком соотношении обеспечивается максимальное трение частиц друг о друга и об измельчающие поверхности ступки и пестика. В основе теоретического обоснования технологии лежит Закон Стокса указывает на возможность изменения факторов, повышающих устойчивость суспензий. Ими в первую очередь являются размер частиц дисперсной фазы и вязкость дисперсионной среды, которая обеспечивается введением в состав суспензий ВМС (слизей, эфиров целлюлозы, твинов и др.). Необходимое измельчение гидрофобных веществ достигается растиранием их в ступке с прибавлением небольшого количества смачивающей жидкости. Адсорбируясь на поверхности твердых частиц, жидкость понижает запас свободной поверхностной энергии и, таким образом, препятствует соединению мелких частиц, облегчает их дальнейшее диспергирование - смачивающая жидкость проникает в поверхностные микротрещины твердых частиц и оказывают расклинивающее действие (эффект Ребиндера). Чем выше энергия смачивания, тем сильнее выражен расклинивающий эффект и тем легче происходит процесс измельчения. Гидрофильные вещества (например, белая глина, магния окись, цинка окись и др.), легче измельчаются в присутствии воды. Лиофильные вещества, адсорбируя на своей поверхности частицы дисперсионной среды, образуют оболочку, которая препятствует слипанию твердых частиц и превращению их в быстро оседающие хлопья.
Контроль качества проводится в соответствии с требованиями ГФ. - Проверка документации: расчеты количества ЛВ, массы суспензии. - Проверка оформления (соответствие этикетки) и упаковки суспензии (соответствие её физико-химическим свойствам ЛВ, герметичность). Необходимая этикетка «Перед употреблением взбалтывать» и при необходимости «Хранить в прохладном месте». - Отклонения в массе. - Органолептический контроль (цвет, запах). - Однородность частиц дисперсной фазы. - Время седиментации - визуально определяют высоту отстоявшегося слоя в течении определенного времени. Чем выше высота отстоявшегося слоя, тем устойчивость больше. - Ресуспендируемость - способность частиц дисперсной фазы равномерно распределяться во всем объеме суспензии при взбалтывании. Получение суспензий на крупных фармацевтических предприятиях осуществляется разными способами: интенсивным механическим перемешиванием с помощью быстроходных мешалок и РПА; размолом твердой фазы в жидкой среде на коллоидных мельницах, ультразвуковым диспергированием с использованием магнитострикционных и электрострикционных излучателей. Твердое вещество предварительно измельчают до мелкодисперсного состояния на специальных машинах, готовят концентрированную суспензию перемешиванием в смесителях, затем многократно диспергируют на коллоидных мельницах или на ультразвуковых и других установках. Для «сухих» суспензий, представляющих собой смесь лекарственного и вспомогательных веществ, образующих взвесь после добавления воды (в аптеке или домашних условиях), каждый ингредиент измельчают отдельно и просеивают через тонкое сито. После смешивания ингредиентов во избежание расслоения смесь вновь просеивают. Полученную готовую продукцию подвергают анализу в соответствии с требованиями НТД, стандартизуют и фасуют. Для механического диспергирования применяют пропеллерные и турбинные мешалки закрытого и открытого типов. Растворители, входящие в состав неводных растворов подразделяются на группы: 1. летучие: этанол, диэтиловый эфир, хлороформ, 2. нелетучие: глицерин, минеральные масла, димексид, полиэтиленоксиды (ПЭО - 400), силикон.
3. Для обнаружения цинка оксида в данной прописи студент применил фармакопейные реакции на ион цинка, а для количественного определения - метод комплексонометрии. Обоснуйте выбор данных испытаний. • Предложите реакции, доказывающие наличие иона цинка. Почему необходима для их проведения разведенная кислота хлористоводородная? Напишите схемы реакций. • Объясните суть метода комплексонометрии и условия его проведения при анализе цинка оксида (растворитель, значение рН, индикатор). Напишите схемы реакций. • Предложите реакции, доказывающие наличие иона цинка. Почему необходима для их проведения разведенная кислота хлористоводородная? Напишите схемы реакций.
1) Наличие цинка устанавливают по образованию белого осадка сульфида цинка, нерастворимого в уксусной кислоте и легко растворимого в разведенной соляной кислоте. Поэтому реакцию нужно выполнять в нейтральной среде: ZnSO4 + Na2S = ZnS + Na2SO4 ZnS + HCl à ZnCl2 + H2S 2. Растворы солей цинка образуют белый гелеобразный осадок при взаимодействии с гексационоферратом (П) калия нерастворимый в HCl.: ZnSO4 + K4[Fe(CN)6] → K2Zn[Fe(CN)6] ↓ + K2SO4
• Объясните суть метода комплексонометрии и условия его проведения при анализе цинка оксида (растворитель, значение рН, индикатор). Напишите схемы реакций. Метод комплексонометрического титрования основан на реакции образования внутрикомплексных соединений ионов металлов со специальными комплексообразующими реактивами, называемыми комплексонами. Титрант: трилон Б, pH=9,5-10. Инд – кислотный хром черный Сущность определения заключается в том, что индикатор кислотный хромовый черный специальный в присутствии аммиачного буферного раствора образует с ионами комплексное соединение красно-фиолетовое: Кислотный хромовый черный специальный (смотреть окраску красную)
При титровании трилоном Б вначале связываются находящиеся в растворе ионы металлов:
Затем трилон Б связывает ион металла, содержащийся в менее прочном его комплексе с индикатором. Поэтому в эквивалентной точке раствор приобретает окраску свободного индикатора – синюю. Равновесие реакций комплексообразования зависит от рН раствора, поэтому для обеспечения полноты протекания аналитической реакции необходимо поддерживать постоянное и определенное значение рН раствора. Требования к индикаторам. 1.Комплекс индикатора с ионом металла должен быть достаточно устойчивым Кдисс. Больше 10-4. 2.Индикатор должен образовывать с ионами металлов комплекс в 10 раз менее стойкий, чем с трилоном Б. 3.Концентрация индикатора в растворе должна быть достаточно малой (индикатор должен связывать менее 0,01 ионов металлов). 4.Изменение окраски должно быть четким, контрастным и быстрым 4. Вам необходимо спланировать заготовку лекарственного растительного сырья «Корневища змеевика». • Дайте оценку сырьевой базы змеевика, отметьте особенности местообитания растения и заготовки корневищ змеевика. Обоснуйте режим сушки и хранения сырья. • Какие методы фармакогностического анализа необходимо использовать для подтверждения подлинности и качества корневищ змеевика? По каким признакам вы можете забраковать корневища змеевика при внешнем осмотре? • Укажите химический состав и область терапевтического применения препаратов из данного растительного сырья. ОТВЕТ. Корневища Змеевика – Rhizomata Bistorta Горец змеиный - Polygonum bistorta Горец мясо-красный - Polygonum carneum Сем. гречишные – Polygonaceae Химический состав. В корневищах содержатся дубильные вещества (15-25%), свободные полифенолы (галловая кислота и катехин), оксиантрахиноны, крахмал (до 26%), оксалат кальция. Качественные реакции. ГФ ХI: К 1 мл отвара корневищ (1:10) прибавляют 2-3 капли раствора железоаммониевых квасцов; появляется черно - синее окрашивание (дубильные вещества). Количественное определение: ГФ ХI дает определение содержания дубильных веществ в ЛРС: Метод: пермангонатометрии, основан на окислении дуб. веществ перманганатом калия. Методика по ГФ ХI, параллельно проводят контрольный опыт. По ГФ XI требуется содержание дубильных веществ не менее 15%. Ситуационная задача № 42 1. В РПО аптеки поступил рецепт: Rp.: Platyphyllini hydrotartratis 0,003 Papaverini hydrochloridi 0,05 Dibazoli 0,05 Basis axungicae q.s. ut fiat suppositorium. Da tales doses № 40. Signa. Вводить в прямую кишку по 1 суппозиторию 2 раза в день. После изготовления суппозиториев провизор-технолог установил соответствие их качества по всем показателям. • Перечислите показатели качества суппозиториев и назовите методики их определения. • Производится ли проверка доз для данной лекарственной формы? Ответ обоснуйте. • Какие физико-химические свойства лекарственных и вспомогательных веществ учитываются в процессе изготовления препарата? Каковы особенности введения лекарственных веществ в состав жировой основы? Изложите рациональный вариант технологии изготовления препарата в аптеке. • Назовите основные группы и ассортимент вспомогательных веществ, применяемых в промышленном производстве суппозиториев. Перечислите основные стадии технологического процесса производства суппозиториев методом выливания. Рассмотрите с позиций биотехнологии в производстве лекарственных средств растительного происхождения: • сравнительную характеристику способов культивирования клеточных культур растений с целью получения фармацевтических субстанций алкалоидов. • Укажите область терапевтического применения данного препарата. ОТВЕТ. В рецепте прописаны ректальные суппозитории распределительным способом. Суппозитории – это твердая при комнатной температуре и расплавляющаяся или растворяющаяся при температуре тела, дозированная ЛФ для введения в естественные и патологические отверстия организма. Требования: - д.б. твердыми при комнатной температуре - однородными (на срезе) - д.б. одинаковой формы - должны деформироваться в течение 15 мин или растворятся в течение 1 часа Прописана свободнодисперсная система с упруго пластичной дисперсионной средой и дисперсной фазой в виде частиц разной формы (платифиллин, дибазол, папаверин). Проверка доз обязательна, т.к ЛВ из слизистой кишечника быстро попадают в системный кровоток, минуя печень. (ВРД и ВСД приравниваются к дозам внутривенного введения) ВРД(плат)= 0,01 (0,03) ЛРД(плат)= 0,003 ЛСД= 0,003*2=0,006 доза не завышена
ВРД(папав)= 0,2 (0,6) ЛРД(папав)= 0,05 ЛСД= 0,05*2=0,1 доза не завышена
ВРД(диб)= 0,05 (0,15) ЛРД(диб)= 0,05 ЛСД= 0,05*2=0,1 доза не завышена
Технология. Метод выливания. Платифиллин вводят в основу предварительно растворив в воде. Дибазол трудно растворим в воде, папаверина г/хл - медленно, поэтому их вводят в основу по типу суспензии. ЛВ, растворимые в жирах (ментол, камфара, фенилсалицилат, тимол, фенол) растворяют в основе при методе выливания, при методе выкатывания растирают с частью измельченной основы. ЛВ, растворимые в воде (новокаин, соли алкалоидов, танин, колларгол, протаргол) обязательно растворяют в минимальном количестве воды, остальные измельчают в присутствии воды. Эмульгируют водные растворы при методе выливания ПАВами, при методе выкатывания – ланолином безводным (1-1,5г на 30г суппозиторной массы). ЛВ, нерастворимые ни в воде, ни в основе, вводят в основу по типу суспензии в виде мельчайших порошков. Способ измельчения определяется количеством нерастворимой фазы. Для измельчения небольших количеств веществ используют вспомогательную жидкость, значительных количеств – часть расплавленной основы при методе выливания, часть измельченной основы при методе выкатывания.
Основу отвешивают на тарирных весах, переносят в фарфоровую чашку и плавят на водяной бане. В ступке в 5 каплях воды очищенной растворяют платифиллин, добавляют 0,06 ланолина безводного, пестиком перемешивают и отодвигают на край ступки. В ступку отвешивают 2,0 дибазола и 2,0 папаверина, измельчают пестиком. Затем добавляют расплавленую основу, перемешивают, добавляют массу с края ступки, перемешивают и выливают массу в охлажденные формы, смазанные мыльным спиртом или глицерином. Формы ставят в холодильник до полного отвердевания (15-20мин). Затем формы раскручивают, извлекают суппозитории и каждый заворачивают в вощеную капсулу. Помещают в бумажный пакет. Опечатывают. Оформляют к отпуску. Этикетка «Наружное» с оранжевой полосой, «Беречь от детей», «Хранить в прохладном месте», «Обращаться с осторожностью». Срок годности 10сут (приказ №214) Контроль качества По приказу №214 обязательные виды контроля: органолептический (цвет, запах, форма, однородность на срезе), письменный, контроль при отпуске. Выборочные виды контроля: химический (качественный и количественный), физический (по приказу №305 допускается отклонение ±5%), опросный.
Липофильные основы. В качестве суппозиторных основ ГФ XI рекомендует использовать масло какао, сплавы его с парафином и гидрогенизированными жирами, растительные и животные гидрогенизированные жиры, твёрдый жир, ланоль, сплавы гидрогенизированных жиров с воском, твердым парафином. Масло какао в настоящее время в фармакопеях ряда стран остаётся официнальной фармакопейной основой. Оно состоит из смеси триглицеридов: тристеарина, трипальметина, триолеина, трилаурина, триарахина. Для улучшения структурно-механических свойств и способности к высвобождению лек.в-ва. К маслу какао добавляют различные вспомогательные в-ва: лецитин, белый воск, крахмал, микрокристаллическую целлюлозу, аэросил, пальмовое масло. Гидрогенизированные жиры позволяют создать суппозиторные основы, лишенные недостатков масло какао. В промышленном производстве суппозиториев используется основа Нижегородского химико-фармацевтического завода, в состав которой входит 30% масла какао, 49-60%гидрированного подсолнечного масла и 10-21% парафина; ланолевая основа, состоящая из 60-80%ланоля, 10-20% кулинарного жира и 10-20% парафина. Из известных зарубежных липофильных основ особый интерес представляют основы витепсол, эстаринум, лазупол. Гидрофильные основы. Полиэтиленгликоль (ПЭГ) конденсированный полимер этиленоксида и воды. Желатин-глицериновые и мыльно-глицериновые основы значительно реже используются в производстве суппозиториев, хотя и включены в фармакопеи ряда стран. Суппозитории в промышленном производстве изготавливают способами выливания расплавленной массы в формы и прессования на специальном оборудовании. Наиболее часто применяемый способ – это выливание расплавленной массы в формы. Суппозитории должны иметь однородную массу, одинаковую форму и обладать твердостью, обеспечивающей удобство применения. Однородность определяют визуально на продольном срезе по отсутствию вкраплений. На срезе допускается наличие воздушного стержня или воронкообразного углубления. Среднюю массу определяют взвешиванием 20 суппозиториев с точностью до 0,01г. Отклонения в массе не должна превышать + 5% и только 2 суппозитория могут иметь отклонение+_7,5% Для суппозиториев, изготовленных на липофильных основах, определяют темпер. плавления по методу (ГФ XI вып 1) кот. не должна превышать 370С. Если нет др. указаний в частных статьях. Если определение темп.плав. затруднительно. То определяют время полной деформации согласно приложению. Время полной деформации д.б не более 15 мин., если нет др. указаний в частных статьях. Для суппозиториев, изготовленных на гидрофильных основах, определяют время растворения. Для этого один суппозиторий помещают на дно сосуда вместимостью 100 мл. содержащего 50 мл воды, через каждые 5 мин взбалтываем, свеча должна растворится в теч. 1 часа, если нет др. указаний в частных статьях. Определение количественного содержания и однородность дозирования действующих веществ д.б. указаны в частных статьях. При изготовлении суппозиториев могут применяться антиоксиданты - бутилокситолуол, бутилоксианизол, регуляторы рН - лимонная кислота, ПАВ - эмульгатор N1, эмульгатор Т-1, эмульгатор Т-2, твин-80, спирты шерстного воска, аэросил и другие вспомогательные вещества, разрешенные для медицинского применения.
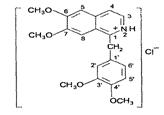
2. Пользуясь нормативной документацией, охарактеризуйте субстанцию папаверина гидрохлорида: 1) приведите русское, латинское, международное непатентованное наименование вещества; укажите химическую классификацию вещества, назовите функциональные группы; 2) обоснуйте физико-химические свойства в соответствии с составом и химическим строением вещества; 3) назовите методы определения примесей, напишите уравнения реакций для примесей, определяемых унифицированными методиками; 4) напишите уравнения реакций подлинности, указанных в нормативной документации; предложите другие методы идентификации вещества; 5) назовите и обоснуйте метод количественного определения, указанный в нормативной документации, приведите химизм реакции, предложите альтернативные методы количественного определения вещества. химическую классификацию вещества, назовите функциональные группы;
Производное бензилизохинолина
2) обоснуйте физико-химические свойства в соответствии с составом и химическим строением вещества Белые или почти белые кристаллы или белый или почти белый кристаллический порошок без запаха. Растворим в хлороформе, умеренно растворим в воде, мало растворим в спирте 96%.
3) назовите методы определения примесей, напишите уравнения реакций для примесей, определяемых унифицированными методиками; Прозрачность раствора. Раствор должен быть прозрачным или выдерживать сравнение с эталоном Цветность раствора - должен выдерживать сравнение с эталоном рН. От 3,0 до 4,5 Легко карбонизируемые примеси. Пятно любой посторонней примеси на хроматограмме не должно превышать пятно на хроматограмме раствора сравнения не более 0,1% Потеря в массе при высушивании не должна превышать 0,5%. Сульфатная зола не должна превышать 0,1% тяжелые металлы не более 0,001% в субстанции Железо. Сульфатная зола не более 0,003% в субстанции Остаточные органические растворители. Бактериальные эндотоксины. Не более 2,9 ЕЭ на 1 мг субстанции. Микробиологическая чистота.
4) напишите уравнения реакций подлинности, указанных в нормативной документации; предложите другие методы идентификации вещества; 1. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см по положению полос поглощения должен соответствовать рисунку спектра папаверина гидрохлорида 2. Ультрафиолетовый спектр поглощения 0,0005% раствора субстанции в 0,01 М растворе хлористоводородной кислоты в области от 230 до 270 нм должен иметь максимум при 251 нм. 3. К субстанции прибавляют 1 мл серной кислоты концентрированной и нагревают; появляется фиолетовое окрашивание. 4. Субстанция дает характерную реакцию на хлориды. 5.Реакции с общеалкалоидными реактивами: Реактив Марки - при добавления бромной воды и р-ра аммиака появляется фиолетовый осадок, после растворения в этаноле окрашивается в фиолетово-красный цвет
- с реактивом молибдата аммония в конц. серной к-те (реактив Фреде) –зеленое окрашивание 5) назовите и обоснуйте метод количественного определения, указанный в нормативной документации, приведите химизм реакции, предложите альтернативные методы количественного определения вещества. Метод неводного титрования в смеси муравьиной кислоты и уксусного ангидрида и титруют 0,1 М раствором хлорной кислоты до появления ярко-желтого окрашивания (индикатор - 0,15 мл 0,1% раствора кристаллического фиолетового). Параллельно проводят контрольный опыт 3. Какие виды внутриаптечного контроля необходимо применить для данной лекарственной формы? Кем проводится контроль при отпуске. Какие процедуры осуществляет работник аптеки при данном виде контроля? Какие журналы должен оформить провизор-аналитик по результатам проведения органолептического контроля? Каковы действия материально-ответственных лиц аптеки, при поступлении большого количества неправильно выписанных рецептов? К какому виду товарооборота относится отпуск лекарственных средств по рецептам? Предложите алгоритм проведения первичного учета амбулаторной рецептуры в аптеке. ОТВЕТ. Рецепт на свечи в случае иногороднего отпуска оформляется согласно приказа №110 МЗСР РФ от 12.02.2007 «О порядке назначения и выписывания лс и имн, а также специализированных продуктов питания» на 107 бланке с указанием всех реквизитов и правилами оформления рецепта, т.к. платифиллин не стоит на пку, а относится к списку А, а папаверин и дибазол относятся к списку Б. В случае поступления большого количества неправильно оформленных рецептов: регистрируем в журнале неправильно выписанных рецептов, по возможности делаем ксерокопию рецепта, рецепт гасим штампом «не действителен», сообщаем в ЛПУ. Отпуск лекарств по рецептам врача относится к розничному товарообороту. Оборот по амбулаторной рецептуре - особый вид продажи, величина которого определяется медицинскими работниками (промежуточными потребителями лекарственных препаратов), выписавшими рецепт на экстемпоральную или готовую лекарственную форму. При учете экстемпоральных лекарственных форм за единицу принимается одна рецептурная пропись независимо от числа входящих в нее ингредиентов и их количества. Данные о количестве и стоимости экстемпоральных лекарственных форм получают на основании записей в рецептурном журнале, который ведется аптечными организациями с небольшим объемом работы, или корешков квитанций на заказанные лекарства, также данные контрольно-кассовой ленты. Ежедневно в конце смены или рабочего дня переносят сведения о количестве и стоимости экстемпоральных лекарственных форм в журнал учета рецептуры, в т.ч. количество и сумму бесплатных и льготных рецептов. Сумма отпуска включается в выручку рецептурно-производственного отдела и отражается в кассовой книге и расходной части товарного отчета материально-ответственного лица. Готовые лекарственные формы ежедневно учитываются по стоимости (бесплатные и льготные ежедневно учитываются по количеству и по стоимости). За 1 готовое лекарственное средство промышленного производства принимают оригинальную единичную упаковку в готовом для отпуска населению виде. Сумма выручки фиксируется в журнале учета рецептуры, кассовой книге и расходной части товарного отчета. Для количественного учета ГЛФ за любой период времени при отсутствии автоматических средств попредметного учета каждой реализованной ассортиментной позиции можно использовать условный расчетный метод: в течение 5 дней в начале периода и 5 дней в конце периода определяется количество и стоимость ГЛФ, отпущенных населению. Рассчитывается средняя стоимость 1 ГЛФ в изучаемом периоде. Получив из журнала учета рецептуры стоимость ГЛФ за весь период, и зная среднюю стоимость первой ГЛФ, рассчитывается количество ГЛФ в этом периоде. При расчете бесплатных и льготных рецептов дополнительно к названным первичным документам по экстемпоральным и ГЛФ составляется сводный реестр, на основе которого аптечная организация, осуществляющая отпуск товаров декретированным группам населения на бесплатных и льготных условиях выписывают счет для оплаты ЛП. К счету прилагается сводный реестр и первые экземпляры рецептов формы 148-1/у-88. Счета регистрируются в реестре выписанных покупателям требованиям-накладным. К обороту стационарной рецептуре также относят ЛФ, изготавливаемые в аптеках по требованиям ЛПУ и ГЛФ. Количество стационарной рецептуры (для определения общего числа ЛП, отпущенных по рецептам) рассчитывают, приравнивая стоимость одного амбулаторного рецепта к стоимости одного стационарного. Рецепты по экстемпоральным и ГЛФ соответственно, используют также условный расчетный метод.
4. Дайте характеристику растения - источника платифиллина. • Приведите латинское название, охарактеризуйте сырьевую базу, условия сбора, сушки и хранения сырья. • Назовите фармакологическую группу, пути использования и лекарственные препараты платифиллина.
Ситуационная задача № 43 1. На фармацевтическое предприятие поступили: лекарственное растительное сырье «Листья подорожника большого» и субстанции теобромина и теофиллина для изготовления лекарственных средств. Необходимо провести аналитический контроль и дать заключение о качестве сырья и субстанций. Дайте экологическую характеристику сырьевой базы подорожника. Составьте инструкцию по сбору, сушке и хранению листьев подорожника большого. Какие приемы могут использовать сборщики при заготовке листьев подорожника, учитывая его морфологические особенности? При анализе сырья по внешним признакам возникло сомнение в его подлинности. Какие методы фармакогностического анализа необходимо использовать для определения подлинности сырья? Как отличить подорожник большой от близких видов (примесей)? Какой числовой показатель свидетельствует о степени чистоты сырья? Как особенности местообитания подорожника большого влияют на качество его сырья? Дайте рекомендации по применению в медицинской практике препаратов подорожника экстемпорального и заводского производства. Отметьте возможные противопоказания или ограничения при их использовании. ОТВЕТ. Анализ осуществляется в соответствии с ГФ ХI вып.2 ст.20: несоответствие по двум показателям: влажность и пожелтевшие и побуревшие листья. Сырье приемке не подлежит. Или принимаем, доводим до стандартного состояния: убираем пожелтевшие и побуревшие листья; и используем для приготовления плантаглюцида (для сока сырье использовать нельзя). Подорожник большой - многолетнее травянистое растение с розеткой прикорневых листьев, стебли безлистные с густым колосовидным соцветием на верхушке, листья эл
|
|||||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 487; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.178.157 (0.129 с.) |
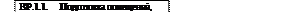
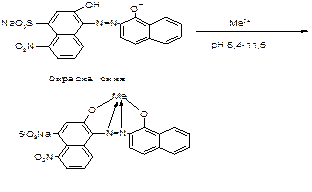
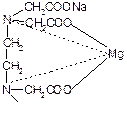
 В структуре суппозиториев различают основные (лек.в-ва) и вспомогательные (носители или основа) компоненты.
В структуре суппозиториев различают основные (лек.в-ва) и вспомогательные (носители или основа) компоненты.
 ,
,  бензойное кольцо, связанная хлороводородная к-та, СН3 метоксигруппа
бензойное кольцо, связанная хлороводородная к-та, СН3 метоксигруппа