
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
А-2- кривая процесса расширения рабочего тела; 2-б-1- кривая процесса сжатия рабочего тела.
Площадь под кривой 1-а-2 равна работе расширения газа, площадь под кривой 2-б-1 равна работе сжатия газа, а площадь, ограниченная замкнутой кривой (кривой цикла) 1-а-2-б-1 представляет собой работу, совершаемую газом в циклическом процессе. Отсюда следует, что для того, чтобы работа, совершаемая газом в циклическом процессе, была положительной и вообще существовала, необходимо, чтобы кривая процесса сжатия газа 2-б-1 в
4.3 Энтропия идеального газа
Энтропия представляет собой функцию состояния термодинамической системы, т.е. энтропия зависит от параметров состояния системы, а именно от абсолютного давления ( Основным уравнением для определения изменения энтропии в обратимом процессе является выражение:
Обратимыми называются процессы, в результате протекания которых в прямом и обратном направлениях в прямом и обратном направлениях термодинамическая система возвращается в исходное состояние, не вызывая при этом никаких изменений в окружающей среде (например, изменения температуры окружающей среды). Привести пример с перемещением металлического шарика между двумя плоскостями. Формула (4.31) показывает, что Поскольку в теплотехнических расчетах в основном приходится рассчитывать не саму величину энтропии термодинамической системы (рабочего тела), а ее изменение, то отсчет значений энтропии можно вести от любого состояния рабочего тела. Для газов принято считать значение энтропии равным нулю при нормальных условиях. Определение энтропии при постоянной теплоемкости (т.е. в расчетах полагается, что теплоемкость не зависит от температуры) осуществляется по следующим формулам:
Изменение энтропии при переходе газа из состояния 1 в состояние 2, т.е. при осуществлении термодинамического процесса определяется по следующим формулам:
Лекция №5
5.1 Цикл Карно
Очевидно, что чем больше теплоты ( В связи с этим, возникает вопрос: какое максимальное значение может иметь КПД цикла? Впервые этот вопрос изучил в 1827 году французский инженер Сади Карно. В результате своих исследований Карно предложил цикл, имеющий наивысший термический КПД в диапазоне температур горячего источника (
Рассмотрим цикл Карно в 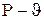 координатах. координатах.
На рисунке 5 изображены следующие процессы: 4-1- адиабатное сжатие смеси воздуха и топлива в цилиндре двигателя; 1-2- изотермический подвод теплоты к смеси воздуха и топлива (воспламенение и горение топливной смеси, например, от свечи зажигания). Продукты сгорания топлива расширяются, перемещают поршень в цилиндре и, следовательно, совершают работу. После того, как продукты сгорания топлива расширились до состояния, соответствующего точке 2, (все топливо сгорело и, следовательно, подвод теплоты прекращается), дальнейшее расширение газа до точки 3 происходит без подвода теплоты по адиабате. Адиабатное расширение продуктов сгорания в цилиндре двигателя (топливо превратилось в продукты сгорания, следовательно, подвода теплоты нет). В процессе адиабатного расширения температура продуктов сгорания уменьшается, поскольку теплота к ним не подводится, и работа совершается только за счет изменения внутренней энергии продуктов сгорания.
Изотермическое вытеснение продуктов сгорания из цилиндра двигателя. На это затрачивается работа того же поршня. Одновременно с вытеснением продуктов сгорания из цилиндра, осуществляется передача теплоты продуктов сгорания холодному источнику теплоты.
Таким образом, цикл Карно состоит из двух изотерм и двух адиабат. Работа, совершаемая газом при расширении, изображается в
|
||||||||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 188; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.141.31.209 (0.005 с.) |
 координатах была расположена ниже кривой расширения 1-а-2.
координатах была расположена ниже кривой расширения 1-а-2.
 ), плотности (
), плотности ( ) и абсолютной температуры (
) и абсолютной температуры (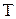 ).
).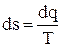 (4.31)
(4.31)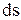 и
и  имеют одинаковые знаки, следовательно, по характеру изменения энтропии в обратимом процессе можно судить о том, в каком направлении протекает процесс. При подводе теплоты к рабочему телу
имеют одинаковые знаки, следовательно, по характеру изменения энтропии в обратимом процессе можно судить о том, в каком направлении протекает процесс. При подводе теплоты к рабочему телу  его энтропия возрастает (
его энтропия возрастает (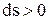 ), а при отводе теплоты энтропия рабочего тела убывает.
), а при отводе теплоты энтропия рабочего тела убывает. (4.32)
(4.32)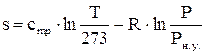 (4.33)
(4.33) (4.34)
(4.34)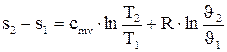 (4.35)
(4.35)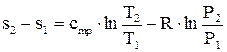 (4.36)
(4.36) (4.37)
(4.37) ), подведенной к рабочему телу в цикле, превращается в механическую работу (
), подведенной к рабочему телу в цикле, превращается в механическую работу (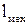 ) и, следовательно, чем меньше передается ее холодному источнику теплоты (окружающей среде), тем, очевидно выше КПД цикла.
) и, следовательно, чем меньше передается ее холодному источнику теплоты (окружающей среде), тем, очевидно выше КПД цикла.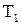 ) и холодного источника (
) и холодного источника (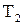 ).
).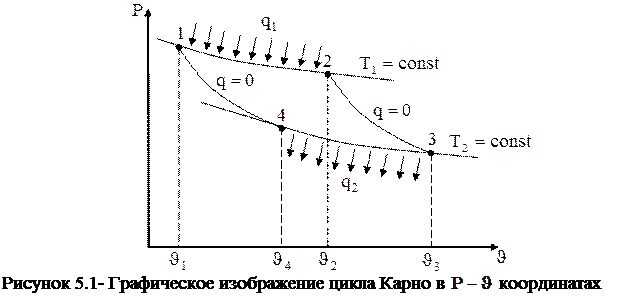
 (5.1)
(5.1) (5.2)
(5.2)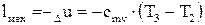 (5.3)
(5.3)


