Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Пищевые кислоты, их характеристика
Уксусная кислота
Уксусная кислота (ледяная) (СН3СООН) – пищевой консервант Е 260. Является наиболее известной пищевой кислотой и выпускается в виде эссенции, содержащей 70 – 80% собственно кислоты [9]. Уксусная кислота – бесцветная жидкость, смешивающаяся с водой во всех отношениях. Она впитывает из окружающей среды влагу и замерзает при температуре 16,5°С с образованием бесцветных твердых кристаллов. В быту используют для консервирования разбавленную водой уксусную эссенцию, которая получила название столовый уксус. В зависимости от сырья, из которого получают уксусную кислоту, различают винный, фруктовый, яблочный, спиртовой уксус и синтетическую уксусную кислоту. Уксусную кислоту получают путем уксуснокислого брожения. Уксусно-кислое брожение представляет собой процесс превращения этилового спирта при участии кислорода в уксусную кислоту. Брожение является значимым в хозяйственном отношении, так как позволяет получать в больших количествах из доступных субстратов уксусную кислоту ‒ вещество, обширно используемое в пищевой, текстильной и других отраслях промышленности. Процесс уксусно-кислого брожения проходит в два этапа. Сначала этиловый спирт окисляется до уксусного альдегида:
а затем уксусный, альдегид в результате дальнейшего окисления превращается в уксусную кислоту:
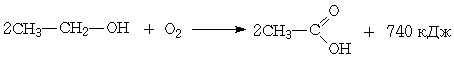
Результаты этих превращений могут быть выражены следующим суммарным уравнением:
Важным способом промышленного синтеза уксусной кислоты является каталитическое карбонилирование метанола моноксидом углерода, которое происходит по формальному уравнению:
Соли и эфиры этой кислоты называются ацетаты. В качестве пищевых добавок применяются ацетаты калия и натрия (Е 461 и Е 462) [8]. Уксусная кислота не имеет законодательных ограничений; ее действие основано, главным образом, на снижении pH консервируемого продукта, проявляется при содержании выше 0,5% и направлено, в основном, против бактерий. Основная область применения – овощные консервы и маринованные продукты. Используется в майонезах, соусах, при мариновании рыбной продукции и овощей, ягод и фруктов. Уксусная кислота широко используется также как вкусовая добавка.
Молочная кислота Молочная кислота (СH3–СH(ОH)–СООH) – пищевой консервант Е 270, прозрачная жидкость без мути и осадка, имеющая слабый, характерный для молочной кислоты запах и кислый вкус. Выпускается в двух формах, отличающихся концентрацией: 40%-й раствор и концентрат, содержащий не менее 70% кислоты. Получают молочнокислым брожением сахаров.
Ее соли и эфиры называются лактатами. Применяется молочная кислота в консервной, мясоперерабатывающей, рыбной, молокоперерабатывающей, масложировой и других отраслях пищевой промышленности. А также в производстве безалкогольных напитков и некоторых сортов пива, кондитерских изделий. Молочная кислота имеет ограничения к применению в продуктах детского питания. Добавка-консервант Е 270 разрешена для использования в пищевой промышленности Российской Федерации и других стран.
Лимонная кислота
Лимонная кислота ((HООС–СH2)2–С(ОH)–СООH) – пищевой антиоксидант Е 330. Кристаллическое вещество белого цвета, температура плавления 153°С, хорошо растворима в воде, растворима в этиловом спирте, малорастворима в диэтиловом эфире. Продукт лимоннокислого брожения сахаров. Осуществляется при участии ферментов плесневого гриба Aspergillius niger:
Обладает наиболее мягким вкусом по сравнению с другими пищевыми кислотами и не проявляет раздражающего действия на слизистые оболочки пищеварительного тракта. Соли и эфиры лимонной кислоты – цитраты, применяются для регулирования кислотности, усиления вкуса, а также в качестве консерванта. Особенно широко лимонная кислота применяется при производстве безалкогольных напитков, некоторых видов рыбных консервов, кондитерских и хлебобулочных изделий. В последних, добавка Е 330 зачастую применяется как один из компонентов разрыхлителей или "улучшителей" теста [8]. Все известные организации по контролю за пищевыми продуктами относят пищевую добавку Е 330 к классу безопасных для здоровья. В Российской Федерации входит в список разрешенных пищевых добавок.
Яблочная кислота Яблочная кислота (HООС–СH2–СH(ОH)–СООH) – консервант Е 296, представляет собой бесцветные гигроскопичные кристаллы, хорошо растворимые в воде и этиловом спирте, плавящиеся при температуре 100°С. Обладает менее кислым вкусом, чем лимонная и винная. Для промышленного использования эту кислоту получают синтетическим путем из малеиновой кислоты, в связи с чем критерии чистоты включают ограничения по содержанию в ней примесей токсичной малеиновой кислоты.
Соли и эфиры яблочной кислоты называются малатами. Яблочная кислота обладает химическими свойствами оксикислот. При нагревании до 100°С превращается в ангидрид. Применяется при изготовлении вин, кондитерских изделий (желе, пастила, мармелад), бакалейных продуктах (майонез, сыры, рыба, соус), фруктовых газированных вод и соков, а также в молочных продуктах в качестве стабилизатора эмульсии яичного желтка, в замороженных изделиях (мороженое) [1]. Винная кислота Винная кислота (HООС–СH(ОH)–СH(ОH)–СООH) – антиоксидант Е 334, кристаллическое вещество без цвета и запаха, но с кислым вкусом. Является продуктом переработки отходов виноделия (винных дрожжей и винного камня). Расщепление виннокислой извести. Из полученной тем или иным способом виннокислой извести в специально предназначенных для этих целей коррозионно-стойких реакторах (расщепителях) выделяют винную кислоту по реакции:
В растворе образуется свободная винная кислота, а в осадке гипс. Расщепление надо проводит так чтобы получить кристаллы гипса наибольшей величины, что уменьшает удельное сопротивление при его промывке и облегчает фильтрацию [15]. Винная кислота не обладает каким-либо существенным раздражающим действием на слизистые оболочки желудочно-кишечного тракта, также не подвергается обменным превращениям в организме человека. Основная часть (около 80%) разрушается в кишечнике под действием бактерий. Соли и эфиры винной кислоты называются тартратами. В пищевой промышленности винная кислота используется в качестве регулятора кислотности и антиоксиданта при производстве консервов, джемов, желе и различных кондитерских изделий. Добавка Е 334 добавляется при изготовлении напитков и столовых вод, находит широкое применение в сфере виноделия. Винная кислота является одной из составляющих терпкого вкуса в вине. Добавка Е 334 входит в перечень разрешенных пищевых добавок в России [23]. Аскорбиновая кислота Аскорбиновая кислота (витамин С) – антиоксидант Е 300. Представляет собой белое кристаллическое вещество с Тпл – 192°С, очень чувствительна к нагреванию, хорошо растворима в воде, плохо в спиртах (за исключением метанола), практически нерастворима в неполярных растворителях. Она очень чувствительна к тяжелым металлам, медь и железо на аскорбиновую кислоту действуют разрушающе. Аскорбиновая кислота, как природный антиоксидант, используется для предотвращения окислительной порчи жиров в продуктах питания. Она прерывает реакции самоокисления в компонентах пищевых изделий, предотвращая снижение органолептических характеристик продуктов. Аскорбиновая кислота увеличивает срок хранения продуктов в несколько раз. Она замедляет ферментативное окисление вина, пива и безалкогольных напитков, предохраняет фрукты, овощи и продукты их переработки от потемнения при замораживании, консервировании и расфасовке, сохраняя в них витамины. Аскорбиновая кислота позволяет на треть снизить количество нитритов и нитратов, необходимых в мясных изделиях. Она обеспечивает устойчивый и равномерный посол, ускоряет процесс консервирования, замедляет образование метмиоглобина на поверхности мяса.
Аскорбиновая кислота принимает активное участие в окислительно – восстановительных процессах в организме и входит в состав ряда сложных ферментов, обусловливающих процессы клеточного дыхания. Витамин С участвует в процессах углеводного и белкового обмена, повышает сопротивляемость организма к инфекционным заболеваниям, регулирует холестериновый обмен, участвует в нормальном функционировании желудка, кишечника и поджелудочной железы; совместно с витамином Р обеспечивает нормальную эластичность стенок кровеносных капилляров, обезвреживает действие ряда лекарственных веществ и ядов. Аскорбиновая кислота применяется при лечении цинги, инфекционных заболеваний, ревматизма, туберкулеза, язвенной болезни, при гепатитах, шоковом состоянии и др. В случае нехватки аскорбиновой кислоты развивается гиповитаминоз, в тяжелых случаях ‒ авитаминоз (цинга, скорбут). При цинге отмечается утомляемость, сухость кожи, расшатываются и выпадают зубы, наблюдаются боли в конечностях, снижается сопротивляемость к инфекциям. В конечном итоге, цинга приводит к летальному исходу. Аскорбиновая кислота содержится в значительных количествах в овощах, плодах, ягодах, хвое, шиповнике, в листьях черной смородины.
Рис.1. Растительные объекты, содержащие аскорбиновую кислоту Под влиянием высоких температур, кислорода, особенно в присутствии тяжелых металлов, витамин С легко разрушается. В организме человека и большинства животных аскорбиновая кислота не синтезируется.
|
|||||||
|
Последнее изменение этой страницы: 2020-03-27; просмотров: 112; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.185.180 (0.008 с.) |