Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Производные арилоксипропаноламина
Группа β-адреноблокаторов является одной из первых групп лекарственных средств, введенных в медицинскую практику в 60-е годы двадцатого столетия. При исследовании новых производных изопреналина (описанного ранее) оказалось, что дихлоризопреналин играет роль антагониста изопреналина, блокируя β-адренорецепторы и усиливая α-адренэнергические свойства адреналина. Это наблюдение направило поиски новых соединений в сторону модификации ароматической части при сохранении боковой части молекулы, характерной для β-адренэргетиков. Было получено много соединений, содержащих заместители в положении 3 или 3 и 4 изопреналина, либо новых соединений, содержащих вместо бензола другие ароматические или гетероциклические радикала. При этом на первом этапе исследований боковая цепь должна была содержать остаток этаноламина в которой в положении С2 должен был стоять метильный радикал. Эти исследования имели теоретическое значение и в настоящее время имеют незначительное медицинское значение, т.к. в этой группе не удалось найти β-адреноблокаторов лишённых адреномиметического действия. Успехи в области создания β-адренолитиков были достигнуты путём введения в молекулу арильного, оксиметильного и изопропиламинного радикалов. В настоящее время можно выделить три основные группы β-адреноблокаторов, которые имеют следующую структуру
где: R1 - заместитель ароматического или гетероциклического строения R2 – изопропильный остаток или его аналог
Пропранолол Propranolol Анаприлин Anaprilinum Пропранолола гидрохлорид Propranolol Hydrochloride
М.м.= 295,8 1-(изопропиламино)-3(1-нафтокси)-пропанола-2 гидрохлорид Получают пропранолол следующим образом: α-нафтол образует с 1-хлор-2,3-эпоксипропаном 1-хлор-3(1-нафтокси)-пропанол-2. При его дальнейшем взаимодействии с изопропиламином образуется рацемический пропранолол.
Пропранолол - это белый кристаллический порошок, растворим в воде и спирте. Подлинность пропранолола устанавливают по УФ- и ИК-спектрам. УФ-спектр пропранолола должен иметь в метанольном растворе три полосы поглощения с максимумами при 290, 306 и 319 нм.
ИК-спектр должен совпадать с ИК-спектром стандартного образца пропранолола. Кроме того, подлинность пропранолола устанавливают по температуре плавленияего основания и по реакции на хлоридионы. Количественное определение пропранолола проводят методом титрования в безводной кислоте уксусной в присутствии ртути ацетата. Титрантом является кислота хлорная, а индикатором - кристаллический фиолетовый Пропранолол является β-адреноблокатором и проявляет гипотензивное, антиаритмическое и антиангинальное действие. Применяется он при стенокардии, аритмии и некоторых видов гипертонии в дозах от 0,01 до 0,08г. Выпускается пропранолол в таблетках, капсулах, в виде 1% раствора для инъекций.
Тимолола малеат Timolol maleate
М.м.= 432,5 (S)-1-третбутиламино-3-[(4-морфолино-1´,2´,5´-тиадиазол-3´-ил) окси] пропанола-2 малеат Тимолола малеат - это белый кристаллический порошок, растворим в воде и спирте. Подлинность тимолола малеата устанавливают по совпадению с ИК-спектром стандартного образца. УФ-спектр тимолола малеата в метаноле должен иметь полосу поглощения с максимумом при 299 нм, при 295 нм – в 0,1 М растворе кислоты хлористоводородной или при 296 нм – в 0,1 М растворе натрия гидроксида. На остаток малеиновой кислоты проводят реакцию обесцвечивания бромной воды. Удельное вращение тимолола малеата должно быть в пределах от -11,70 до -12,50 (в 5% растворе кислоты хлористоводородной). Количественное определение тимолола малеата проводят методом титрования кислотой хлорной в среде безводной кислоты уксусной, используя в качестве индикатора 1-нафтолбензеин
Тимолола малеат проявляет β-адреноблокаторное действие, подобное действию пропранолола. Он применяется при сердечно-сосудистых заболеваниях в дозах по 0,01. Широкое применение тимолол нашёл при глаукоме для снижения внутриглазного давления. Выпускается тимолол в таблетках по 0,005; 0,01 и 0,02г, в виде 0,1%; 0,25% и 0,5% растворов.
Атенолол
М.М.=266,3 4-(2-окси-3-изопропиламинопропокси)-фенилацетамид Атенолол - это белый порошок, умеренно растворим в воде и растворим в спирте.
Подлинность атинолола устанавливают по совпадению ИК-спектра с ИК-спектром стандартного образца. УФ-спектр атенолола в метаноле должен иметь полосы поглощения с максимумами при 275 и 282 нм. Температура плавления атенолола должна находиться в пределах 152-155 0С. Количественное определение атенолола проводят методом титрования кислотой хлорной в безводной кислоте уксусной. Атенолол является кардиоселективным β-адреноблокатором длительного действия. Назначают атенолол при артериальных гипертензиях, стенокардии, инфаркте миокарда внутрь по 0,05 и 0,1г 1-2 раза в день. Внутривенно атенолол вводят при аритмиях до 0,01 г. Выпускается атенолол в таблетках по 0,025; 0,05 и 0,1г, в виде 0,1% раствора.
1[(1-изопропоксиэтокси)-n-толил]-окси]-3изопропиламинопропанол-2 Бисопролол относится также к кардиоселективным β-адреноблокаторам. Применяется бисопролол при артериальной гипертензии, стенокардии, в постинфарктном периоде. Обычно его назначают в дозах 0,005 – 0,01 г. Выпускается бисопролол в таблетках по 0,005 и 0,01 г. Флуоксетин Fluoxetin Флуоксетина гидрохлорид
М.м.= Флуоксетин - это белый порошок, трудно растворим в воде, растворим в этаноле и метаноле. Подлинность флуоксетина устанавливают по совпадению ИК-спектра с ИК-спектром стандартного образца флуоксетина. УФ-спектр флуоксетина в метанольном растворе имеет полосу поглощения с максимумом при 227 нм. Кроме того, можно провести минерализацию и последующую идентификацию фторид-ионов. Количественное определение флуоксетина проводят методом титрования кислотой хлорной в безводной кислоте уксусной, после добавления ртути ацетата в присутствии индикатора кристаллического фиолетового. Разработана методика спектрофотометрического определения флуоксетина в метанольном растворе при длине волны 227 нм. Флуоксетин ингибирует мускариновые, гистаминовые и α1-адренергические рецепторы в ЦНС, эффективен при депрессиях, булимии, анорексии, алкоголизме в дозах от 20 мг с повышением суточной дозы до 80 мг в сутки в 2-3 приёма. Выпускается в капсулах по 20 мг.
Хлорамфеникол Chloramphenicolum Левомицетин Laevomycetinum
М.м.=323,1 1-n-нитрофенил-2-(2`,2-дихлорацетамино)-пропандиол-1,3 Хотя структурно левомицетин (хлорамфеникол) близок к выше приведенным фенилалкиламинам по фармакологическому действию он значительно отличается от них.Хлорамфеникол является продуктом жизнедеятельности актиномицета Streptomyces venezuele. При рассмотрении его структуры можно выделить в ней фрагмент фенилалкиламина, нитрогруппу и остаток дихлоруксусной кислоты. Это придаёт хлорамфениколу совершенно другие фармакологические свойства, а именно – противомикробные. Хлорамфеникол получают путём ферментации актиномицета (Streptomyces venezuele) в обычных для актиномицетов условиях (т.е. питательная среда, рН среды, температурный режим). Контроль за ферментацией ведут поляриметрическим методом. Когда удельное вращение этилацетатной вытяжки достигает определённого значения угла вращения. Следует заметить, что плоскость плоскополяризованного света хлорамфеникола в этилацетате имела левое вращение. Отсюда произошло первое название хлорамфеникола – левомицетин. Это название сохранилось в некоторых нормативных документах отдельных фирм.
Хлорамфеникол получают ферментативным путём. В настоящее время большую часть хлорамфеникола получают путём синтеза, который оказался более экономичным.

Хлорамфеникол В результате такого синтеза получают рацемическую смесь, которая в 2 раза менее активна по сравнению с R-изомером. Разделение такой смеси на изомеры проводят на стадии получения амина с помощью правовращающей винной кислоты, соли которой имеют разную растворимость в метаноле (в метаноле растворяется только R-изомер). Хлорамфеникол - это белый с желтоватым оттенком кристаллический порошок, малорастворимый в воде, растворим в спирте. Для определения подлинности хлорамфеникол растворяют в кислоте хлористоводородной и добавляют цинковую пыль, при этом нитрогруппа восстанавливается до аминогруппы. Далее проводят обычную реакцию образования азокрасителя.
При кипячении хлорамфеникола со щёлочью образуется осадок красно-бурого цвета. После охлаждения раствор фильтруют и в фильтрате обнаруживают хлорид-ионы
NaCl + AgNO3 → AgCl ↓ + NaNO3 УФ-спектр хлорамфеникола в спиртовом растворе должен иметь полосу поглощения с максимумом при 278 нм. ИК-спектр хлорамфеникола должен совпадать с ИК-спектром стандартного образца или со спектром, прилагаемым к НД. Удельное вращение хлорамфеникола в спиртовом растворе (5%) находится в пределах от +180 до + 210. Количественное определение хлорамфеникола проводят методом нитритометрическим методом после его восстановления цинковой пыдью в кислой среде. В качестве индикатора обычно используют йодкрахмальную бумажку. Химические реакции приведены ранее.
По фармакологическому действию хлорамфеникол является типичным антибиотиком. Он тормозит синтез белка внутри микробной клетки путём ингибирования пептидилтрансферазы врибосомах. Хлорамфеникол является бактериостатическим средством. Назначают хлорамфеникол при различных заболеваниях: при брюшном тифе, дизентерии, при различных глазных заболеваниях. Разовая доза для взрослых - 0,25 -0,5 г, детям назначают хлорамфеникол в зависимости от возраста. Курс лечения обычно 7-10 дней. Кроме хлорамфеникола выпускаются его эфиры со стеариновой и янтарной кислотами. Эти эфиры терапевтических преимуществ по сравнению с хлорамфениколом не имеют. Хлорамфеникола стеарат
Хлорамфеникола стеарат почти не имеет горького вкуса. Его фармакологическое действие такое же как и хлорамфеникола. Его активность примерно в два раза ниже по сравнению с хлорамфениколом. Выпускается хлорамфеникола стеакрат в таблетках по 0,25г.
|
||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 2429; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.190.167 (0.04 с.) |





 Известны и другие методы получения пропранолола, позволяющие получить разные энантиоформы
Известны и другие методы получения пропранолола, позволяющие получить разные энантиоформы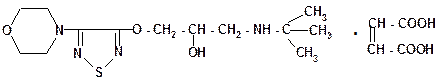



 Бисопролол
Бисопролол Fluoxetine Hydrochloride
Fluoxetine Hydrochloride
 Исходным продуктом является n-нитрофенилацетон, который подвергают бромированию, а затем атом брома замещают на аминогруппу. Для этого проводят реакцию с гексаметилентетрамином, а затем обрабатывают кислотой хлористоводородной. Полученный амин ацетилируют для защиты аминогруппы и формируют для введения оксиметильной группы. Полученный продукт восстанавливают в присутствиии алюминия изопропилата, гидролизуют и ацетилируют с помощью хлорангидрида или метилового эфира дихлоруксусной кислоты
Исходным продуктом является n-нитрофенилацетон, который подвергают бромированию, а затем атом брома замещают на аминогруппу. Для этого проводят реакцию с гексаметилентетрамином, а затем обрабатывают кислотой хлористоводородной. Полученный амин ацетилируют для защиты аминогруппы и формируют для введения оксиметильной группы. Полученный продукт восстанавливают в присутствиии алюминия изопропилата, гидролизуют и ацетилируют с помощью хлорангидрида или метилового эфира дихлоруксусной кислоты