
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ароматические углеводороды (Арены)
Ароматические УВ (арены) – это УВ, молекулы которых содержат одно или несколько бензольных колец или ядер.
C6H6
SP2 – гибридизация 1200 – валентный угол l = 0,140 нм (длина связи) π-электронное облако состоит из 6 Pe (электронов).
Гомологический ряд С6H6 – бензол С6H5 – CH3 – метилбензол С6H5 – C3H5 – этилбензол С6H5 – C3H7 – пропилбензол С6H5 – C4H9 – бутилбензол Физические свойства Бензол – бесцветная, нерастворимая в воде жидкость со своеобразным запахом. Его t кипения = 80,10 С. При охлаждении он легко застывает в белую кристаллическую массу с t плавления = 5,50 С. Химические свойства I. Реакции замещения 1. Взаимодействие с галогенами C6H6 + Br2 à C6H5Br + HBr (в присутствии FeCl3) 2. Взаимодействие с HNO3 C6H6 + HONO2 à C6H5NO2 + H2O (в присутствии H2SO4) нитробензол II. Реакции присоединения 1. Гидрирование (присоединение Н2)
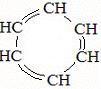
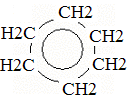
бензол циклогексан 2. Присоединение галогенов
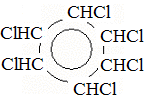
бензол гексохлорциклогексан III. Реакции окисления 1. Горение 2C6H6 + 15O2 à 12CO2 + 6H2O 2. Бензол стоек к действию окислителей. Окисляются только гомологи по боковой цепи. C6H5 – CH3 + 3O à C6H5 – COOH + H2O (в присутствии KMnO4) бензойная кислота Получение 1) Из циклогексана C6H12 à 3H2 + C6H6 (при t и катализаторе) циклогексан бензол 2) Из гексана C6H14 à C6H6 + 4H2 (при t и катализаторе) 3) Из ацетилена 3C2H2 à C6H6 (при t и катализаторе) Применение бензола: получение пластмасс, красителей, растворителей, бутадиенового каучука, волокна лавсана, сахарина, анилина, лекарств, средств для борьбы с вредными насекомыми и болезнями.
Задача № 4. Решение. n (H2SO4) = 49 г: 98 г/моль = 0,5 моль n (NaOH) = 20 г: 40 г/моль = 0,5 моль Так как серная кислота двухосновна, то она может образовать два ряда солей: 2 NaOH + H2SO4 = Na2SO4 + 2H2O средняя соль NaOH + H2SO4 = NaHSO4 + H2O кислая соль В нашей задаче оказалось равное мольное количество кислоты и щелочи, поэтому расчет следует вести по второму уравнению реакции: 0,5 моль 0,5 моль 0,5 моль NaOH + H2SO4 = NaHSO4 + H2O
m (NaHSO4) = M · n = 120 г/моль · 0,5 моль = 60 г. Ответ: 60 г гидросульфата натрия – кислая соль
Билет № 5 1. Общие физические и химические свойства металлов. Электрохимический ряд напряжений металлов. 2. Альдегиды, их строение и свойства. Получение, применение муравьиного и уксусного альдегидов.
3. Задача № 5. Через раствор, содержащий 60 г гидроксида натрия, пропущен углекислый газ, полученный при действии избытка соляной кислоты на 200 г карбоната кальция. Определите состав и массу полученной соли.
Металлы В периодах и группах периодической системы Д. И. Менделеева существуют закономерности в изменении металлических и неметаллических свойств элементов, можно достаточно определённо указать положение элементов-металлов и элементов-неметаллов в периодической системе. Если провести диагональ от элемента бора B (порядковый номер 5) до элемента астата At (порядковый номер 85), то слева от этой диагонали в периодической системе все элементы являются металлами, а справа от неё элементы побочных подгрупп являются металлами, а элементы главных подгрупп – неметаллами. Элементы расположенные вблизи диагонали (например, Al, Ti, Ge, Sb, Te, As, Nb), обладают двойственными свойствами: в некоторых своих соединениях ведут себя как металлы; в некоторых – проявляют свойства неметаллов. Все s -элементы (кроме H и He), d -элементы (все элементы побочных подгрупп) и f -элементы (лантаноиды и актиноиды) являются металлами. Среди p -элементов есть и металлы, и неметаллы, число элементов-металлов увеличивается с увеличением номера периода. Деление на металлы и неметаллы объясняется различием в строении атомов. Рассмотрим, например, строение атомов третьего периода: Элементы третьего периода: Na, Mg, Al, Si, P, S, Cl, Ar (аргон). Радиус атома: 0.19; 0.16; 0.143; 0.134; 0.130; 0.104; 0.099. Число электронов на внешнем слое: 1, 2, 3, 4, 5, 6, 7. Электроотрицательность: 0.9; 1.2; 1.5; 1.8; 2.1; 2.5; 3.0. Любой гидроксид содержит гидроксидные группы – OH. Слева направо: а. Радиус атомов уменьшается; б. Заряд ядра увеличивается; в. Электроотрицательность увеличивается; г. Число электронов на внешнем слое увеличивается; д. Прочность связи внешних электронов с ядром увеличивается; е. Способность атомов отдавать электроны уменьшается. Поэтому: Na, Mg, Al – металлы, а Si, P, S, Cl – неметаллы. Атомы большинства металлов на внешнем электронном слое имеют от 1 до 3 электронов. Исключение: атомы германия Ge, олова Sn, свинца Pb на внешнем электронном слое имеют четыре электрона, атомы сурьмы Sb, висмута Bi – пять, атомы полония Po – шесть. Атомы металла имеют меньший заряд ядра и больший радиус (размер) по сравнению с атомами неметаллов данного периода. Потому прочность связи внешних электронов с ядром в атомах металлов небольшая. Атомы металлов легко отдают валентные электроны и превращаются в положительно заряженные ионы.
Простые вещества, которые образуют элементы-металлы, при обычных условиях являются твёрдыми веществами (кроме ртути). Кристаллическая решётка металлов образуется за счёт металлической связи. Имеющиеся между узлами кристаллической решётки свободные электроны могут переносить теплоту и электрический ток, что является причиной главных физических свойств металлов – высокой электро- и теплопроводности. Металлическая связь образуется во всех металлах. Это связь, которую осуществляют относительно свободные электроны с положительными ионами металлов в кристаллической решётке. Атомы металла легко отдают валентные электроны и превращаются в положительные ионы. Относительно свободные электроны перемещаются между положительными ионами металла и между ними возникает металлическая связь, то есть электроны как бы цементируют положительные ионы металла в кристаллической решётке. Атомы металлов более или менее легко отдают электроны, то есть окисляются. Энергия, которая необходима для отрыва электрона от атома и превращение его в положительно заряженный ион, называется энергией ионизации. Металлы характеризуются небольшими величинами энергий ионизации. Атомы металлов не могут присоединять электроны. Поэтому металлы во всех химических реакциях являются восстановителям и и в соединениях имеют только положительные степени окисления. Восстановительная активность различных металлов не одинакова. В периодах слева направо восстановительная активность уменьшается; в главных подгруппах сверху вниз – увеличивается. Восстановительная активность металлов в химических реакциях, которые протекают в водных растворах различных веществ, характеризуется положением металлов в электрохимическом ряду напряжений металлов. Металлы являются восстановителями и вступают в химические реакции с различными окислителями.
Альдегиды – органические вещества, содержащую функциональную группу (альдегидную группу). Альдегидная группа Карбонильная группа Гомологический ряд Н СН3 С2Н5 С3Н7 Физические свойства Формальдегид – газ, его 40% раствор называется формалином. Остальные жидкие и твёрдые. Химические свойства 1. Реакция «серебряного зеркала», качественная реакция CH3 укс. альдегид укс. кислота 2. С гидроксидом меди CH3 3. Восстановление водородом CH3 этанол Получение 1. Окисление спиртов R – CH2 – O + H + O à R 2. Окисление метана СH4 + O2 à H 3. Окисление метанола 2CH3OH + O2 à 2H
4. Гидратация ацетилена H – С 5. --------------------------------
|
||||||||
|
Последнее изменение этой страницы: 2017-02-22; просмотров: 200; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.136.170 (0.015 с.) |


 (при температуре)
(при температуре)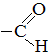 2. Альдегиды
2. Альдегиды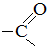
 + 2Ag
+ 2Ag C – H + H2O à CH
C – H + H2O à CH 


