
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Залежність теплоти фазових переходів від температури
Молярна теплота фазового переходу – це кількість теплоти, яка необхідна для переходу одного моля речовини з агрегатного стану, стійкого при низькій температурі, в агрегатний стан, стабільний при вищій температурі.
Приклад 11. Визначити молярну теплоту фазового переходу при плавленні олова при Т= 505 К. Розв’язок. Процес плавлення можна представити наступним чином: При наближених розрахунках: З довідника виписуємо, що При точному розрахунку необхідно користуватися рівнянням Кірхгофа:
Слід зауважити, що Другий закон термодинаміки та його застосування до фізико-хімічних процесів Зміна ентропії в фізичних процесах 1. Нагрівання при сталому тиску:
а) при розрахунках в невеликому інтервалі температур можна прийняти, що
б) при точному розрахунку потрібно враховувати залежність теплоємності від температури:
Приклад 12. Розрахувати наближену ентропію кристалічного магнію при Т = 700 К. Розв’язок. Виписуємо з довідника:
Користуючись рівнянням (1.26), запишемо:
2. Зміна ентропії при фазових переходах (агрегатних перетвореннях) чистих речовин
Ентропія при фазових переходах змінюється стрибкоподібно. При цьому, якщо фазовий перехід відбувається в напрямі зростання температури, ентропія також зростає ( Приклад 13. Визначити зміну ентропії при плавленні олова при Т= 505 К. З попереднього прикладу виписуємо, що
3. Зміна ентропії в результаті ізотермічного розширення ідеального газу
Абсолютна ентропія Абсолютна ентропія – це ентропія речовини при заданій температурі, яка розрахована від її нульового значення при абсолютному нулі температур. Абсолютна ентропія є сумою змін ентропії при нагріванні речовини від 0 К до заданої температури, а саме: змін ентропії при нагріванні твердої речовини від температури абсолютного нуля до температури плавлення, при переході з твердого в рідкий стан, при нагріванні рідини від температури плавлення до температури кипіння, внаслідок випаровування при температурі кипіння та при нагріванні пари від температури кипіння до заданої Т.
Ентропія індивідуальної кристалічної речовини у вигляді ідеально твердого тіла (тверда речовина з ідеальними кристалічними ґратками, де всі ґрати зайняті атомами чи молекулами) при абсолютному нулі дорівнює нулю.
Згідно з постулатом Планка абсолютна ентропія одного моля газоподібної речовини при температурі Т буде дорівнювати сумі зміни ентропії при переході речовини з одного агрегатного стану в інший при нагріванні твердої, рідкої та газоподібної речовини від абсолютного нуля до температури Т. Тоді можливі такі процеси:
тоді
де Приклад 13. Визначити зміну ентропії в результаті нагрівання 1 моля PbO(черв.) при Р = 1 атм від 298 К до 2000 К (
Розв’язок. Користуючись рівнянням (1.33) сумарна зміна ентропії буде становити:
У відповідності з рівнянням (1.32) абсолютне значення ентропії буде виражатися як Цей процес схематично можна представити наступним чином: 1) згідно з рівнянням (1.26) нагрівання
згідно з рівнянням (1.28) поліморфне перетворення
2) нагрівання
3) фазове перетворення
4) нагрівання
5) фазове перетворення
6) нагрівання пари до 2000 К у відповідності з рівнянням (1.26)
Ентропія при нагріванні від 298 К зростає майже в 3,3 рази. Збільшення ентропії за рахунок нагрівання становить
|
|||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 481; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.61.119 (0.008 с.) |
 .
.
 .
.

 , а
, а  . Звідси
. Звідси  .
. або
або  , якщо Т1 = 298 К
, якщо Т1 = 298 К .
.
 > 0, якщо здійснюється перехід із фази стійкої при низькій температурі, у фазу, стійку при вищій температурі (плавлення, випаровування, сублімація).
> 0, якщо здійснюється перехід із фази стійкої при низькій температурі, у фазу, стійку при вищій температурі (плавлення, випаровування, сублімація). .
.
 = const, тоді інтегрування цього рівняння дає:
= const, тоді інтегрування цього рівняння дає: .
.
 – для неорганічних речовин.
– для неорганічних речовин.


 .
.
 > 0), а при зворотних процесах (конденсація, кристалізація) зменшується (
> 0), а при зворотних процесах (конденсація, кристалізація) зменшується ( . У відповідності з рівнянням (1.28) знаходимо:
. У відповідності з рівнянням (1.28) знаходимо: .
.

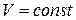




 Зміна ентропії в цьому процесі буде така:
Зміна ентропії в цьому процесі буде така: , оскільки
, оскільки 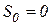 ,
,

 – теплоти поліморфного перетворення, плавлення та випаровування речовини;
– теплоти поліморфного перетворення, плавлення та випаровування речовини;  – температури поліморфного перетворення, плавлення та кипіння;
– температури поліморфного перетворення, плавлення та кипіння;  – відповідно молярні теплоємкості модифікації
– відповідно молярні теплоємкості модифікації  та
та  твердого, рідкого та газоподібного стану речовини.
твердого, рідкого та газоподібного стану речовини. ) та абсолютне значення при 2000 К
) та абсолютне значення при 2000 К  , якщо:
, якщо: ;
; 
 ;
; 
 ;
;  ;
;  ;
; 
 ;
;  ;
;  .
.
 .
. до
до 


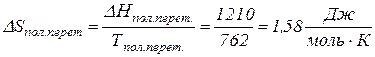 ;
; до
до 


 ;
; до
до 
 ;
;
 ;
;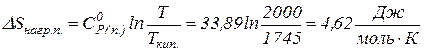

 .
. , за рахунок поліморфного перетворення
, за рахунок поліморфного перетворення 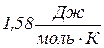 , плавлення
, плавлення  , випаровування
, випаровування  . Тобто
. Тобто  <
< 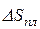 <
<  .
.


