
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Закон Бойля–Мариотта для суміші газів.
Для обчислення парціальних об'ємів за законом Бойля–Мариотта для всіх газів, що входять в суміш
Рівняння полягання суміші газів
Є суміш з n газів, що підкоряються рівнянню стану газу. Суміш займає об'єм Vсм, м3, при тиску Рсм, Па, і температурі Тсм К. Грунтуючись на законі Дальтона, можна для кожного газу написати рівняння стану
де Ri – питома газова постійна i-того компоненту, Дж/(кг К).
Формули для розрахунку газових сумішей.
Залежність між масовими і об'ємними частками можна одержати для i-того компоненту таким чином.
Густини компоненту і суміші повинна бути узяті при тиску і температурі суміші. Аналогічно рівнянням (2.6) і (2.7) можна одержати рівняння
Оскільки μ, кг/кмоль, обернено пропорційно до R, Дж/(кг К), то можна записати
Або
але, так як
то
Якщо склад суміші заданий числом кіломолів, то це рівнозначно завданню її об'ємними частками. Формули для визначення парціального тиску матимуть різний вигляд залежно від того, в яких частках задана суміш. Якщо суміш задана об'ємними частками, то з рівняння (2.4) виходить
Якщо суміш задана масовими частками
и
Завдання на самостійну роботу:
1. Поняття парціального об'єму i-того компоненту; 2. Вивід рівняння для розрахунку газової постійної для суміші газів; 3. Вивід основних формул для розрахунку газових сумішей; 4. Доказ того, що завдання суміші числом кіломолей однаково завданню її об'ємними частками.
Питання для самоперевірки:
Лекція 3
Тема. Основні поняття теплообміну. Тепловий баланс
План лекції:
3.1. Рівняння теплового балансу; 3.2. Закон Фур’є; 3.3. Диференціальне рівняння теплопровідності; 3.4. Теплопровідність при стаціонарному режимі і граничних умовах першого роду через одношарову плоску стінку; 3.5. Конвективний теплообмін; 3.6. Коефіцієнт тепловіддачі. Диференціальне рівняння конвективного теплообміну; 3.7. Теплопередача; 3.7.1. Передача теплоти через багатошарову плоску стінку.
Кількість тепла, що передається в одиницю часу від одного тіла до іншого називається тепловим потоком. При теплообміні між двома теплоносіями відбувається зменшення ентальпії гарячого теплоносія і збільшення ентальпії холодного теплоносія. Хай кількість гарячого теплоносія, його початкова і кінцева ентальпія рівні відповідно G, кг/с, і I, Дж/кг, холодного g, кг/с, та i, Дж/кг. Кількість тепла, що передається від гарячого теплоносія до холодного складає Q, Вт, – ця величина називається тепловим навантаженням, а втрати тепла в оточуючу середовище Qв, Вт.
Тоді рівняння теплового балансу запишеться у вигляді
или
Якщо знехтувати Qв, то
або
Якщо в апараті відбувається охолоджування гарячого теплоносія, то
I1=cг T1; I2=cг T2,
де сг – питома теплоємність гарячого теплоносія, Дж/(кг К); Т1 та Т2 – температури теплоносія на вході в апарат і виході з нього
аналогічно
де сх – питома теплоємність холодного теплоносія, Дж/(кг·К); t1 та t2– температури на вході в апарат і виході з нього,ºС; ΔТ та Δt температурні перепади, ºС; W і w називаються водяними еквівалентами, Вт/К.
При конденсації пароподібного теплоносія величини I1 та I2 в рівнянні (3.1) є відповідно ентальпією поступаючої пари і конденсату, що йде. Якщо пара поступає перегрітим з температурою Т1 то величина G I1 складається з ентальпії рідини при температурі насичення Тн, тепла, що витрачається на випаровування рідини і рівного теплу конденсації пари Qконд, а також тепла Qпер, необхідного для перегріву пари, тобто
Величина
где Т2 – температура конденсату, що йде, ºС. Тоді рівняння (3.3) запишеться
Тепло, що віддається при охолоджуванні перегрітої пари, рівно теплу, що затрачується на перегрів при його отриманні, і складає
Тепло, що віддається при конденсації пари, рівно теплу, що витрачається на випаровування рідини
Тепло, що віддається при охолоджуванні конденсату, складає
У цих рівняннях сп та сж– питомі теплоємності пари і рідини, Дж/(кг К); r – теплота випаровування, Дж/кг. При конденсації насиченої пари без охолоджування конденсату
Закон Фурье.
Для розповсюдження теплоти в будь-якому тілі або просторі необхідна наявність різниці температур в різних точках тіла. Зв'язок між кількістю теплоти,
де Кількість теплоти, що проходить через одиницю изотермной поверхні в одиницю часу, називають щільністю теплового потоку q, Вт/(м2·с)
|
||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 177; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.213.214 (0.019 с.) |
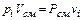 , (2.4)
, (2.4)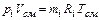 (2.5)
(2.5)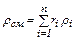 (2.6)
(2.6)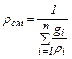 (2.7)
(2.7)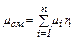 (2.8)
(2.8)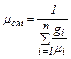 (2.9)
(2.9)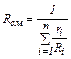 (2.10)
(2.10)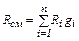 (2.11)
(2.11)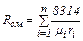 (2.12)
(2.12)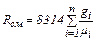 (2.13)
(2.13)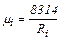 ,
,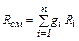 (2.14)
(2.14)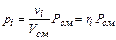 (2.15)
(2.15)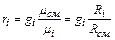 (2.16)
(2.16)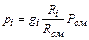 (2.17)
(2.17)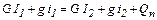 (3.1)
(3.1)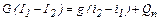 (3.2)
(3.2)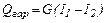 (3.3)
(3.3)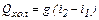 (3.4)
(3.4)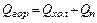 (3.5)
(3.5)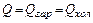 (3.6)
(3.6)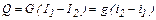 (3.7)
(3.7)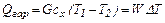 (3.8)
(3.8)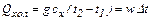 (3.9)
(3.9)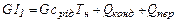 (3.10)
(3.10)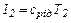
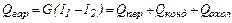 (3.11)
(3.11)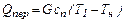 (3.12)
(3.12)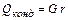 (3.13)
(3.13)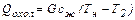 (3.14)
(3.14)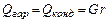 (3.15)
(3.15)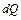 Дж, що проходе через елементарну площу,
Дж, що проходе через елементарну площу, 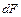 м, розташовану на ізотермній поверхні за проміжок часу,
м, розташовану на ізотермній поверхні за проміжок часу, 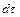 , с, і градієнтом температури,
, с, і градієнтом температури, 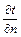 , С/м, встановлюється законом Фурье
, С/м, встановлюється законом Фурье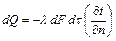 (3.16)
(3.16)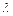 – коефіцієнт теплопровідності, Вт/(м К).
– коефіцієнт теплопровідності, Вт/(м К).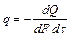 или
или 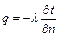 (3.17)
(3.17)


