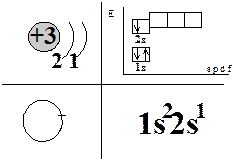Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Слайд №4. Схемы строения атома водорода. ⇐ ПредыдущаяСтр 5 из 5
Эти записи содержат одинаковые сведения: химический знак элемента, заряд ядра его атома число энергетических уровней и число электронов на каждом из них. Чтобы установить связь между строением атома химического элемента и его свойствами, рассмотрим еще несколько химических элементов. Посмотрите на экран мультимедиа проектора и по компьютерной программе “Таблица химических элементов и их свойства”, скажите мне, какой химический элемент находится сразу за водородом? Следующий за водородом гелий — инертный элемент. Он не образует соединений с другими элементами, а значит, валентности не проявляет. Посмотрите на схему (Слайд №5) и попробуйте описать данный элемент? Ядро атома гелия имеет заряд +2; вокруг него движутся 2 электрона, образуя один электронный уровень. Атомы гелия не образуют соединений с атомами других химических элементов, это говорит о большой устойчивости его электронной оболочки. Внешние электронные оболочки атомов гелия и других инертных газов называют завершенными. Вы познакомились со строением и свойствами водорода и гелия — элементов первого периода периодической системы химических элементов Д.И. Менделеева.
Слайд №5. Схемы строения атома гелия. Следующий элемент, который мы рассмотрим — литий.
В атоме лития 3 электрона. Два из них находятся на первом, ближнем к ядру электронном слое, а третий образует второй, внешний электронный слой (Слайд 6). Слайд №6. Схемы строения атома лития. Значит, в атоме лития, химического элемента второго периода, появился второй электронный слой. Находящийся на нем электрон слабее связан с ядром, чем два других. В соединениях атомы лития имеют постоянную валентность равную 1.
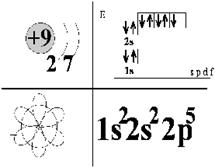
Слайд №7. Схемы строения атома фтора. Найдите в периодической системе химический знак лития, от лития до неона Ne закономерно возрастает заряд ядер атомов. Постепенно заполняется электронами второй слой. С ростом числа электронов на втором слое металлические свойства элементов постепенно ослабевают и сменяются неметаллическими. Фтор — самый активный неметалл, в его атоме два электронных слоя, содержащих соответственно 2 и 7 электронов (Слайд 7). За фтором следует неон Ne (Слайд 8). По свойствам эти элементы резко отличаются. Неон инертен так же, как и гелий, не образует соединений. Второй электронный слой содержащий восемь электронов, является завершенным. Это значит, что электроны образовали устойчивую систему, придавая атому инертность (неспособность образовывать химические соединения).
|
||||||||||||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 126; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.55.14 (0.006 с.) |