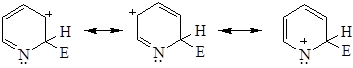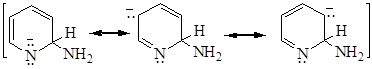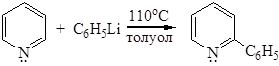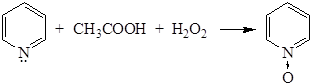Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физические свойства, строение⇐ ПредыдущаяСтр 17 из 17
Пиридин – бесцветная жидкость с неприятным запахом, т. кип. 115,5°С, растворим в воде, плотность больше 1. Пиридин – шестичленный гетероароматический аналог бензола. Его плоская молекула имеет сопряженную систему из 6 π-электронов. Все атомы цикла находятся в состоянии sp2-гибридизации и вносят по одному р-электрону в ароматический секстет. Ввиду большой электроотрицательности атома азота электронная плотность в молекуле смещена в сторону азота, и пиридин является электронодефицитным гетероциклом. У атома азота есть неподеленная пара электронов, которая обуславливает основные свойства пиридина. Пиридин инертен к электрофильным реагентам и обладает повышенной склонностью к реакциям с нуклеофилами. Химические свойства Из рассмотренного выше строения пиридина следует, что для него возможны реакции присоединения, основные свойства, реакции замещения. 1. Электрофильное замещение в пиридине протекает по β-полжению. Хлорирование
Электрофильный реагент первоначально атакует атом азота, имеющий неподеленную пару электронов, тем самым еще больше увеличивая положительный заряд в кольце пиридина, затрудняя реакцию электрофильного замещения. 2) Бромирование. Реакция идет в жестких условиях
Сульфирование
Нитрование
Если температура выше 400°С, можно получить с невысоким выходом 2-нитропиридин. Преимущественная атака в положение 3 связана с меньшим по величине положительным зарядом на атоме углерода, чем в положениях 2 и 4:
Кроме того, σ-комплекс при замещении в положение 3 может быть описан набором более выгодных резонансных структур, чем при замещении в положения 2 и 4 (отсутствует положительный заряд на атоме азота). Атака в положение 3:
Атака в положение 2:
Реакции алкилирования и ацилирования пиридина невозможны. Нуклеофильное замещение Ароматическое кольцо молекулы пиридина обеднено электронной плотностью, это облегчает реакции нуклеофильного замещения. В отличие от бензола пиридин легко реагирует с нуклеофильными реагентами, причем атака идет по положениям 2 и 4. 1) Аминирование пиридина (реакция Чичибабина)
Механизм реакции Чичибабина:
σ-комплекс может быть описан набором резонансных структур:
2- и 4-аминопиридины способны к таутомерным превращениям:
Реакция с гидроксидом калия
2-гидроксипиридин также способен к таутомерии:
3) реакция с литийорганическими соединениями протекает аналогично:
Реакции пиридина как основания 1) Взаимодействие с минеральными кислотами. Пиридин обладает слабыми основными свойствами, К = 1,7·10-9. С минеральными кислотами дает соли:
2) Алкилирование по азоту. Пиридин легко алкилируется по азоту с образованием N-алкилпиридиновых оснований:
3) Образование N-окисей. При нагревании пиридина с уксусной кислотой и перекисью водорода образуется N-окись пиридина:
N-окись в отличие от пиридина значительно легче вступает в реакции электрофильного замещения. Применение Пиридин используют в качестве растворителя, для получения пестицидов, лекарственных веществ, пиперидина, аминопиридина. ХИНОЛИН Хинолин состоит из сконденсированных бензольного и пиридинового колец.
Хинолин входит в состав алкалоидов. Хинолиновые основания – бесцветные жидкости с характерным запахом. В воде растворимы меньше, чем пиридин и его гомологи. Способы получения Синтез Скраупа
На первой стадии происходит конденсация анилина с акролеином, затем дегидратация и дегидрированное окисление. Если взять в качестве исходного соединения уксусный альдегид, то в результате реакции образуется 2-метилхинолин:
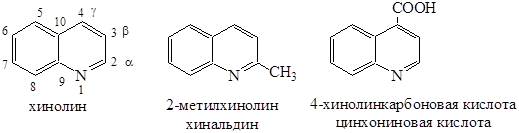
Строение хинолина
Влияние атома азота на бензольное кольцо выражено слабее, чем на пиридиновое кольцо. Реакции электрофильного замещения протекают легче, чем в пиридине. Также протекают реакции нуклеофильного замещения, и хинолин проявляет основные свойства, как пиридин. Химические свойства Основные свойства Образование солей с минеральными кислотами
Образование N-окисей
Реакции электрофильного замещения Нитрование
Сульфирование
Ацилирование и формилирование провести не удается, так как используемые агенты являются слабыми электрофилами. Нуклеофильное замещение Аминирование
Реакция с гидроксидом калия
Алкилирование
Окисление
|
||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 908; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.115.120 (0.012 с.) |