
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
усиление химического сигнала ⇐ ПредыдущаяСтр 3 из 3
Эффект регуляции характеризуют, с одной стороны, коэффициент усиления, а с другой стороны, полнота использования потенциальной производительности регулируемого белка или молекулярного комплекса (важно, чтобы синтезированный белок использовался, т.к. иначе он бесполезно занимает часть объёма клетки и разрушается со временем). Полноту использования потенциальной производительности выражает непосредственно Y: при малом Y работает лишь небольшая часть регулируемого белка. Значение коэффициента усиления непосредственно из полученных общих формул для связывания с несколькими молекулами регулятора (в соответствие с его определением) выражать неудобно в силу громоздкости вычислений и необозримости результата. Зависимость степени насыщения от двух основных факторов: числа молекул регулятора и наличия релаксированного состояния, можно получить, считая одинаковыми константы равновесия для различных этапов присоединения субстрата. Тогда выражению для степени насыщения (которая в общем виде позволяет представить многие возможности регуляции, обсуждаемые в РМ, Биофизике и т.д.)
где: – произведение Kс обозначено как a (где ki/k–i = K); – константа для перехода между ненапряженной и напряженной конформациями белкового комплекса обозначена как L = k+/k–; – учтена комбинаторика с точки зрения возможностей заполнения свободных мест связывания при соответствующем числе уже заполненных – РМ, с.; Биофизическая химия, с.). Наличие ненапряженного состояния (которое дает слагаемое L в знаменателе) обеспечивает многие возможности регуляции. Удобно сразу рассмотреть случай L >> 1, т.к. промежуточные значения L дают промежуточные возможности в сравнении с малыми L (т.е. практическим отсутствием такого состояния), когда многие возможности регуляции отсутствуют, в чем легко убедиться, проведя вычисления. (Д) графически зависимости такого вида при L около 100 при n = 3 представлены в РМ, с. 149 для фосфофруктокиназы (ФФК), фермента регулирующего скорость гликолиза
Эффект различия констант можно проанализировать на простейшем случае двух центров связывания (с двумя молекулами регулятора). Важная промежуточная задача: какую степень сигмоидности можно обеспечить в схеме с двумя этапами
В рассматриваемых схемах наибольшее значение коэффициента усиления (как отношения U = (∆Y/Y)/(∆ c / c)достигается на степенном участке зависимости Y(c), где абсолютное значение степени насыщения относительно невелико, т.е. доля активных молекул белка невелика. Тогда регулируемая скорость далека от максимального значения, а значит, эффективность его использования не высока. Следствие: в простых схемах коэффициент усиления низкий, если стоит задача не терять максимальных значений
Более дорогой способ еще больше увеличить усиление – вычитание скоростей противоположно направленных процессов (как есть и в данном примере с ФФК), каскады или некоторая специфическая кооперативность.
Общий вывод: в простых схемах трудно обеспечить высокое усиление без потери эффективности, отсюда при потребностях в большом усилении сложные энергозатратные решения (футильные циклы, каскады и т.д.)
Обещанная связанность при регуляции энергетического метаболизма: Важно, что сначала происходит превращение слабого сигнала (как относительно малого изменения концентрации АТФ) в большое изменение концентрации АМФ (350-кратное усиление), а затем дополнительное усиление большого изменения концентрации АМФ в изменение регулируемой скорости (ФФК регулирует скорость гликолиза). А креатинфосфат стабилизирует концентрацию АТФ, пока не произойдет включение гликолиза в результате этой регуляции. Упражнение: оцените, как изменится общее усиление, если поменять местами этапы усиления. Как количественно оценить эффект наличия стабилизирующего пула креатинфосфата (что изменится, если заменить креатинфосфат на АТФ в отношении 1 молекула на одну)
+ в этом же полугодии были объяснения к «физиологии»: содержание CO2 в крови высота прыжков скорость подъема вверх
Е полугодие 11.1.14 к/р №2 Вариант 1. 1. Связывание с кислородом гемоглобина (Hb) и миоглобина (Mb) представлено в таблице: Таблица (Кантор, Шиммел, «Биофизическая химия», т.3, с. 104)
Можно ли по этим данным сравнить, насколько «полезны» для переноса кислорода гемоглобин и миоглобин (если бы он заменял гемоглобин как переносчик в крови), если артериальная кровь насыщается в легких при давлении 100 Торр, а для венозной равновесная концентрация 30 Торр?
Считайте, что концентрация растворенного кислорода пропорциональна его давлению *Как можно проверить данные по связыванию миоглобина?
2. При САМ-метаболизме фотосинтез происходит как фиксация CO2 в форме органических кислот ночью при открытых устьицах листа или фотосинтезирующей ткани, с высвобождением фиксированного CO2 днем (при закрытых устьицах) с его включением в биохимические превращения (собственно фотосинтеза). Такой механизм позволяет не терять воду при фотосинтезе из-за ее испарения, т.к. устьица открыты только ночью, когда относительная влажность воздуха высока и приближается к 100%. Типичный пример САМ-растений – это всем известные кактусы (из которых делают текилу, они растут в мексиканских пустынях, где осадки выпадают не каждый год). Попробуйте оценить, сколько CO2 может связать литр объема ткани, если весь объем будет занят органической кислотой малатом (= яблочная кислота, формула HOOC–CHOH–CH2–COOH), из которой можно высвободить 1 моль CO2 на моль кислоты. Считайте, что плотность самой оргкислоты и ее раствора не отличаются от плотности воды.
Вариант 2. 1. Попробуйте оценить, сколько кислорода может связать литр объема ткани, если весь объем будет занят миоглобином?
2. Соединение, которое мы будем обозначать КФ, используется для замещения АТФ по реакции: КФ + АДФ = К + АТФ. Пусть константа равновесия такая, что в покое (при АТФ = 5мМ и АДФ = 0,1 мМ) отношение КФ/К = 4. Чему тогда равно значение константы равновесия? Какое соотношение КФ/К будет при нагрузке, когда АТФ уменьшается на 10%? Какой эффект замещения АТФ тогда будет достигнут? Почему в условии указано «соединение, которое мы будем обозначать КФ», а не креатинфосфат?
Дальнейшие занятия: Вопрос после задач на оценку запаса вещества в объеме при плотности, примерно равной плотности воды: почему нормальное содержание гемоглобина у человека 125–140 г/л (а не 500 г)? 18.1.14 сопротивления транспорту CO2 и кислорода: отношения потоков + тема сопряжения диффузионных потоков Описание на «языке сопротивлений» – полная аналогия закону Ома (поток молекул как сила тока, разность концентраций как разность потенциалов, сопротивление в газовой фазе как электрическое сопротивление) Пример: при фотосинтезе поток СО2 в лист связан с разницей концентраций СО2 в воздухе и межклеточном пространстве листа линейным соотношением A = (ca – c i)/ r, (1) где A –– скорость ассимиляции СО2, ca и c i –– концентрации СО2 соответственно в воздухе (индекс «а» от «air») и в межклеточном пространстве листа (индекс «i» от «intercellular»), а величина r (по аналогии с законом Ома) имеет смысл сопротивления транспорту СО2, а обратная ему величина g = 1/ r –– это проводимость в газовой фазе. Аналогичное соотношение E = (w i – wa)/ r ', (2) связывает скорость транспирации E (испарения воды, evaporation) с разницей концентраций паров воды (w) в воздухе и межклеточном пространстве (индексация та же, знак разности учитывает, что транспирационный поток направлен из листа в воздух, т.е. то, что, w i > wa) с тем отличием, что сопротивление для воды в 1.6 раза меньше, чем для СО2, т.е. r = 1.6 r '.
Коэффициент 1,6 учитывает все факторы, прежде всего, различие в молекулярной массе. В силу различия масс различается скорость, с которой молекулы идут по заданному пути. При одинаковой температуре скорость обратно пропорциональна корню квадратному из молекулярной массы (равны кинетические энергии различных частиц при заданной температуре). Для молекул H2O и CO2 отношение скоростей – это 1,56. Но есть и другие факторы: различие эффективного сечения молекул, вынос CO2 с транспирационным током (т.е. транспорт молекул не является чисто диффузионным.) и др. Обычно считают, что w i –– это насыщающая концентрация паров воды при соответствующей температуре, тогда D w = w i – wa –– это дефицит давления паров воды в воздухе. Сравнение потоков молекул H2O и СО2 по абсолютной величине дает отношение E (c i)/ A (c i)
E / A =1,6D w /(c a – c i). (3) При обычных условиях газообмена значение c a не превосходит 0,035%, т.е. 350 мкл/л (разность D c = c a – c i еще меньше, т.к. c i всегда порядка c a, в некоторых случаях даже близка к c a), а D w имеет порядок 10 мл/л. Учитывая такое соотношение числителя и знаменателя в правой части (3), потери воды измеряются в сотнях молекул в расчете на одну ассимилированную молекулу СО2.
Оглавление Занятия – их темы: как за счет связывания с белком большой молекулярной массы можно увеличить содержание кислорода (в сравнении с растворенной формой)
кривая связывания кислорода с миоглобином = кривая насыщения миоглобина
быстрая и медленная мускулатура – объяснения к «физиологии» Окштейна если превращать анаэробно, то 1 молекула АТФ «стоит» 60–90 Да (180 Да в глюкозе дают 2–3 АТФ) в сравнении с 507, если делать запас АТФ, или 3000, если запасать кислород, связывая его с белком (Hb или Mb)
кривая насыщения при двух центрах связывания, Y = (K2[O2] + 2[O2]2)/2(K1K2 + K2[O2] + [O2]2) вид для кривой насыщения гемоглобина
к/р №1
разбор задачи из к/р (Вариант 1, задача 2): строим график зависимости Y = (K2[O2] + 2[O2]2)/2(K1K2 + K2[O2] + [O2]2) при
эффект переноса кислорода в зависимости от кривой насыщения: выражение для потока аналогичная проблема при организации идеального переключателя и возможности при связывании с регулятором
получили, что нужно большое изменение концентрации (особенно для полного переключения – с использованием или выключением всех возможностей)
как получить большое изменение концентрации регулятора (как индикатора изменения ситуации)? биохимический усилитель АТФ-АДФ-АМФ
депо креатинфосфата
кооперативное переключение
+ были объяснения к «физиологии»: содержание CO2 в крови высота прыжков скорость подъема вверх
2-е полугодие к/р №2
Дальнейшие занятия: сопротивления транспорту CO2 и кислорода: отношения потоков
коэффициент диффузии в выражении для сопротивления
архитектура листа (как следствие негативной оценки)
Универсальность:
еще сопротивления и сопряжения: транспорт газов в яйце
циклическое дыхание насекомых
гидродинамические сопротивления крови
развитие 1: объяснение таблицы влажности (детальное равновесие + ЗСЭ: следствие – распределение частиц по энергиям)
абсолютные значения энергий связи и энергии активации в сравнении с кинетической энергией частиц
+ через численный счет к регуляции в количественном выражении (продолжение/соединение примеров с бактериофагом и кооперативной регуляцией)
развитие 2: экологические приложения, биохимические модификации C4-фотосинтеза, идея ОУФ и термодинамические потенциалы в C4-цикле
|
|||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 263; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.86.121 (0.045 с.) |
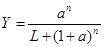 ,
,


