
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химические свойства гидроксидов
Be(OН)2 – амфотерный гидроксид: Be(OН)2 + SiO2 = BeSiO3 + H2O; Be(OН)2 + Na2O = Na2BeO2 + H2O; Be(OН)2 + 2HNO3 = Be(NO3)2 + 2H2O; Be(OН)2 + 2NaOH Be(OН)2 + 2NaOH = Na2[Be(OH)4]. Остальные гидроксиды – типичные основания. Mg(OH)2 – слабое основание. Ca(OН)2, Sr(OН)2, Ba(OН)2, Ra(OН)2 – сильные основания (щелочи). Щелочи взаимодействуют: С амфотерными элементами: Zn + 2H2O + Ca(OН)2 = Сa[Zn(OH)4] + H2; Zn + Ca(OН)2 С некоторыми неметаллами: 2 Ca(OН)2 + 2Cl2 = СaCl2 + Сa(ClO)2 + 2H2O;
Белильная известь 6Ca(OН)2 + 6Cl2 С кислотами (реакция нейтрализации): Ca(OН)2 + 2HCl = СaCl2 + 2H2O. С кислотными и амфотерными оксидами: Ca(OН)2 + SiO2 = СaSiO3 + H2O; Ca(OН)2 + ZnO = СaZnO2 + H2O. С амфотерными гидроксидами: Ca(OН)2 + Zn(OH)2 = СaZnO2 + 2H2O. С кислыми, основными солями: Ca(OН)2 + Ca(НCO3)2 = 2СaCO3 + 2H2O; 2CuOНCl + Ca(OН)2 = 2Cu(OН)2 + CaCl2. Со средними солями, если в результате образуется осадок: Ca(OН)2 + Na2SO4 = СaSO4↓ + 2NaOH. Гидроксиды термически неустойчивы, при нагревании разлагаются: Ca(OН)2 Способы получения оксидов металлов II A группы. Промышленный способ – прокаливание известняка: CaCO3 Лабораторные способы. Окисление металлов кислородом воздуха: 2Ca + O2 = 2CaO. Термическое разложение солей – нитратов и карбонатов: 2Mg(NO3)2 CaCO3 Способы получения гидроксидов металлов II A группы. В промышленности щелочи получают электролизом растворов хлоридов данных металлов: CaCl2 + 2H2O В лаборатории Ве(ОН)2 и Mg(OH)2 получают по обменной реакции: MgCl2 + 2NaOH ® Mg(OH)2↓ + 2NaCl; BeCl2 + 2NaOH(нед) ® Be(OH)2↓ + 2NaCl. Гидроксиды остальных металлов получают взаимодействием оксидов с водой: СаО + Н2О → Са(ОН)2. Жесткость воды Природная вода, содержащая ионы Ca2+ и Mg2+, называется жесткой. Жесткая вода при кипячении образует накипь на котлах, которая приводит к коррозии стенок котлов и выходу из строя оборудования, существенно повышает расход топлива. Жесткая вода не пригодна для стирки, моющие средства в ней не дают пены. В ней не развариваются пищевые продукты, а очень жесткая вода непригодна для питья. Единицы измерения жесткости воды в системе СИ – число молей эквивалентов ионов Са2+ и Mg2+, содержащихся в 1 м3 воды (или число миллимолей эквивалентов ионов Са2+ и Mg2+, содержащихся в 1 дм3 Н2О). Жесткость выражается в градусах жесткости (°Ж). 1°Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его моля на 1 м3 воды (или 1/2 его миллимоля на 1 дм3 воды).
Принято классифицировать жесткость воды следующим образом: – мягкая вода – 4,0°Ж и менее; – средняя жесткость – 4,0‒8,0°Ж; – жесткая вода – свыше 8,0°Ж. Карбонатная (временная) жесткость обусловлена присутствием в воде гидрокарбонатов кальция и магния, некарбонатная (постоянная) жесткость – хлоридов и сульфатов. Общая жесткость воды рассматривается как сумма карбонатной и некарбонатной. Удаление жесткости воды осуществляется путем осаждения из раствора ионов Ca2+ и Mg2+. Виды жесткости воды и способы ее устранения приведены в табл. 6.2. Таблица 6.2.
|
|||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 45; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.20.57 (0.004 с.) |
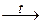 Na2BeO2 + 2H2O;
Na2BeO2 + 2H2O;
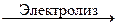 Са(ОН)2 + H2 + Cl2.
Са(ОН)2 + H2 + Cl2.


