
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общая характеристика d -элементов VI Б-группы.
Конфигурация валентных электронов Сг и Мо — (n-1)d5ns1, W — 5d46s2. Сумма валентных электронов хрома, молибдена, вольфрама равна 6, что и определяет их положение в VIБ-группе. У Сr и Мо последний электронный слой занимают 13 электронов, у W — 12. Как у большинства d-элементов этот слой неустойчив. Поэтому валентность хрома, молибдена и вольфрама непостоянна. По этой же причине соединения металлов группы VIБ характеризуются набором степеней окисления от +2 до +6. В группе d-элементов проявляется общая тенденция: с увеличением порядкового номера увеличивается устойчивость соединений с высшей степенью окисления. Самым сильным окислителем в состоянии Э6+ является хром. «Пограничный» Мо6+ проявляет слабые окислительные свойства. Молибде-нат-ион МоО42- восстанавливается лишь до Мо6О17 («молибденовая синь»), где часть атомов молибдена имеет степень окисления +5. Эта реакция используется в аналитической химии для фотометрических определений. В низших валентных состояниях, следуя все той же тенденции, более сильные восстановительные свойства проявляет Сг2+. У ионов Мо2+ и W2+ увеличение энергии ионизации приводит к уменьшению восстановительных и металлических свойств. Комплексные соединения данной группы элементов чаще всего имеют координационное число 6 и гибридизацию типа sр3d2, которая в пространстве описывается октаэдром. Характерной особенностью соединений этой группы является склонность к полимеризации (конденсации) кислородных форм элементов VI группы. Это свойство усиливается при движении по группе сверху вниз. При этом образуются соединения типа М6О2412-, составленные из октаэдров МоO4 и WO4. Эти октаэдры образуют полимерные кристаллы. У оксида хрома (VI) способность к полимеризации проявляется, но слабо. Поэтому у оксидов молибдена и вольфрама степень полимеризации выше.
По строению электронной оболочки атомов с незаполненной d-орбиталью, совокупности физических и химических свойств, по склонности к образованию электроположительных ионов и координационных соединений элементы VI группы относятся к переходным металлам. Химические свойства соединений хрома. Большинство соединений хрома имеет яркую окраску самых разных цветов. Название происходит от греч. хромоc — цвет, окраска. Соединения трехвалентного хрома (в отличие от соединений молибдена, а для вольфрама степень окисления +3 вообще не характерна) химически инертны. В природе хром находится в трехвалентном (шпинель — двойной оксид МnСrO4 — магнохромит) и шестивалентном состоянии (РbСrO4 — крокоит). Образует оксиды основного, амфотерного и кислотного характера. Оксид хрома (II) СrО — кристаллы красного (красно-коричневого) цвета или черный пирофорный порошок, нерастворимый в воде. Соответствует гидроксиду Сr(ОН)2. Гидроксид желтого (влажный) или коричневого цвета. При прокаливании на воздухе превращается в Сr2О3 (зеленого цвета): 2Сr(ОН)2 + 0,5О2 = Сr2O3 + 2Н2О Катион Сr2+ — бесцветен, его безводные соли белого, а водные — синего цвета. Соли двухвалентного хрома являются энергичными восстановителями. Водный раствор хлорида хрома (II) используется в газовом анализе для количественного поглощения кислорода: 2СrСl2 + 2НgО + 3Н2O + 0,5О2 = 2НgСl2 + 2Сr(ОН)3↓ (грязно-зеленый осадок) Гидроксид хрома (III) обладает амфотерными свойствами. Легко переходит в коллоидное состояние. Растворяясь в кислотах и щелочах, образует аква- или гидроксокомплексы: Сr(ОН)3 + 3Н3О+ = [Сr(Н2О)6]3+ (сине-фиолетовый раствор) Сr(ОН)3 + 3ОН- = [Сr(ОН)6]3- (изумрудно-зеленый раствор) Соединения трехвалентного хрома, как и двухвалентного, проявляют восстановительные свойства: Сr2(SO4)з+КСlО3 + 10КОН = 2К2СrO4 + 3К2SО4 + КСl + 5Н2О Соединения хрома (VI), как правило, кислородсодержащие комплексы хрома. Оксид шестивалентного хрома соответствует хромовым кислотам. Хромовые кислоты образуются при растворении в воде СrО3. Это сильно токсичные растворы желтого, оранжевого и красного цвета, обладающие окислительными свойствами. СrО3 образует полихромовые кислоты состава Н2СrnО(3n+1): nCrО3 + Н2О → Н2СrnО(3n+1). Таких соединений может быть несколько: Н2СrО4, Н2Сr2О7, Н2Сr3О10, Н2Сr4О13. Цвета растворов меняются от желтого до красного. Окраска зависит от содержания СrО3 в растворе, концентрация СrО3 влияет на образование полихромовых кислот разной степени полимеризации (от моно- до полихромовой кислоты).
Окислительные свойства дихромовой кислоты лежат в основе объемного оксидиметрического метода количественного анализа — хроматометрии. В методе применяется раствор сильного окислителя — дихромата калия. Государственная фармакопея рекомендует для определения подлинности раствора пероксида водорода использовать реакцию К2Сr2О7 + 4Н2О2 + Н2SО4 = К2SО4 + 2Н2СrО6 + 3Н2О При этом образуется дипероксохромовая (Н2СrО6) или пероксохромовая (НСrО5) кислота — соединение синего цвета. Синяя окраска и подтверждает подлинность препарата Н2О2. Хроматометрию применяют также в санитарно-гигиенической практике для анализа промышленных и сточных вод. В ходе анализа определяется «окисляемость воды», которая показывает общее содержание соединений восстановительного характера. СrО3 обладает прижигающим действием. Это свойство используется в медицине. Тем не менее, необходимо помнить, что соли хрома (III) и хрома(VI) токсичны для человека. Смертельная доза К2Сг2О7 для взрослого человека составляет всего 0,3 г.
|
||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 25; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.15.128.243 (0.005 с.) |
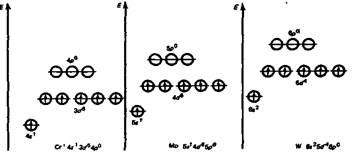
 VIБ-группу составляют элементы (переходные металлы) — хром, молибден и вольфрам. Эти редкие металлы находятся в природе в небольшом количестве. Однако благодаря целому ряду полезных химических и физических свойств, широко применяются не только в машиностроении и химической технологии, но и в медицинской практике (сплав Сr—Со—Мо используется в хирургии и стоматологии, молибден и его сплавы применяются как детали рентгеновских трубок, из вольфрама изготовляют аноды рентгеновских трубок, сплавы вольфрама — основа экранов для зашиты от γ-лучей).
VIБ-группу составляют элементы (переходные металлы) — хром, молибден и вольфрам. Эти редкие металлы находятся в природе в небольшом количестве. Однако благодаря целому ряду полезных химических и физических свойств, широко применяются не только в машиностроении и химической технологии, но и в медицинской практике (сплав Сr—Со—Мо используется в хирургии и стоматологии, молибден и его сплавы применяются как детали рентгеновских трубок, из вольфрама изготовляют аноды рентгеновских трубок, сплавы вольфрама — основа экранов для зашиты от γ-лучей).


