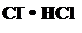Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
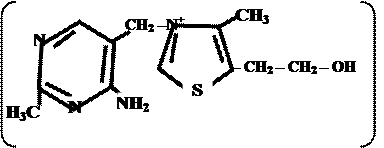
Витамины пиримидинтиазолового ряда и их производные
Тиамина бромид | |||||||||||
| Thiamini chloridum Thiamine Chloride * |
Thiamini bromidum Thiamine Bromide* | |||||||||||
| Vitaminum B1 | ||||||||||||
|
| |||||||||||
4-метил-5 β -оксиэтил- N -(2 ′ -метил- 4 ′ - амино-5 ′ -метилпиримидил)-тиазолий | ||||||||||||
| хлорида гидрохлорид | бромида гидробромид | |||||||||||
|
Свойства | ||||||||||||
| Белый кристаллический порошок | Белый или со слегка желтоватым оттенком кристаллический порошок | |||||||||||
| С ощутимым запахом. Легко растворимы в воде, мало растворимы в спирте. Устойчивы к сильно кислой среде и устойчивы к действию окислителей. Легко разрушается в щелочной среде с образованием тиохромной формы. | ||||||||||||
| Гигроскопичен | ||||||||||||
|
Подлинность | ||||||||||||
| 1. р-ция с NaOH, в качестве окислителя K3 [Fe(CN)6] → тиохром, который извлекается бутиловым (изоаминовым) спиртом. В УФ наблюдается синяя флюоресценция, которая изчезает при подкислении раствора и вновь появляется при подщелачивании. | ||||||||||||
| 2. экспресс анализ- р-ция с реактивом Неслера → желтое окрашивание → черное | ||||||||||||
| 3. с пикриновой к-той → желтый осадок | ||||||||||||
| 4. с р-ром йода → красно-коричневый осадок | ||||||||||||
| 5. с NaOH 15% → желтое окрашивание | ||||||||||||
| 6. сплав c кристаллическим NaOH→ разрушение с образованием S, которая определяется р-ром нитропруссида Na → красно-фиолетовое окрашивание | ||||||||||||
| 7. (на хлорид-ион) — АgNO3 → белый | (на бромид-ион) — АgNO3→ желтоватый | |||||||||||
| 8. (на бромид-ион – отличие) — с р-ром хлорамина + HCI + хлороформ → слой хлороформа окрашивается в желто- бурый цвет | ||||||||||||
|
Количественное определение | ||||||||||||
|
Метод неводного титрования (ГФ) Метод основан на усилении слабых основных свойств препарата при растворении его в растворителе протогенного характера. Методика: Тн пр-та растворяют в ледяной уксусной к-те + уксусный ангидрид+ индикатор кристаллический KBr и титруют 0,1 н р-ром хлорной к-ты до зеленого окрашивания [Thiam]•Cl•HCl + 2 HClO4 + Hg(CH3COO)2 → [Thiam]•2HClO4 + HgCl2 + 2 CH3COOH fэкв. = 1/2 M1/z = М/2 | ||||||||||||
|
Метод аргентометрии после нейтрализации Проводят нейтрализацию щелочью. Сумму бромид-ионов оттитровывают нитратом серебра. Расчеты ведут по разнице объемов (VAgNO3 – VNaOH) 2 AgNO3 [R3N]•Br•HBr + NaOH → [R3N]•Br + NaBr →
[R3N]•NO3 + 2 AgBr↓ + NaNO3 fэкв. = 1/2 M1/z = Mm/2 | ||||||||||||
|
Метод алкалиметрии Метод основан на вытеснении слабого органического основания более сильным минеральным Методика: Тн пр-та растворяют в воде + индикатор бромтимоловый синий и титруют 0,1 н р-ром NaOH → до голубовато- зеленого окрашивания | ||||||||||||
| [R3N]•Cl•HCl + NaOH → [R3N]•Cl + NaCl | [R3N]•Br•HBr + NaOH → [R3N]•Br + NaBr | |||||||||||
| fэкв. = 1 M1/z = 1 | ||||||||||||
|
Метод аргентометрии по Фаянсу Методика: Тн пр-та растворяют в воде + индикатор бромфеноловый синий и по каплям разведенную уксусную к-ту, титруем 0,1 н р-ром Ag NO3 до фиолетового окрашивания. | ||||||||||||
|
Применение | ||||||||||||
| - при нарушении функций нервной системы, невриты, неврозы; - при гипо- и авитаминозе витамина В1; - энцефалопатия; - пептическая язва желудка и ДПК; ФВ: р-р для инъекций, комплексные препараты. | ||||||||||||
|
Хранение | ||||||||||||
| В ХУТ, в защищенном от света месте без контакта с металлами (обр-ся неактивный дигидротиамин) | ||||||||||||
АЛКАЛОИДЫ
Это вещества основного характера, растительного реже животного происхождения. Получают синтетически.
Классификация алкалоидов
1. Производные пиридина и пиперидина (анабазин, никотин, лобелин)

N N
|
Н
2. Производные тропана (атропин, скополамин, гиосциамин))
 |
N – CH3
3. Производные хинолина (хинин)
 |
N
4. Производные изохинолина (все алкалоиды опия- папаверина г/хл, дротаверин)
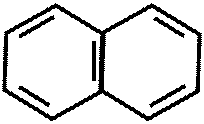

N 
5. Производные индола (резерпин, стрихнин)

N
|
Н
6. Производные пурина (теофиллин, теобромин, кофеин- обладают амфотерными свойствами)
 NH
NH
|
|
N
N N
Физические свойства
Алкалоиды-основания
Алкалоиды-соли -
Химические свойства
∙∙
R3N + H+X- → [R3N+]X-
|
H
R3N • HCl + NaOH → NaCl + R3N↓ + H2O
Общеалкалоидные реакции
1. Реактив Бушарда, Вагнера или Люголя (KI + I2= KI3 перйодид калия) р-ция выполняется в кислой среде HCI – бурые осадки
2. Реактив Майера (HgI2 + КI = K2[HgI4] в нейтральной или слабокислой среде – осадки белые или желтоватые (исключение: кофеин и колхицин)
3. Реактив Драгендорфа (BiI3 + KI = K[BiI4] тетрайодависмутат калия) - осадки оранжевого цвета
4. Реактив Зонненштейна (H3PO4•12MoO3•2H2O – фосфорно-молибденовая к-та) сначала осадки желтого цвета → синие → зеленые (восстановление молибденовой к-ты). Это наиболее чувствительный реактив на алкалоиды.
5. Реактив Шейблера (H3PO4•12WO3•2H2O – фосфорно-вольфрамовая к-та) – белые осадки.
6. Раствор танина (свежеприготовленный 10%-ый водный раствор) – среда нейтральная или слабокислая - осадки белого цвета или желтоватые
7. Пикриновая кислота (1%-ый раствор) – желтые осадки (исключение: кофеин, теобромин, морфин).
8. Реактив Марки (раствор формалина в концентрированной серной кислоте) – разные окрашенные осадки
9. Реактив Фреде (раствор молибдата аммония (NH4)2MoO4 в концентрированной серной кислоте) – разные осадки
10. Реактив Марме (CdI2 + KI- йодид кадмия в йодиде калия) - дает желтые осадки.